Centrale Physique et Chimie 1 PSI 2021
| Thème de l'épreuve | Le feu et l'eau |
| Principaux outils utilisés | thermodynamique, diffusion thermique, mécanique des fluides, cristallographie |
| Mots clefs | combustion, conduction, Bernoulli, incendie, Reynolds, lance à incendie, perte de charge, Notre-Dame, plomb, bois |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)







Rapport du jury
(télécharger le PDF)




Énoncé obtenu par reconnaissance optique des caractères
Physique-chimie 1
PSI
4 heures Calculatrice autorisée
2021
Le feu et l'eau
Le 15 avril 2019, un violent incendie s'est déclaré dans la cathédrale de
Notre-Dame de Paris. La charpente
constituée de milliers de poutres provenant de chênes centenaires a entièrement
brulé, la flèche réalisée en plomb
s'est effondrée et la structure a été endommagée. Ce sujet traite quelques
points concernant cet incendie. Il est
constitué de trois parties.
Certaines questions peu ou pas guidées, demandent de l'initiative de la part du
candidat. Leur énoncé est repéré
par une barre en marge. Il est alors demandé d'expliciter clairement la
démarche et les choix effectués et de
les illustrer, le cas échéant, par un schéma. Le barème valorise la prise
d'initiative et tient compte du temps
nécessaire à la résolution de ces questions.
Certaines données numériques sont regroupées en fin d'énoncé.
I Le feu
Le processus de combustion est une réaction chimique d'oxydation d'un
combustible par un comburant (rôle le
plus souvent joué par l'oxygène de l'air). Pour des raisons cinétiques, la
combustion ne se produit que lorsque les
réactifs sont portés à une température élevée. Il est donc nécessaire de
fournir de l'énergie -- généralement sous
forme de transfert thermique -- pour amorcer la combustion. Un feu est ainsi la
résultante de la combinaison
de ces trois éléments (combustible, comburant et énergie). En cas de
suppression d'un élément de ce « triangle
du feu », la combustion s'arrête ou le feu ne prend pas.
I.A --- Démarrage d'une combustion
Cette sous-partie s'intéresse au rôle de la température dans le triangle du feu.
La réaction combustible-comburant est une réaction d'oxydation exothermique qui
dégage de l'énergie et auto-
entretient le feu.
Q 1. Rappeler la loi empirique d'Arrhenius et expliquer pourquoi la plupart des
réactions chimiques sont
accélérées par une augmentation de la température.
Q 2. Pour quelle phase (solide, liquide ou gaz) du combustible, l'amorçage
d'une réaction de combustion
devrait-il être plus aisé ? Justifier succinctement.
On appelle point d'auto-inflammation, la température à partir de laquelle une
substance s'enflamme spontané-
ment dans l'atmosphère normale. Pour une feuille de papier typique, le point
d'auto-inflammation est de 232 °C.
Le papier est ainsi facilement inflammable si l'on concentre, à l'aide d'une
loupe, les rayons du soleil sur une
feuille.
On place une feuille de papier noir (de masse surfacique o -- 100 g-m ? et de
capacité thermique massique
c=1,4kJ-K Lkg !) au foyer d'une lentille convergente de distance focale f" = 10
cm et de rayon r = 5 cm.
L'axe optique est dirigé selon la direction moyenne des rayons lumineux
solaires. La lentille absorbe environ
25% du rayonnement solaire dont le flux surfacique moyen est égal à 800 W-m ?.
Q 3. Déterminer la durée minimale nécessaire à l'auto-inflammation de la
feuille de papier, de température
initiale 20 °C, sachant que le Soleil est vu sous un diamètre angulaire
apparent a = 32 minutes d'arc.
Q 4. La durée réelle devrait-elle être plus importante ou plus faible ? Le
choix du papier noir est-il judicieux ?
I.B - Combustion du bois
Un solide, en particulier le bois, passe par plusieurs phases au cours de son
échauffement avant de bruler, avec
apparition des flammes. D'abord l'eau qu'il contient s'évapore autour de 100 °C
à la pression atmosphérique,
puis les constituants du bois commencent à se décomposer ; il s'agit du
phénomène de pyrolyse, généralement
observé entre 250 °C et 500 °C, qui conduit à la formation de gaz. C'est une
partie de l'énergie dégagée par la
combustion de ces gaz de pyrolyse dans le dioxygène de l'air qui permet de
perpétuer l'ensemble de ces étapes.
Lorsque le processus de pyrolyse est terminé et qu'il n'y a plus de substances
volatiles, il subsiste un résidu
charbonneux rougeoyant qui dégage encore beaucoup d'énergie, sa surface
extérieure atteignant 800 °C.
Le bois de chêne est composé principalement d'environ 25 % de lignine
(C49H4406) et 75% de carbohydrates
C,(H0),, (cellulose (CH:90;), et hemicellulose).
P037/2021-01-27 15:27:13 Page 1/10 (cc) BY-NC-SA
F3
«
( Imbrüûülés gazeux et
|
?
solides
|
Sortie de | |
l'humidité Rayon-
nement
Combustion des gaz
de pyrolyse
Combustion du
charbon
Cendres
/
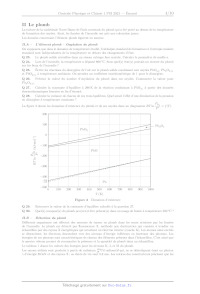
Figure 1 Différentes phases de combustion du bois!
Q 5. Une analyse élémentaire a fourni les pourcentages massiques respectifs en
élément carbone, hydrogène
et oxygène de 50%, 6% et 44%. Montrer que, si le bois pouvait être considéré
comme un corps pur, sa formule
chimique serait CH; 4406 66-
Dans la suite, on assimilera le bois à un corps pur de formule chimique brute
CH; 440 66:
Q 6. Écrire l'équation-bilan de la réaction de combustion du bois avec
l'oxygène de l'air. La combustion est
supposée complète et conduire à la formation de CO, et H,0.
On appelle pouvoir calorifique inférieur (PCI) l'énergie dégagée par la
combustion complète d'un kilogramme
de combustible à pression constante, l'eau produite étant sous forme de vapeur.
Q 7. Pour le chêne, on mesure un PCI de 19 MJ-kg"!. Quelle serait la valeur
numérique de l'enthalpie de
réaction de cette combustion ?
Q 8. En admettant qu'en fin de pyrolyse, les gaz libérés soient pour
l'essentiel du dihydrogène H, et du
monoxyde de carbone CO, retrouver, à partir des données tabulées, la valeur de
l'enthalpie standard de réaction
de la combustion de ces gaz de pyrolyse dans le dioxygène de l'air. Conclure.
Q 9. Dans une pièce calorifugée et fermée, initialement à 20 °C et de capacité
thermique totale de l'ordre
de 6,0 x 10° J-K !, brule une buche de bois de chêne de 1 kg. Quelle est la
température maximale atteinte dans
la pièce ? Commenter.
I.C --- Propagation de la chaleur dans le combustible
Q 10. Citer les trois modes de transfert thermique et donner leurs spécificités.
Q 11. Indiquer le rôle de chacun de ces modes dans la propagation d'un incendie.
On s'intéresse à l'avancée du front de combustion, au cours du temps, d'une
poutre qui entre en combustion par
l'une de ses extrémités. On fait l'hypothèse que les transferts thermiques dans
le bois sont de nature purement
diffusive.
La poutre en combustion est un parallélépipède, infiniment long dans la
direction (Ox). La température sur une
section transverse d'aire S de la poutre est supposée uniforme. On note T'(x,t)
la température à l'abscisse x de
la poutre à un instant t. On suppose que le feu prend à l'une de ses extrémités
d'abscisse nulle à un instant
pris comme origine des temps (4 = 0). À un instant t ultérieur, on estime, dans
ce modèle simple, que la poutre
peut-être découpée en trois zones (figure 2) :
-- Ja zone ayant brulé entre l'instant initial et l'instant t, dont la
température est supposée constante et égale
à la température 7°., dite température de combustion, 7°, = 720 K :
-- une zone dans laquelle se déroule la combustion ;
-- la zone encore inaltérée.
On note x,(t) l'abscisse de la frontière entre la zone brulée et la zone de
combustion et x,(t) l'abscisse de la
frontière entre la zone de combustion et la zone inaltérée. Loin de x,(t), la
température est supposée constante
et égale à 7, = 320 K.
La température T(x,t) dans la zone en combustion et celle de la zone inaltérée
augmentent par diffusion au
cours du temps jusqu'à atteindre les températures de combustion 7°, et
d'inflammation du bois 7; = 520 K,
conduisant à l'avancement des frontières x, et x, au cours du temps. Ainsi,
tant que la poutre n'a pas fini de
bruler, on a toujours T{x,(t),t) =T,, et T{xo(t),t) =T..
?
Benoît BRANDELET. (2016). Caractérisation physico-chimique des particules
issues du chauffage domestique au bois. Thèse de
doctorat. Université de Lorraine.
P037/2021-01-27 15:27:13 Page 2/10 (CO) 8Y-Nc-SA |
section S
a
zone zone en zone
brulée combustion inaltérée
a Y
O T1 (4) Ta(t)
Figure 2 Schéma de la poutre à l'instant #
Les valeurs des conductivités thermiques, notées À, et des diffusivités
thermiques, notées D, du charbon et du
bois étant relativement proches, nous considérerons qu'elles sont égales dans
les trois zones. Nous prendrons
comme valeur de la diffusivité thermique D = 1.0 x 10 7 m2:8 !. On rappelle que
la diffusivité thermique d'un
matériau est le rapport entre sa conductivité thermique et sa capacité
thermique volumique à pression constante.
On note c, la capacité thermique massique à pression constante du bois dans la
zone de combustion, 4 sa masse
volumique et P, la puissance thermique massique correspondant à l'enthalpie de
réaction de combustion par
unité de masse de bois et par unité de temps. On donne P, = 4,0 x 10° W-kg * et
c, = 2,0 x 10° J-K *kg ?.
Q 12. Effectuer un bilan d'enthalpie sur un élément de longueur dx de poutre de
bois de section $ compris
entre x et x + dx, dans la zone de combustion. En supposant la loi de Fourier
applicable, en déduire l'équation
régissant l'évolution de la température T'(x,t) dans la zone de combustion.
Mettre cette équation sous la forme
OT O°T
-- = D-- +Kk
OL Ox?
en précisant les expressions de D et k en fonction des données du problème.
Q 13. De même, écrire l'équation régissant l'évolution de la température
T'(x,t) dans la zone non altérée.
On souhaite dans un premier temps vérifier si l'on peut se placer dans le cadre
simplifié de l'approximation des
régimes quasi stationnaires thermiques.
Q 14. Calculer la durée caractéristique 7, de diffusion thermique pour une
longueur d'une dizaine de cen-
timètres d'un tronçon de poutre. Comparer ce temps de diffusion à l'ordre de
grandeur de la durée 7, de
combustion d'une même longueur de poutre. Conclure.
On se propose de résoudre les équations précédentes sous forme d'une onde se
propageant dans la poutre. On
pose u = x -- ct où c est une constante positive et on effectue le changement
de variables tel que T'(x,t) = O(u).
Q 15. Donner une interprétation de la quantité c.
Q 16. Déterminer les équations différentielles régissant l'évolution de la
dérivée de 0(u) dans la zone inaltérée
et dans la zone en combustion.
Q 17. Montrer que la forme générale des solutions @;(u) (i -- 1, 2 ou 3) dans
chacune des trois zones
respectives peut s'écrire
O,(u) = a, pour üu < U}, C k Ou) = a2 + b3 exp (su) -- --U POUr Uy LU < Uo, C Ou) = a3 + ba exp (su) pour ü > Ua.
Q 18. Déterminer, en justifiant la réponse, les expressions de a, et a, en
fonction des données.
Q 19. Tracer l'allure de la fonction O(u) dans la poutre.
Q 20. Quelles conditions permettent d'obtenir les constantes a; , b, et bà ? On
ne cherchera pas à les expliciter
littéralement.
On montre que la constante c est solution de l'équation
c? c?
KD KD
On se propose de déterminer la valeur de c par une méthode graphique. La
représentation graphique de la
fonction x H In(1 -- x) est fournie en annexe.
Q 21. Déterminer une valeur approchée de c. Conclure.
Q 22. Estimer la durée de combustion complète d'un mètre de poutre.
P037/2021-01-27 15:27:13 Page 3/10 (C2) BY-Nc-SA |
II Le plomb
La toiture de la cathédrale Notre-Dame de Paris contenait du plomb qui a été
porté au dessus de la température
de formation des oxydes. Aïnsi, les fumées de l'incendie ont pris une
coloration jaune.
Les données concernant l'élément plomb figurent en annexe.
IT. A --- L'élément plomb --- Oxydation du plomb
On supposera que dans le domaine de température étudié, l'enthalpie standard de
formation et l'entropie molaire
standard sont indépendantes de la température en dehors des changements d'état.
Q 23. Le plomb solide cristallise dans un réseau cubique face centrée. Calculer
le paramètre de maille a.
Q 24. Lors de l'incendie, la température a dépassé 800 °C. Sous quel(s) état(s)
pouvait-on trouver du plomb
sur les lieux de l'incendie ?
Q 25. Écrire les réactions du dioxygène de l'air sur le plomb solide conduisant
aux oxydes PRO,,, Pb30, 4
et PbO,,, à température ambiante. On prendra un coefficient stwchiométrique de
1 pour le dioxygène.
Q 26. Préciser la valeur du nombre d'oxydation du plomb dans ces oxydes.
Commenter la valeur pour
Ph30, 4).
Q 27. Calculer la constante d'équilibre à 298 K de la réaction conduisant à
PbO,,, à partir des données
thermodynamiques fournies en fin d'énoncé.
Q 28. Calculer la variance de chacun de ces trois équilibres. Quel serait
l'effet d'une diminution de la pression
en dioxygène à température constante ?
©
La figure 3 donne les domaines d'existence du plomb et de ses oxydes dans un
diagramme RÀT In De = f(T).
200
I
PbO,
ne 0
S
= --100
es
. PbO
oIA
A. 200
=
=
--300
--400
--438
--448
--500
0 100 200 300 AOÛ 900 600 700 SUÙ 900 1000
T'(K)
Figure 3 Domaines d'existence
Q 29. Retrouver la valeur de la constante d'équilibre calculée à la question 27.
Q 30. Quel(s) composé(s) du plomb peu(ven)t être présent(s) dans un nuage de
fumée à température 500 °C ?
ITI.B -- Détection du plomb
Différents organismes ont effectué des mesures de teneur en plomb dans les
zones atteintes par les fumées
de l'incendie. Le plomb est détecté par fluorescence X, méthode non
destructrice qui consiste à irradier un
échantillon par des rayons X énergétiques qui arrachent un électron interne
(couche K). Les atomes ainsi excités
se désexcitent, les électrons descendent vers des niveaux d'énergie inférieurs
en émettant des photons. Les
énergies de ces photons sont caractéristiques de chacun des éléments présents
dans l'échantillon. C'est ainsi que
le spectre obtenu permet de reconnaitre la présence et la quantité de plomb
dans un échantillon.
Le tableau 1 donne les valeurs des énergies pour les niveaux K, L et M du plomb.
Les rayons utilisés sont produits à partir de cadmium }$°Cd radioactif qui, en
se désintégrant émet un photon
y d'énergie 88 keV et des rayons X ; sa durée de vie vaut 5,3 ans. Les notices
des constructeurs précisent que les
P037/2021-01-27 15:27:13 Page 4/10 (C2) 8Y-Nc-sA |
À
|
M
M,
o Y Y L
# La Le
D
a
SD
YY Y K
Kx Ks
à
Figure 4 Diagramme énergétique simplifié du plomb --
Les couches K, L et M correspondent respectivement à des
états de nombre quantique principal n = 1,2,3
Niveau K L M
Énergie (keV) --88,0 --14,3 --3,0
Tableau 1 Énergies pour les niveaux K, L et M de l'atome de plomb
appareils à source de cadmium détectent les raies K et L du plomb, alors que
les appareils à tube à rayons X
(énergie 15 keV) détectent les raies L du plomb mais pas les raies K.
Q 31. Justifier cette dernière assertion.
Q 32. Quelles sont les énergies libérées lors des passages des couches M, puis
L, au niveau fondamental ? Les
photons correspondants sont-ils visibles ?
Q 33. La figure 5 donne deux spectres obtenus pour un échantillon contenant du
plomb. L'abscisse est
l'énergie du rayonnement émis exprimée en keV. Quelles raies ces spectres
permettent-ils d'identifier ? Le modèle
simple proposé permet-il de rendre compte des deux raies à 10,5 keV et 12,6 keV
? Proposer une explication
possible pour l'existence de ces deux raies.
_Low Enersy Spectrum mean MlaxPeak: 6129 __High Enerey Spectrum (Y-lmear)
[laxPeak: 336
<-Pb=10.50 <-Pb=12.60 <- Pb = 74.20 CT LL A ireposraze Un L | : Ù 20 40 60 #0 100 1240 140 160 140 200 2440 440 0 490 530 590 610 650 690 730 770 #10 #50 #40 Figure 5 Spectres rayons X obtenus pour un échantillon de plomb III L'eau TIIT. À --- Extinction du feu Comme évoqué en première partie, éteindre un feu nécessite la suppression d'un élément du triangle du feu : le combustible, le comburant ou l'apport d'énergie nécessaire à l'amorçage de la combustion. L'eau, par ses deux effets, permet d'agir sur deux des éléments du triangle du feu : -- l'eau présente une grande capacité thermique et une enthalpie de vaporisation élevée, elle utilise de l'énergie pour se vaporiser. Elle peut donc « refroidir » le feu ; -- l'eau vaporisée remplace partiellement l'air, et donc le dioxygène, à proximité des gaz de pyrolyse et des flammes. Q 34. Vérifier dans un premier temps que la molécule d'eau ne se décompose pas en H, et O, à haute température. Q 35. Quelle est l'énergie nécessaire pour vaporiser à pression constante 1 kg d'eau initialement à 15 °C et de température finale 800 °C ? P037/2021-01-27 15:27:13 Page 5/10 (C2) BY-Nc-SA | Q 36. Les pompiers appellent puissance d'un feu l'énergie thermique qu'il dégage chaque seconde. On constate que, pendant l'aspersion d'eau, seulement un tiers de l'eau se vaporise. Estimer dans ce cas la puissance de feu que peut traiter une lance de débit 500 L:min *. Dans le cas de l'incendie de Notre-Dame, les pompiers ont estimé que la puissance du feu a atteint 1500 MW. Commenter. Q 37. Estimer la quantité d'eau réellement évaporée par minute, toujours pour un débit de 500 L:min !. En déduire le volume de vapeur d'eau produit par minute. ITI.B --- Lances à incendie Pour éteindre les feux, les pompiers utilisent des lances à incendie, reliées à de longs tuyaux acheminant l'eau depuis des fourgons ou des moto-pompes. Ces lances permettent de régler le débit et la forme du jet. Lors de l'incendie de Notre-Dame de Paris, le débit Q des lances utilisées était de l'ordre de 500 L:min ! et le diamètre d de 70 mm. Q 38. Estimer la valeur de la vitesse d'éjection V, du jet arrosant la charpente du chevet de la cathédrale situé le plus en avant sur la photographie présentée figure 6. On admettra que cette image ne présente pas de déformation de perspective. Figure 6 Photographie du chevet (côté Est) de Notre-Dame de Paris le soir de l'incendie Q 39. Comparer la valeur de V, à la vitesse de l'eau dans le tuyau et expliquer la différence observée. L'eau utilisée est pompée dans un camion-citerne ou fourgon-pompe stationné sur la route (figure 7). On appelle AP = P,-- PF, la différence de pression entre la sortie de la pompe (pression P,) et l'extrémité de la lance (pression P,). Q 40. En supposant le fluide parfait, quelle doit être, en régime permanent, la différence de pression pour que l'eau arrive au niveau d'une nacelle située à 30 m de hauteur ? En réalité, l'eau est visqueuse ; il est nécessaire de prendre en compte des frottements sur la paroi interne des tuyaux. Q 41. Pour le débit des lances étudiées, l'écoulement dans les tuyaux est-il laminaiïire ou turbulent ? Les frottements induisent une perte de charge (diminution de pression) lors du passage dans les tuyaux. La perte de charge linéique, notée J, est donnée par la formule de Darcy-Weisbach pV° J = f-- Ta où d est le diamètre intérieur du tuyau, V' la vitesse moyenne du fluide, p sa masse volumique et f un facteur pouvant dépendre du nombre de Reynolds et de la rugosité relative EUR/d. Q 42. Quelle est la dimension du facteur f ? P037/2021-01-27 15:27:13 Page 6/10 CIEL Les... se... ............... ss. nacelle T I -- LD 2 7) 7 pompe bouche d'incendie Figure 7 Schéma d'acheminement de l'eau depuis la prise d'eau jusqu'à la nacelle Pour un écoulement laminaire, le facteur f vaut f = 64/R, où R, est le nombre de Reynolds de l'écoulement. Si l'écoulement est turbulent, on utilise la formule de Colebrook 1 o c/d 4 2,51 7 -- -- OS ------ VW 3,7 RVf où EUR est la rugosité, c'est-à-dire la dimension moyenne des aspérités de la paroi interne du tuyau. Cette formule de Colebrok n'est pas soluble littéralement et les pompiers utilisent des abaques ou des tableaux qui donnent les pertes de charge. Le tableau 2 donne les pertes de charge en fonction du débit et de la longueur d'un tuyau de diamètre 70 mm. Longueur (m) Débit (L-min :) 40 80] 100! 120) 160, 200, 240! 280, 520, 360] 400 125 0,0! 0,0! 0,0! 0,0! O1) O,1! 0,1! O,1! O1! O1! 0,1 250 0,1) 0,1! 0,1! 0,2} 0,2! 0,3) 0,3! O4 0,4! 0,5) 0.6 375 0,1} 0,2] 0,2! 0,4 0,5, 0,6! 0,7/ 0,9 1,0! 1,1) 1,2 500 0,2! 0,4, 0,55, 0,7] 0,9! 1,1) 1,3 1,5) 1,8 2,0) 2,2 675 0,47 O,8[ 1,0! 1,2] 1,6/ 2,0) 2,4! 2,8] 3,2/ 3,6] 4,0 750 0,5! 1,0] 1,2} 1,5) 2,0) 2,5) 3,0! 3,5] 4,0] 45! 5,0 875 0,7/ 1,3, 1,7, 2,0] 2,7] 3,4) 4,0! 4,7) 54! 6,1] 6,7 1000 0,9! 1,8] 2,2! 2,61 3,5] 4,4 5,3) 6,2) 7,0! 7,9] 8,8 1250 1,4) 2,8] 3,4) 4,1! 5,5) 6,9! 8,3! 9,6! 11,0] 12,4) 13,8 1500 2,0) 4,0! 5,0! 5,9] 7,9) 9,9! 11,9) 13,9) 15,8! 17,8] 19,8 Tableau 2 Pertes de charge (en bar) en fonction du débit Q et de la longueur L pour un tuyau de diamètre d = 70 mm Q 43. débit de 500 L:min ? ? Q 44. un nombre de Reynolds de 5 x 10°. Commenter. Q 45. une longueur totale de 200 m ? Peut-il y avoir d'autres causes de perte de charge ? Q 46. D'après le tableau 2, le facteur f de la relation de Darcy dépend-il de la longueur du tuyau pour un Exploiter la formule de Colebrook afin de calculer la rugosité relative, £/d, d'un tuyau de 70 mm pour Quelle doit être la différence de pression AP si le tuyau qui alimente la lance en haut de la nacelle a En s'aidant d'un bilan de puissance, déterminer la puissance électrique minimale à fournir à la pompe pour obtenir une pression à la lance P, = 6 bar et un débit de 500 L:min ' dans les conditions décrites plus haut (hauteur de la nacelle 30 m, longueur du tuyau 200 m). On supposera que la pression d'alimentation de la pompe est de 1 bar (en réalité elle peut aller jusqu'à 16 bar pour les bouches d'incendie). Q 47. L''incendie a duré 15 heures et a mobilisé plus de 500 pompiers, appuyés par 18 lances supposées toutes identiques et de même débit 500 L:min *. Toutes les lances n'ont pas été en action pendant cette durée. En admettant que les lances ont été utilisées à leur maximum pendant 2 heures, quelle quantité d'eau a été déversée sur Notre-Dame ? Page 7/10 CEE P037/2021-01-27 15:27:13 Données Constantes et conversions de quelques unités Constante des gaz parfaits R = 8.31 J:mol !-K Constante d'Avogadro N 1 = 6,02 x 10% mol | Constante de Planck h = 6,63 x 107% Je Charge élémentaire e = 1,60 x 10 C Accélération normale de la pesanteur terrestre g =9.81mess ? Le faraday 1F = 9,65 x 10% C-mol La minute d'arc 1° = 1/60° Données atomiques Élément H C O Pb Numéro atomique I 6 8 82 Masse molaire (g-mol*) 1,0 12,0 16,0 207,2 Données thermodynamiques et autres caractéristiques Viscosité dynamique de l'eau (supposée indépendante de la température) : 7 = 1,0 x 10 * Pas. Masses volumiques dans les conditions usuelles de températures et de pression : eau liquide 1,0 x 10° kg-m * air 1,2 kg-m * Capacité thermiques dans les conditions usuelles de températures et de pression (on admet que ces grandeurs ne dépendent pas de la température) eau liquide Cp = 4180 Jkg !.K"! eau vapeur Cp = 1850 Jkg !.K°l air sec Cp = 1005 J-kg !.K°1 air saturé en vapeur d'eau Cp = 1030 J-kg !.K°l Enthalpie massique standard de vaporisation de l'eau à 100 °C : À,,, 4° = 2257 kJ kg" 1 Enthalpies de formation et entropies molaires standards à 298 K : Espèces À ;H° (kJ-mol") S°, (J-mol-K") H (4 0 130,5 Oyte 0 205,0 HO -285,1 70,0 HO, 21,8 188,7 C(graphite) 0 D,7 CO -110,6 197,6 CO: (9 -393,5 213,7 Pb, 0 64,5 PbO -218,0 66,5 PbO; (4 _277,1 68,0 PbS4 -100,4 1,2 PbyO( _719,0 211 SO» _296,9 248 P037/2021-01-27 15:27:13 Page 8/10 (C2) BY-Nc-SA | Données spécifiques à l'élément plomb et description de quelques oxydes Numéro atomique 82 Masse molaire 207,2 g-mol ! Masse volumique 11,35 g-cm * États d'oxydation 2 et 4 Température de fusion 327 °C Température d'ébullition 1749 °C Enthalpie molaire de fusion A;,, 1° 4,9 kJ:mol " Type |Couleur Masse volumique (kg-m *)| Évolution PbO jaune (litharge) 9500 décomposition entre 300 °C et 400 °C en Pb:0, Pb;0, lorange (minium) 9100 fusion et décomposition après 500 °C PbO, noir 9380 fusion et décomposition à 290 °C en Pb;,0, puis PbO PbCO; blanc (céruse) instable au-dessus de 400 °C en PbO, CO et CO, Représentation graphique de la fonction In(1 -- x) In(1 -- x) 0.5 0 --0,5 --] 1,5 2 _25 01 02 03 04 05 0,6 L La cathédrale Notre-Dame de Paris Principales dimensions de l'édifice : P037/2021-01-27 15:27:13 longueur largeur superficie intérieure hauteur des tours hauteur de la flèche hauteur de la façade sans les tours hauteur estimée de chaque arc-boutant Page 9/10 07 O8 127 m 48 m 4800 m° 69 m 96 m 45 m 30 m 0,9 CETTE VV en Haies de Balai CTm - One CRU Je À N + Z / " NU J ne + En 2 Pendr | ". lon. Car Gmnns, à E Pine 4 lo Lui que Sournt lomin -- à L a rs |, low 4 } LA 0 reve door / Feshraies DT TA Soie Ron dent Cao Que L ttc (id. LR GS Schéma réalisé par le dessinateur de la Brigade des Sapeurs-Pompiers de Paris. Les marques circulaires noires indiquent les positions des pieds des échelles coulissantes porte-nacelles ou BEA (bras élévateurs aériens). LE (rt Schéma de la cathédrale réalisé lors de l'incendie par René Dosne, pompier retraité. ee eFINeee P037/2021-01-27 15:27:13 Page 10/10
