Mines Chimie PSI 2025
| Thème de l'épreuve | Chimie et céramiques |
| Principaux outils utilisés | cristallographie, oxydoréduction, diagrammes E-pH, thermodynamique |
| Mots clefs | nitrure de bore, borazine, zirconium, carbure de zirconium |
| Sujet jumeau | Mines Chimie MP 2025 |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - -
Énoncé complet
(télécharger le PDF)



Rapport du jury
(télécharger le PDF)




Énoncé obtenu par reconnaissance optique des caractères
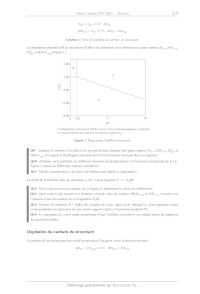
A2025 CHIMIE PSI ÉCOLE NATIONALE DES PONTS et CHAUSSÉES, ISAE-SUPAERO, ENSTA PARIS, TÉLÉCOM PARIS, MINES PARIS, MINES SAINT-ÉTIENNE, MINES NANCY, IMT ATLANTIQUE, ENSAE PARIS, CHIMIE PARISTECH - PSL. Concours Mines-Télécom, Concours Centrale-Supélec (Cycle International). CONCOURS 2025 ÉPREUVE DE CHIMIE Durée de l'épreuve : 1 heure 30 minutes L'usage de la calculatrice ou de tout dispositif électronique est interdit. Les candidats sont priés de mentionner de façon apparente sur la première page de la copie : CHIMIE - PSI L'énoncé de cette épreuve comporte 4 pages de texte. Si, au cours de l'épreuve, un candidat repère ce qui lui semble être une erreur d'énoncé, il le signale sur sa copie et poursuit sa composition en expliquant les raisons des initiatives qu'il est amené à prendre. . Les sujets sont la propriété du GIP CCMP. Ils sont publiés sous les termes de la licence Creative Commons Attribution - Pas d'Utilisation Commerciale - Pas de Modification 3.0 France. Tout autre usage est soumis à une autorisation préalable du Concours commun Mines Ponts. Chimie et céramiques Ce sujet propose d'aborder certaines propriétés des céramiques. Les trois parties du sujet sont totalement indépendantes. Les données utiles à la résolution du problème et les approximations de calcul sont fournies à la fin de l'énoncé (page 4). Il existe trois grandes classes de matériaux : les métaux et leurs alliages, les polymères organiques et les céramiques. Ces dernières sont des matériaux minéraux non métalliques qui peuvent être catégorisées en traditionnelles ou techniques. Les céramiques techniques et plus particulièrement les céramiques non-oxydes, telles que le nitrure de bore (BN), le carbure ou nitrure de silicium (SiC ou Si3 N4 ), ou le carbure de zirconium (ZrC) présentent des propriétés physico-chimiques intéressantes pour des applications hautes performances. Le nitrure de bore Le nitrure de bore (BN) peut être obtenu après traitement thermique d'un précurseur nommé le polyborazylène, obtenu par polymérisation d'un monomère cyclique, la borazine, de formule brute B3 N3 H6 . Les atomes de bore et d'azote forment de manière alternée un cycle à six chaînons. Le nitrure de bore peut cristalliser selon une structure de type blende : les atomes de bore décrivent une structure CFC dont la moitié des sites tétraédriques sont occupés par les atomes d'azote. Q1- Donner le nombre d'électrons de valence des éléments bore, azote et hydrogène. Q2- Dessiner la structure de Lewis de la borazine. Q3- Quelle est la géométrie autour des atomes de bore et d'azote ? Q4- Quel est du bore ou de l'azote l'élément le plus électronégatif ? Justifier votre réponse. Q5- Dessiner la maille du nitrure de bore (les atomes de bore seront représentés par un disque et ceux d'azote par une croix). Quelle est la nature des liaisons entre les atomes ? Q6- Déterminer le nombre d'atomes par maille pour chaque élément ainsi que leur coordinence, dont on précisera la définition. Q7- Calculer le paramètre de maille ! associé à cette maille, sachant que les atomes de bore et d'azote sont en contact mais pas les atomes de bore entre eux. Q8- Déterminer la masse volumique " du nitrure de bore. Le carbure de zirconium Le carbure de zirconium est une céramique ultraréfractaire, ultradure de formule chimique ZrC(s) . Il peut être préparé en utilisant une « voie poudre » à haute température par réaction entre le zirconium Zr(s) et le carbone C(s) via une synthèse autopropagée (self-propagating high-temperature synthesis), mais également par réduction, par le carbone, de la zircone, ou dioxyde de zirconium ZrO2 (s) (Schéma 1). Page 1/4 Zr(s) + C(s) ZrC(s) ZrO2 (s) + C(s) ZrC(s) + CO2 (g) Schéma 1. Voies de synthèse du carbure de zirconium. Le diagramme potentiel-pH du zirconium (E-pH) a été déterminé en se limitant aux quatre espèces Zr(s) , ZrO2 (s) , Zr4+ (aq) et HZrO3 (aq) (Figure 1). -1,00 B C E (V) -1,50 -2,00 A -2,50 -3,00 0 1,25 7 14 pH Le diagramme a été tracé à 298 K et sous 1 bar en solution aqueuse, en prenant les concentrations des espèces en solution égales à !! . Figure 1. Diagramme E-pH du zirconium. Q9- Indiquer le nombre d'oxydation du zirconium dans chacune des quatre espèces Zr(s) , ZrO2 (s) , Zr4+ (aq) et HZrO3 (aq) (l'oxygène et l'hydrogène sont dans leur état d'oxydation classique dans ces espèces). Q10- Attribuer, en le justifiant, les différents domaines de prédominance ou d'existence (numérotés de A à C, Figure 1) parmi les différentes espèces considérées. Q11- Quelle concentration '0 de tracé a été utilisée pour établir ce diagramme ? La droite de la frontière entre les domaines A et C a pour équation E = a + b.pH. Q12- Par le calcul (et non par lecture sur la Figure 1), déterminer la valeur du coefficient b. Q13- Quel serait le pH associé à la frontière verticale entre les espèces HZrO3 (aq) et ZrO2 (s) . Conclure sur l'absence d'une des espèces de ce diagramme E-pH. Q14- Donner les relations E = f(pH) des couples de l'eau, après avoir indiqué les demi-équations redox correspondantes (les pressions des gaz seront supposés égales à la pression standard )" ). Q15- Le zirconium Zr(s) est-il stable en présence d'eau ? Justifier, et écrire le cas échéant toutes les équations de réaction possibles. Oxydation du carbure de zirconium Le carbure de zirconium peut être oxydé en présence d'oxygène, selon la réaction suivante : ZrC(s) + 2 O2 (g) ZrO2 (s) + CO2 (g) Page 2/4 Q16- Indiquer, en le justifiant, le caractère endothermique ou exothermique de la réaction. Q17- Calculer l'entropie standard de réaction et justifier qualitativement son signe. Q18- Calculer l'enthalpie libre standard # + " de réaction à 300 K dans le cadre de l'approximation d'Ellingham. Q19- Déterminer la valeur de la constante d'équilibre , " de la réaction à 300 K. La réaction peut-elle être considérée comme totale ? Q20- Préciser, en justifiant la réponse, le sens de variation de la constante d'équilibre , " avec la température. Q21- Quelle est l'influence de la pression sur l'équilibre d'oxydation du carbure de zirconium ? Justifier votre réponse. Q22- Conclure quant aux conditions opératoires optimales pour cette réaction. Fin de l'épreuve Page 3/4 Annexes Annexe 1. Constantes usuelles et approximations de calcul. Constante d'Avogadro : -$ 6.1023 mol1. Constante des gaz parfaits : R 8 J·K1·mol1. %& On considèrera : 2 10/7 ; 3 7/4 et × ln x 0,06 × log x à 298 K. Annexe 2. Masses molaires et rayons atomiques. M(H) = 1 ; M(B) = 11 ; M(N) = 14. rB = 85 pm ; rN = 65 pm. Annexe 3. Potentiels standards d'oxydoréduction à pH = 0 et à 25 °C. Zr4+ (aq) /Zr(s) : E° = 1,44 V ; O2 (g) /H2 O() : E° = 1,23 V ; H+(aq) /H2 (g) : E° = 0,00 V. Annexe 4. Constantes d'équilibre à 25°C. 4+ + 4 HO Zr(aq) (aq) ZrO2 (s) + HO(aq) ZrO2 (s) + 2 H2O() logK1 = 55 HZrO3(aq) logK2 = 5 Annexe 5. Données thermodynamiques (considérées indépendantes de la température). Espèce ZrC(s) O2 (g) CO2 (g) ZrO2 (s) + C" (kJ·mol1) 200 0 400 1100 " D, (J·mol1·K1) 30 200 210 50 Annexe 6. Classification périodique. Page 4/4
