Mines Chimie PSI 2007
| Thème de l'épreuve | Préparation du cuivre. Jasmin synthétique. |
| Principaux outils utilisés | thermochimie, solutions aqueuses, atomistique, chimie organique |
| Mots clefs | cuivre, jasmin |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - -
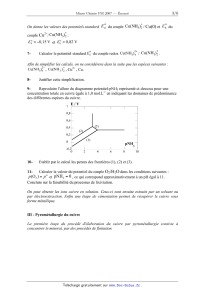
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - -
Énoncé complet
(télécharger le PDF)



Rapport du jury
(télécharger le PDF)

Énoncé obtenu par reconnaissance optique des caractères
A 2007Chimie PSI ECOLE NATIONALE DES PONTS ET CHAUSSEES. ECOLES NATIONALES SUPERIEURES DE L'AERONAUTIQUE ET DE L'ESPACE, DES TECHNIQUES AVANCEES, DES TELECOMMUNICATIONS, DES MINES DE PARIS, DES MINES DE SAINT--ETIENNE, DES MINES DE NANCY, DES TELECOMMUNICATIONS DE BRETAGNE. ECOLE POLYTECHNIQUE ( Filière TSI ). CONCOURS D'ADMISSION 2007 EPREUVE DE CHIMIE Filière : PSI Durée de l'épreuve : 1 heure 30 minutes L'usage d'ordinateur ou de calculatrice est interdit Sujet mis à la disposition des concours : Cycle International, ENSTIM, TPE-EIVP. Les candidats sont priés de mentionner de façon apparente sur la première page de la copie : CHIMIE 2007-Filière PSI Cet énoncé comporte 6 pages de texte. Si au cours de l'épreuve, un candidat repère ce qui lui semble être une erreur d'énoncé, il le signale sur sa copie et poursuit sa composition en expliquant les raisons des initiatives qu'il est amené à prendre. DEBUT DE L'ENONCE CHIMIE GENERALE : LE CUIVRE Les données numériques nécessaires à la résolution du problème sont regroupées à la fin de l'énoncé. I - L'atome de cuivre et ses ions Le cuivre est l'élément de numéro atomique Z=29. 1- Donner la configuration électronique attendue, d'après les règles de Klechkowski et de Hund et le principe d'exclusion de Pauli, de l'atome de cuivre dans son état fondamental. 2- En fait, cet atome constitue une exception à la règle de Klechkowski : le niveau 45 n'est peuplé que d'un électron. Proposer une explication. , . . , . . 2 , 3- Prev01r la configuraùon electronique des ions Cu+ et Cu + dans leur etat fondamental. Les énergies de première et de seconde ionisation du cuivre sont respectivement 7,7 eV/at et Page 1/6 Tournez la page S.V.P. Chimie 2007 -- Filière PSI 20,2 eV/at. Commenter l'écart entre ces valeurs. Le cuivre est-il un élément de transition ? Justifier la réponse. Il - Hydrométallurgie du cuivre La première étape de l 'élaboration du cuivre par hydrométallurgie est une lixiviation acide ou basique, qui permet de solubiliser le cuivre. Dans le cas d'une lixiviation ammoniacale, les processus chimiques peuvent être modélise's par les équations suivantes : 1 Cu + 4NH3 + 5 02 + HZO = Cu(NH3)ï + 2H0" ... Cu2O + 8NH3 + %oz + 2H20 = 2Cuan3)ï + 4Ho-- @) . . . . , . pi , + : , Par souc1 de 51mphoete, les 10ns X représentent les especes XÎq solvatees par l'eau 4- Quels sont les rôles respectifs joués par l'ammoniac et par le dioxygène '? Nous allons établir le diagramme E / V = f (pNH3) ,aVec pNH3 = --log([NHJ/c°) qui permet de definir les conditions de lixiviation ( c° représente la concentration standard, égale à 1,000 mol.L'l). 5- Les ions Cu+ sont-ils stables en solution aqueuse à pH=O, en l'absence d'ammoniac ? Justifier qualitativement la réponse. Déterminer la valeur du potentiel standard Eä du couple Cu2+/Cu. Les ions Cu2+ forment avec NH3 plusieurs complexes dont la formule peut s'écrire 2 , . CU(NH3)p+ , p etant un entier tel que 0 s p s 4 Les ions Cu+_forment avec NH 3 le complexe CU(NH3)Ê . 6- A l'aide des données fournies à la fin de l'énoncé, calculer les valeurs des constantes de formation successives K pour les équations : p--Lp cu(NH3 )Îa+--l + NH3 : CU(NH3 )î+ 15 p s 4 En déduire le diagramme de prédominance des espèces en fonction de pNH3. Page 2/6 Chimie 2007 -- Filière PSI On donne les valeurs des potentiels standard E :: du couple CU(NH3)Ë/ Cu(0) et EË du couple Cu2+/ Cu(NH3); : Ej; = --0,15 v et E; = 0,82 v 7- Calculer le potentiel standard E ;' du couple redox Cu(NH3)Ê+/ Cu(NH3); . Afin de simplifier les calculs, on ne considérera dans la suite que les espèces suivantes : 2 Cu(NH3)4+, Cu(NH3 ); , Cu2+ , Cu, 8- Justifier cette simplification. 9- Reproduire l'allure du diagramme potentiel--pNH3 représenté ci--dessous pour une concentration totale en cuivre égale à 1,0 mol.L'1 en indiquant les domaines de prédominance des différentes espèces du cuivre. 1E/V 0,8 0,6 10- Établir par le calcul les pentes des frontières (l), (2) et (3). 11- Calculer la valeur du potentiel du couple 02/H20 dans les conditions suivantes : P(02) = 190 et PNH3 = 0 , ce qui correspond approximativement à un pH égal à 11. Conclure sur la faisabilité du processus de lixiviation. On peut obtenir les ions cuivre en solution. Ceux-ci sont ensuite extraits par un solvant ou par électroextraction. Enfin une étape de cémentation permet de récupérer le cuivre sous forme métallique. III - Pyrométallurgie du cuivre La première étape du procédé d'élaboration du cuivre par pyrométallurgie consiste à concentrer le minerai, par des procédés defiottation. Page 3/6 Tournez la page S.V.P. Chimie 2007 -- Filière PSI La seconde étape consiste a] faire fondre dans un _ four tous les composants à une température sufisante pour obtenir deux phases liquides : c 'est la «fusion pour matte ». On obtient alors une phase - la matte - mélange de sulfures fondus de cuivre et d'éléments chalcophiles (Ni, Co, Pb... ). Lefer et les éléments de la gangue sont rejetés dans les scories. Au cours des opérations intervient la transformation modélisée par l'équation de réaction suivante, entre espèces solides non miscibles : CU20(S) + FEURS(S) = CU28(S) + FGO(S) 12- Déterminer un ordre de grandeur (à 10% près) de la température minimale à partir de laquelle un système constitué des 4 solides évolue dans le sens direct. Dans ces conditions, quel est l'état final ? On se placera dans l'approximation d'Ellingham. La dernière étape permet l'obtention du cuivre métallique. Cette opération s 'appelle la « conversion de la matte ». Elle se réalise en y insufiant du dioxygène. 13- Écrire l'équation de la réaction entre Cuzs et le dioxygène gazeux, conduisant à l'obtention du cuivre métallique. Proposer une application industrielle du co-produit gazeux obtenu. La matte peut encore contenir un peu d 'oxyde Cu 20, qui réagit avec C M 2S pour former du cuivre selon l'équation : 2 CuZO(S) + Cu2S(S) = so + 6 Cu (5) 2(a) 14- Définir et calculer la variance d'un système contenant Cu20, CU2S, 802 et Cu à l'équilibre chimique. Commenter la valeur obtenue. On précise que les 3 solides sont non miscibles. On obtient ainsi le cuivre métallique sous forme de blister. Ce dernier est coulé dans un _ four pour obtenir des plaques ou des lingots devant être ensuite rafinés. Analyse de la pureté du métal obtenu L 'acide nitrique concentré réagit violemment avec le cuivre et provoque un dégagement de monoxyde d 'azote gazeux NO. 15- Écrire l'équation de la réaction d'oxydoréduction mise en jeu. 16- On fait réagir une masse m=0,l8g de cuivre non raffiné avec un excès d'acide nitrique. On récupère un volume V=0,040 dm3 de gaz, à T=300 K sous une pression de 1 bar. En admettant que le gaz est produit uniquement par la réaction avec le cuivre et que ce dernier est entièrement consommé, calculer la valeur de la fraction massique du cuivre dans le solide impur. On supposera que le gaz obtenu a un comportement de gaz parfait. Page 4/6 Chimie 2007 -- Filière PSI CHIMIE ORGANIQUE : LE JASMIN SYNTHETIQUE Le jasmin est présent dans de nombreux parfums. Dans la plupart des cas, plutôt que le composé naturel, c 'est le composé synthétique que l 'on utilise. Nous allons nous intéresser à sa préparation à partir d'acide cinnamique, en deux étapes successives représentées sur la _ figure ci--après. C% /C % c Na2003 C C \OH --> (: OH --> %c/ ||4 CC|4 H' Î3r acétone | (solvant) (solvant) acide cinnamique produit1 ... , produit2fiÿ I - Première étape : addition du dibrome 17-- Donner le descripteur stéréochimique (la configuration absolue) des atomes de carbone asymétriques de l'isomère du produit 1 représenté ci--dessus. La réponse devra être justifiée. 18- Proposer en le justifiant un mécanisme pour la réaction d'addition, sachant que le composé l est en fait obtenu sous forme racémique (seul un énantiomère est représenté). Il - Seconde étape : élimination Au cours de la transformation donnant le produit à, on observe un dégagement gazeux. 19- De quel(s) gaz s'agit--il ? Ajuster l'équation de réaction correspondante. Seul ce stéréoisomère du l-bromo-2-phényléthène (encore appelé fi-bromostyrène) est odorant. 20- Représenter le stéréoisomère non odorant et donner son descripteur stéréochimique (configuration absolue). 21- Pourquoi était-il inutile de séparer les deux énantioméres du produit 1 pour obtenir le jasmin artificiel ? Page 5/6 Tournez la page S.V.P. Chimie 2007 -- Filière PSI DONNÉES NUMERIQUES On pogera; a = %ln10 = 0,060 V Potentiels standard à pH=O : Couple Cu2+/Cu+ Cu+/Cu 02 /H20 E°/V 0,16 0,52 1,23 Constantes de dissociation globales des complexes cuivre(ll) / ammoniac Cu(NH3)Ë+ : Constante de dissociation globale du complexe cuivre(l) / ammoniac Cu(NH3 ); : pK'i2 = 10,8 Enthalpies et entropies standard de formation, à T=298 K : CuzO(s) Cu;S(s) Fe0(s) FeS(s) ... ___-" Masses molaires : Élément Cu ' C ' Au 0 H M/g--mol'1 64 ' 12 ' 197 16 1 La pression standard vaut p° = 1,000 bar =1,000><105 Pa Pour simplifier les calculs, on prendra la constante des gaz parfaits R = 8,0 J ' K_1 11101--1 FIN DE L'ENONCE Page 6/6
