e3a Physique et Chimie PC 2021
| Thème de l'épreuve | Étude de mammifères marins. Quelques utilisations des alcalino-terreux en chimie. |
| Principaux outils utilisés | diffusion thermique, ondes acoustiques, magnétisme, cristallographie, cinétique chimique, solutions aqueuses, thermodynamique, chimie organique |
| Mots clefs | isolation, écholocalisation, homéothermie, dauphin, baleine, phoque, champ magnétique terrestre, effet doppler, radium, magnésium, alcalino-terreux, Nigari, radioactivité, seychellène |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - -
Énoncé complet
(télécharger le PDF)














Rapport du jury
(télécharger le PDF)


Énoncé obtenu par reconnaissance optique des caractères
SESSION 2021 EUR y PC9IPC
NES
e3a
POLYTECH
ÉPREUVE SPÉCIFIQUE - FILIÈRE PC
PHYSIQUE ET CHIMIE
Durée : 4 heures
N.B. : le candidat attachera la plus grande importance à la clarté, à la
précision et à la concision de la rédaction.
Si un candidat est amené à repérer ce qui peut lui sembler être une erreur
d'énoncé, il le signalera sur sa copie
et devra poursuivre sa composition en expliquant les raisons des initiatives
qu'il a êté amené à prendre.
RAPPEL DES CONSIGNES
e _ Utiliser uniquement un stylo noir ou bleu foncé non effaçable pour la
rédaction de votre composition ; d'autres
couleurs, excepté le vert, peuvent être utilisées, mais exclusivement pour les
schémas et la mise en évidence
des résultats.
e Ne pas utiliser de correcteur.
«_ Écrire le mot FIN à la fin de votre composition.
Les calculatrices sont autorisées.
Le sujet est composé de deux problèmes indépendants, un de physique un de
chimie.
e Tout résultat donné dans l'énoncé peut être admis et utilisé par la suite,
même s'il n'a pas été
démontré par le ou la candidat(e).
e Les explications des phénomènes étudiés interviennent dans l'évaluation au
même titre que les
développements analytiques et les applications numériques.
e Les résultats numériques exprimés sans unité ou avec une unité fausse ne sont
pas comptabili-
Sés.
1/20
PHYSIQUE
« C'est assez ! » dit la baleine, je me cache à l'eau car Jj'ai le dos fin.
Le sujet de Physique est composé de trois parties totalement indépendantes.
Les figures numérotées sont utiles au candidat pour traiter le sujet. Par
commodité de
représentation les échelles ne sont pas respectées. Les simples illustrations,
non numérotées,
proviennent du site www.bing.com/images/phoques et dauphins.
Le sujet, prévu pour durer deux heures, s'intéresse à des aspects de la vie de
certains
mammifères marins comme les phoques ou les cétacés (dont font partie les
baleines, les
cachalots et les dauphins). Ces espèces aux capacités remarquables, sont
réputées
être intelligentes et certains individus semblent vouloir avoir une interaction
avec l'homme. De
la baleine tueuse au dauphin sauveur, les cétacés n'ont cessé d'alimenter notre
imaginaire.
Les cétacés sont les seuls mammifères à vivre exclusivement dans la mer. Devoir
respirer avec
des poumons et maintenir leur température interne constante a nécessité une
adaptation qui en
fait des animaux exceptionnels. L'étude scientifique de ces espèces, dont
certaines sont en voie
de disparition, est menée par de nombreuses équipes de recherche en
collaboration avec les
associations de défense des espèces animales.
La partie I, faisant appel à la thermodynamique, s'intéresse à l'homéothermie
des mammifères
marins en prenant l'exemple d'un phoque.
La partie II, faisant appel à l'étude physique des ondes acoustiques,
s'intéresse à
l'écholocalisation des dauphins.
La partie IIT s'intéresse au champ magnétique terrestre car, selon certaines
hypothèses, ce
serait celui-c1 qui permettrait aux baleines de suivre leur chemin de migration.
Partie I - Homéothermie des phoques
La loi phénoménologique de Fourier, relative à la diffusion thermique, traduit
la
proportionnalité entre la densité de flux thermique 7, et le gradient de
température :
Ja = --À grad(T).
Q1. Quels sont le nom et la dimension du coefficient À ? En déduire son unité
SI. Justifier
physiquement le sens du vecteur densité de flux thermique J;.
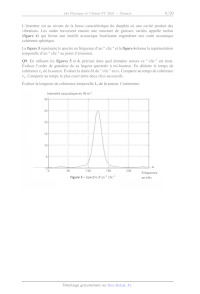
On se place en coordonnées cylindriques (figure 1) pour étudier une situation
physique
stationnaire, unidimensionnelle à symétrie cylindrique, telle que la
température en un point M
(r, 0,z) ne dépend que de r.
, LOT dT\ --
Le gradient de la température T(r) est égal à grad (T) = (S) Er.
2/20
À Matériau
À y + 5
r' caractérisé
| e, par À
2" à Cr
' |
| un
LUN >
ë.| u
+ ÿ | T Axe Oz
os |
(D) la " y È E ,
Er -- et" : { * Ca
Ü ms. 1 /
L
HU à Er
Figure 1- Coordonnées cylindriques Figure 2 -- Conducteur thermique
On considère un cylindre conducteur thermique creux de longueur L, occupant
l'espace
T le,
ms + ... _... - . dede mette es tes ohms tel. Lire dr... f - . ef nn PT
f s. # --
| : : | / 1 ' ST
F .
. : | } à À
; . | 1 | _ .
. s #
. { 1
| . à | /
n l'E | L
| = . |
| * |
. 4
- .
= S ee L.e Le ele © © » ele cle: © © ne ps e es © © n.e © © es © en: © © es ©
ee. © © es © » ge ee e ee. ©
.
.
.
.
.
.
= .
.
D». 4 eh. +... . .....
.
-- ri . .
0,2 w :
, . '
.
.
n
.
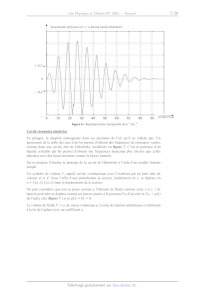
Figure 6 -- Représentation temporelle d'un " clic "
Cavité résonante émettrice
En plongée, le dauphin emmagasine dans ses poumons de l'air qu'il ne relâche
pas. Un
ajustement de la taille des sacs d'air lui permet d'obtenir des fréquences de
résonance variées
comme dans une cavité, dite de Helmholtz, modélisée en figure 7. C'est la
présence d'un
hquide cristallin qui lui permet d'obtenir des fréquences beaucoup plus élevées
que celles
obtenues avec des tissus normaux comme le larynx humain.
On se propose d'étudier le principe de la cavité de Helmholtz à l'aide d'un
modèle linéaire
simple.
Un cylindre de volume V, appelé cavité, communique avec l'extérieur par un
petit tube de
volume si V. Sous l'effet d'une perturbation la section, initialement en x, se
déplace en
x + Ex, t), ECx, t) étant le déplacement de la section.
On peut considérer que tout se passe comme s1 l'élément de fluide contenu entre
x et x + ôx
dans le petit tube se déplace comme un piston soumis à la pression Pexr d'un
côté et Peur + p(£)
de l'autre côté (figure 7 ) avec p(£ = 0) = 0.
Le volume de fluide + sx, de masse volumique p, évolue de manière adiabatique
en obéissant
à la loi de Laplace avec un coefficient y.
7/20
Pression
extérieure
Pext U
X+OX x
\ | | Volume V=SL grand
|!
< - (SL >>sx)
d À
s ( > U _ ]
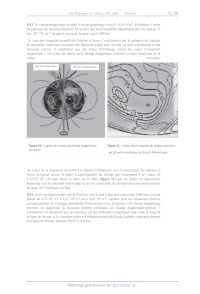
<-- [ me Pression intérieure ] Pint = Pext + D Figure 7 -- Cavité de Helmholtz Q10. Justifier qu'on peut écrire au premier ordre p(£) = 7 À Port en considérant p(E) infiniment petit du premier ordre au même titre que T et S. En appliquant la deuxième loi de Newton à l'élément de fluide, établir l'équation différentielle à laquelle obéit £(t). Quelle est la fréquence caractéristique du mouvement ? On l'exprimera en fonction de PV, s, D, y; Poxt EURt OX. Propagation aller-retour Le faisceau s'atténue au fur et à mesure de sa propagation dans l'eau : le phénomène d'écholocalisation ne peut pas repérer des obstacles à plus de 100 m. On admet que l'intensité acoustique obéit à une loi exponentielle d'atténuation dans l'eau de la forme : I(r) = I(r = 0) exp(-ar). La réflexion du faisceau par l'obstacle entraîne une modification de l'intensité acoustique au niveau de l'obstacle. Cette modification, liée aux impédances acoustiques Z,,, de l'eau et Zopst du matériau de l'obstacle, est donnée par : lréfléchi ... ... (Zeau --Zobst ) Tincident (Zeau +Zobst )2 Le mouvement relatif dauphin-obstacle (figure 8) crée un effet Doppler qui modifie la fréquence du faisceau réfléch1 par rapport à celle f du faisceau incident. On peut établir la ôf 2fcos 0 modification de la fréquence. formule U -- c avec Ü la norme de la vitesse relative dauphin-obstacle et Ôf la 8/20 Sons émis (clics). Q11. Évaluer le coefficient d'atténuation à sachant que l'intensité est divisée par 2 en 50 m. Quelle est l'unité de l'impédance acoustique ? Calculer le rapport R sachant que l'impédance de l'eau vaut 7,4, = 1 480 STet celle d'un poisson (obstacle) vaut Zopstacte = 1 540 SE. Évaluer l'ordre de grandeur du rapport Q des intensités de l'onde reçue par le dauphin et de l'onde émise par celui-c1 pour un banc de poissons à 75 m du dauphin. En assimilant le "clic" à une onde harmonique de fréquence f = 125 KH7z, quelle est la vitesse relative U du banc de poissons détecté par le dauphin, qui se déplace sur la même droite que le banc de poisson, sachant que la modification de fréquence vaut Ôf = 1 kHz ? Dauphin Emetteur et Récepteur Onde sonore émise de Onde sonore reçue de fréquence f fréquence f + ôf obstacle Le Le --_--_ Figure 8 -- Effet Doppler Ü Partie III - Migration des baleines Une hypothèse appuyée sur de nombreux indices, mais encore à préciser, est que les cétacés disposent d'un sens magnétique qu'ils utiliseraient pour migrer sur de longues distances. Les relevés par satellite des baleines à bosse au large de l'archipel d'Hawaï montrent que les trajectoires de ces dernières suivent le nord magnétique avec une grande précision. 9/20 Certains biologistes pensent que les échouages, régulièrement observés (depuis l'Antiquité au moins), sont dus à ce sens magnétique. Dans un certain nombre de cas, une corrélation a effectivement été trouvée entre anomalies magnétiques au sol et zones d'échouages fréquents. Rappel : un moment magnétique M = M e, (figure 9) placé en un point O choisi comme origine d'un repère de coordonnées sphériques crée, en un point P (p, 8,@) éloigné, un champ magnétique égal à : B = Pr (2cos8e, + sinôeo). Placé dans un champ extérieur Bou (O0), un dipôle magnétique est soumis à des actions de moment [ (0) = MA Bert (O0) et de résultante F -- (M. grad Bent. L'énergie potentielle d'interaction vaut E,, = M : Bus (O). Le déplacement élémentaire en coordonnées sphériques est : -- l=dpe, + pd eÿ + psinôdpe,, Figure 9 --- Moment dipolaire Q12. On considère que le champ magnétique terrestre est celui d'un dipôle magnétique de moment magnétique M (figure 10) placé au centre de la Terre. L'angle entre sa direction et l'axe de rotation de la Terre vaut environ 11°. Établir l'équation des lignes de champ et tracer leur allure. Donner le sens et la direction du dipôle magnétique terrestre. Expliquer pourquoi la boussole, qui est elle-même un dipôle magnétique, indique grosso-modo le Nord géographique. 10/20 z A D = y P _, Ba M P ° O Q13. Le champ magnétique au pôle Nord géographique vaut B = 6,0'10*nT. En déduire l'ordre de grandeur du moment dipolaire M sachant que la splitéabilité magnétique de l'air vaut uo = 47 : 1077H-:m et que le rayon de la terre vaut 6 400 km. Le caractère magnéto-réceptif des baleines à bosse s'expliquerait par la présence de cristaux de magnétite (matériau constitutif des boussoles) dans leur cerveau, ce qui les doteraient d'une boussole interne. Il semblerait que les zones d'échouage soient les zones d'anomalie magnétique c'est-à-dire les zones où le champ magnétique terrestre s'écarte beaucoup de la valeur moyenne. Pôle Nord magnétique Pôle Nord géographique Figure 10 -- Lignes de champ du champ magnétique Figure 11 -- Carte équi-intensité du champ terrestre terrestre . | en UT entre Amérique du Sud et Antarctique Au cours de la migration de 6 000 km depuis la Polynésie vers l' Antarctique, les baleines à bosse devraient suivre la ligne d'équi-intensité du champ qui correspond à la valeur de 3,33-10* nT. On peut observer alors sur la carte (figure 11) que les lignes se rapprochent beaucoup vers le continent Antarctique et qu'il y a une zone de champ beaucoup moins intense au large de l' Amérique du Sud. Q14. Avec un déplacement vers le Nord ou vers le Sud à peu près équivalent (800 km) on peut passer de 3,33-10* nT à 2,67 -10* nT ou à 4,67:10* nT : quelles sont les variations relatives correspondantes de l'énergie potentielle d'interaction entre la baleine et le champ magnétique terrestre en supposant la boussole interne colinéaire au champ magnétique terrestre ? Commenter en admettant que les baleines ont des difficultés à maintenir leur route le long de la ligne de champ, si la variation relative d'énergie potentielle locale, linéaire, orthogonalement à la ligne de champ, dépasse 0,025 % par km. 11/20 CHIMIE Quelques utilisations des alcalino-terreux en chimie Les alcalino-terreux, éléments chimiques situés dans la deuxième colonne du tableau périodique, constituent une famille importante en chimie, avec notamment parmi les plus connus les éléments magnésium, calcium et radium. Partie I - Étude en chimie générale L.1 - Structure ionique Q15. Étant donnée la position des éléments de cette famille dans le tableau périodique, en déduire la configuration électronique de valence des atomes associés, dans leur état fondamental. En déduire, en justifiant, la formule des 1ons monoatomiques susceptibles de se former. Soit la structure cristalline du solide ionique CaF2 (appelée fluorine) : les ions calcium Ca°* occupent les sommets d'une maille cubique ainsi que le centre de chaque face (maille cubique à faces centrées) et les 1ons fluorure F7 occupent tous les sites tétraédriques du cube. Q16. Représenter une vue légendée, en perspective, de la maille élémentaire de paramètre a et une projection plane sur laquelle les cotes des ions seront indiquées et exprimées sous forme de fractions du paramètre de maille a. Q17. Déterminer le nombre d'ions Ca'* et F- contenus dans cette maille cubique. Q18. À l'aide des rayons ioniques, déterminer la valeur du paramètre de maille a. Q19. Déterminer la valeur de la compacité. 1.2 - Dosage d'une solution de " Nigari " Le "Nigari" utilisé dans la cuisine japonaise pour la fabrication du tofu, est du chlorure de magnésium MgCb. Ce composé ionique est également utilisé comme complément alimentaire. Il peut être commercialisé sous forme d'une solution aqueuse flaconnée de volume V = 125 mL, contenant une masse m de MgeCl2 que l'on souhaite déterminer par une méthode de dosage conductimétrique. Protocole expérimental du dosage par étalonnage : - on prépare 100,0 mL d'une solution So de titre massique to = 8,00 g:L' 7 en chlorure de magnésium. Par dilution, on prépare ensuite une gamme de 4 solutions filles de S1 à S4 de titres massiques {1 = {0/10 , t2 = t0/20, t3 = to/ 50 et t4 = to/ 100 en chlorure de magnésium ; - on mesure la conductance G de chaque solution de la gamme ; on obtient : Titre massique ti t2 {3 t4 Conductance G (en mS) 2,18 1,11 0,44 0,22 - on dilue quatre cents fois la solution commerciale et on mesure, avec le même dispositif expérimental, la conductance de la solution S" ainsi obtenue. On trouve G° = 0,85 mS. 12/20 Q20. Lister, en justifiant, la verrerie nécessaire à la préparation de 50,0 mL de solution fille de titre massique t1. Q21. Exploiter le dosage par étalonnage pour déterminer la masse de chlorure de magnésium contenu dans le flacon de la solution commerciale. L'étiquette indique m = 15,6 g. Conclure. L.3 - Un élixir radioactif En 1925, un "élixir radioactif" était commercialisé sous le nom de " radithor " représentant emblématique d'une vogue de "radiothérapie douce ", très prisée par certains milliardaires américains. Sa vente prit fin en 1930 avec les morts prématurées de plusieurs jeunes personnes. Cet élixir contenait deux isotopes du radium, dont le radium 226 d'une masse initiale mo = 1,0 pig. Q22. Les noyaux de radium 226 et de radium 228 sont des isotopes. Donner la composition des noyaux et justifier le terme isotopes. La radioactivité de l'élixir était principalement due à la désintégration spontanée du radium 226 selon l'équation : ° 26Ra -- 22Rn+ YHe Soient No le nombre de noyaux à t = 0 et À la constante radioactive de valeur À = 4,28-107* an ! (constante analogue à une constante de vitesse). Q23. Étant donnée la masse initiale, calculer le nombre de noyaux No de radium 226 présents dans le flacon. Q24. Sachant que la désintégration radioactive suit une loi cinétique d'ordre 1, établir l'expression du nombre de noyaux N(t), en fonction du temps et des grandeurs No et À. Q25. Déterminer la valeur du temps de demi-réaction encore appelé "temps de demi-vie " ou "période radioactive ". L.4 - Un flash lumineux La combustion d'un ruban de magnésium a permis aux premiers photographes de réaliser des " flash lumineux " leur permettant d'éclairer, avec une lumière très intense, la scène à immortaliser. On souhaite déterminer indirectement la valeur de l'enthalpie standard AH, de la réaction de l'oxydation du magnésium par le dioxygène selon l'équation : Mg(s) + 2 O2(g) = MgO(s) Le suivi de l'évolution de la température de la réaction étudiée n'étant pas aisé, on utilise l'additivité des enthalpies standard de réaction, en déterminant expérimentalement celles des réactions d'équations suivantes : Mg(s) + 2 H*(aq) = Mg"*(aq) + H2(£) AH, = -- 467 kJ-mol! MgO(s) + 2 H'(aq) = Mg' (aq) + HO(1) AH; = -- 151 kJ-mol! H(£) + % O)(g) = HO(1) AH, = -- 286 kJ-mol! 13/20 Q26. Proposer le nom d'une méthode expérimentale permettant de déterminer la valeur d'une enthalpie de réaction. Q27. À partir des résultats obtenus, déterminer la valeur de l'enthalpie standard AH}; de la réaction d'oxydation du magnésium. 14/20 Partie II - Étude en chimie organique IL.1 - Réaction d'un organométallique sur un époxyde La réaction de composés organométalliques sur un époxyde est une méthode importante pour créer des liaisons C--C. De plus, la nature du métal oriente la régiosélectivité de la réaction sur un époxyde asymétrique. En effet, les organolithiens (RL1) et les organomagnésiens (RMgX) réagissent différemment vis-à-vis d'un époxyde. On note que X -- CI ou Br et R une chaîne alkyle ou phényle. Présentation des résultats expérimentaux OH O protocole a A | | OH protocole b nn. ET Protocole a : addition de l'époxyde goutte à goutte sur l'organolithien (phényllithium) dans l'éther diéthylique (CH3-CH2)20 suivie d'un traitement par hydrolyse acide. Li phényllithium Q28. Proposer un mécanisme permettant de justifier la formation de la molécule A en utilisant le protocole a. Protocole b : addition de l'organomagnésien (bromure de phénylmagnésium) goutte à goutte sur l'époxyde dans l'éther diéthylique suivie d'un traitement par hydrolyse acide. Dans ces conditions, il se forme du bromure de magnésium (MgBr2) qui transforme l'époxyde en un isomère présentant une fonction aldéhyde dont la formule topologique est la suivante : MgBr DA bromure de phénylmagnésium 15/20 On place 1,34 g de bromobenzène (M = 157 g-mol!) et 200 mg de magnésium (M = 24,3 g-mof) dans 5 mL d'éther diéthylique dans un ballon. À la fin de la synthèse magnésienne et à l'aide d'une ampoule de coulée isobare, on additionne 500 mg de l'époxyde (M = 120 g-mof1) dissous dans 5 mL d'éther diéthylique anhydre. Après l'addition, le mélange est chauffé au reflux pendant 10 min, refroidi à température ambiante, puis traité avec 10 mL d'acide sulfurique à 10 %. La phase organique est séchée par du sulfate de magnésium anhydre et le solvant est éliminé à l'évaporateur rotatif. On obtient une masse m = 646 mg du produit A (M = 198 g-mof). Q29. Faire un schéma annoté du montage de la synthèse. Q30. Justifier le choix du solvant de la synthèse. Quel est le rôle de l'acide sulfurique ? Q31. Déterminer le rendement de la réaction. IL.2 - Synthèse de la (+) seychellène La (-)-seychellène est un composé minoritaire dans l'huile essentielle de Patchouli. La synthèse décrite ci-après permet l'obtention d'un mélange racémique de la seychellène. O OTHP 1) NaBH,, éthanol nn. La 2) Cj O OTHP CI : CH;MgBr, CuCI X, 2 3 >
(CH-CH,)0, - 25 °C
OTHP OTHP
O =
À chauffage
4 ------ ----------
0 O
5 6 O
=
Ph;P=CH,; H,; (g)
6 > T Re ô
Rh(PPh;);CI
16/20
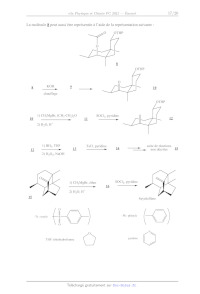
La molécule 8 peut aussi être représentée à l'aide de la représentation
suivante :
LL OTHP
8
OTHP
O
8 D, 2 -- 10
chauffage
OTHP
1) CH;,MgBr, (CH-CH)0 SOC, pyridine
2) H,0, H°
1) BH;, THF TsCI, pyridine suite de réactions
12 > 15 »- 14 --_--# non décrites
2) H,0;, NaOH
1) CH;MgBr, éther SOCT;, pyridine
> 16 >
2) H,0, H°
£ Seychellène
O
-Ts : tosyle - Ph : phényle
O
N
K
THF: tétrahydrofurane pyridine
A
17/20
Q32.
Q33.
Q34.
Q35.
Q36.
Q37.
Q38.
Q39.
Q40.
Q41.
Q42.
Q43.
Q44.
Donner le descripteur stéréochimique du carbone asymétrique de la molécule 1 en
justifiant la
réponse à l'aide des règles de Cahn, Ingold et Prelog.
À l'aide du document 1 entre autres, calculer la variation du nombre
d'oxydation du carbone
fonctionnel modifié entre les molécules 1 et 2. En déduire le rôle du
tétrahydruroborate de
sodium (NaBH) lors de cette réaction en justifiant la réponse.
Dans ces conditions, l'organocuivreux CH3Cu se forme et réagit sur la molécule
2 par une
addition (1,4). Sachant que la molécule 3 est un énolate, proposer un mécanisme
expliquant la
synthèse des molécules 3 et 4. Quelle est la fonction créée lors de la synthèse
de la
molécule 4 ?
Quelle est la fonction créée dans la molécule 5 ? Proposer un réactif
permettant la synthèse de
la molécule 5 à partir de 4.
Donner la représentation de la molécule 7 et le nom de la réaction 6 -- 7.
À l'aide du document 2, justifier la représentation de la molécule 8
Calculer le nombre d'oxydation du ruthénium dans chaque complexe (numérotés de
1 à 4)
présent dans le cycle catalytique du document 2 et préciser la nature de
chacune des étapes du
cycle :1--2;:2--3;:3--4;41.
Proposer un mécanisme de la réaction 8 -- 9.
Proposer un réactif permettant de réaliser la réaction 9 -- 10.
Donner la représentation de la molécule 11.
Donner les représentations des molécules 13 et 14.
Donner la représentation de la molécule 16.
On obtient un mélange racémique de la seychellène. Après avoir rappelé la
définition d'un
mélange racémique, décrire une technique expérimentale permettant d'effectuer le
dédoublement d'un racémique.
18/20
(S) : solvant
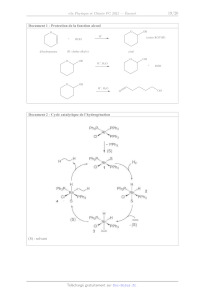
Document 1 - Protection de la fonction alcool
O O OR
À pou HR (notée ROTHP)
dihydropyrane (R: chaîne alkyle) cétal
o OR | O OH
H*, H,0
TR + ROH
O OH
H", H0 PNR
Document 2 - Cycle catalytique de l'hydrogénation
Ph3P,, .. s«PPh3
Rh
CI PPh;
- PPh3
(S)
H Ph;3P:, NS
HT RMS H2
CI 4 PPh3
| |
Ph3P... | LH Ph3P.. | «H
CS or
CIT | "PPh; ci | "PPh;
4 - S S
H
(S) PhaPe.. |. _
a" PPh;: - (S)
3 --
19/20
Données
- Constante d'Avogadro Na = 6,02-107* mol !
- Numéros atomiques :
Symbole H Be C O M£g Ca ST Rh Ba
Ra
Z I ' 6 8 12 20 38 45 56
88
- Masse molaire du radium 226 : M = 226 g mol |
- Rayons ioniques : r(Ca**) = 1,00:107!° met r(F) = 1,36:107!°m
- _ Électronégativités des atomes dans l'échelle de Pauling :
x (H)=2,2;% (0) 2,55 ; x (O) = 3,44
FIN
20/20
IMPRIMERIE NATIONALE - 211166 - D'après documents fournis
