X/ENS Chimie PC 2025
| Thème de l'épreuve | Nouvelles stratégies de synthèse totale d'alcaloïdes naturels. Autour du norbornadiène. |
| Principaux outils utilisés | oxydoréduction, thermodynamique, cinétique chimique, courbes courant-potentiel, orbitales moléculaires, chimie organique, Python |
| Mots clefs | alcaloïde, réaction de Pictet-Spengler, mavacuran, norbornadiène, quadricyclane, éthène, cycloaddition, Eyring, calorimètre, calorimétrie, réacteur ouvert, RPAC |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)













Rapport du jury
(télécharger le PDF)

Énoncé obtenu par reconnaissance optique des caractères
ECOLE POLYTECHNIQUE - ESPCI
ECOLES NORMALES SUPERIEURES
CONCOURS D'ADMISSION 2025
MARDI 15 AVRIL 2025
14h00 - 18h00
FILIERE PC
-
CHIMIE A
Epreuve n° 4
(XEULS)
Durée : 4 heures
L'utilisation des calculatrices n'est pas
autorisée pour cette épreuve
Le sujet est composé de deux parties totalement indépendantes. La première
partie porte sur des
stratégies de synthèse totale d'alcaloïdes naturels. La deuxième s'intéresse à
la physico-chimie du
norbornadiène et de ses dérivés.
Des annexes sont disponibles à la fin de l'énoncé et comportent des données
spectroscopiques
infrarouge et RMN (annexe 1), une banque de conditions pour la mise en place de
groupes protecteurs
et leur déprotection (annexe 2), et des données physico-chimiques (annexe 3).
Même si ce n'est pas explicitement demandé dans chaque question, toutes les
réponses doivent être
justifiées.
Partie 1
Nouvelles stratégies de synthèse totale d'alcaloïdes naturels
Cette partie est consacrée à une nouvelle stratégie de synthèse totale d'une
famille d'alcaloïdes
complexes à l'activité biologique très prometteuse. Ce domaine de recherche est
une des voies pour
développer des nouveaux médicaments plus actifs ou avec moins d'effets
secondaires.
Nous nous intéresserons ici à la synthèse d'un sous-groupe de substances
naturelles appartenant aux
alcaloïdes indolomonoterpéniques. Ces molécules forment une classe étendue et
fascinante de produits
naturels étudiés en raison de leurs bioactivités prometteuses (cytotoxiques,
immunosuppressives, antiinflammatoires, antibactériennes...) et de leur
diversité structurale. On en dénombre plus de 3000
découverts dans plusieurs familles du règne végétal comme les Apocynaceae,
Loganiaceae et
Rubiaceae.
Il s'agit en particulier ici de la synthèse de 6 alcaloïdes dits mavacurans (à
l'origine isolés de plantes ou
fruits et utilisés en Amazonie pour préparer des flèches empoisonnées au
curare) en moins de 15 étapes,
une prouesse par rapport aux synthèses reportées jusqu'ici pour ces alcaloïdes
très complexes. Cette
synthèse totale, réalisée pour la première fois en 2023 et adaptable à d'autres
molécules de la famille
des alcaloïdes indolomonoterpéniques, est une étape importante dans la synthèse
efficace de futurs
médicaments.
Dans cette partie, un soin particulier est attendu dans l'écriture des
mécanismes réactionnels ; les
formules utilisées dans les réponses aux questions devront obligatoirement être
des représentations
topologiques et faire apparaître les doublets non liants et les formes
mésomères pertinentes des
intermédiaires réactionnels s'il y a lieu. Une représentation simplifiée des
molécules peut être utilisée
dans l'écriture des mécanismes réactionnels ou des équations de réaction mais,
si c'est le cas, elle doit
être clairement explicitée.
I Première stratégie de synthèse
L'équipe qui a mené cette recherche s'est lancée dans une première stratégie de
synthèse qui répondait
au schéma rétrosynthétique (Figure 1) concernant la dernière étape (fermeture
du 5e cycle noté « D »
pour mener aux deux alcaloïdes mavacuran notés 1 et 2) :
1 / 23
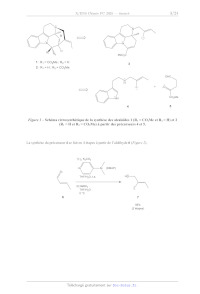
Figure 1 Schéma rétrosynthétique de la synthèse des alcaloïdes 1 (R1 = CO2Me
et R2 = H) et 2
(R1 = H et R2 = CO2Me) à partir des précurseurs 4 et 5.
La synthèse du précurseur 4 se fait en 4 étapes à partir de l'aldéhyde 6
(Figure 2).
2 / 23
Figure 2 Synthèse du composé 4 à partir de 6.
1. La DMAP (N,N-diméthylpyridin-4-amine) est un dérivé de la pyridine utilisé
comme catalyseur
nucléophile dans un grand nombre de réactions. Expliquer en quoi la
nucléophilie de l'azote du
cycle de la pyridine est augmentée ici par rapport à celui de la molécule de
pyridine seule.
2. Donner la structure de l'intermédiaire réactionnel obtenu après la première
étape de la
transformation 6 7, puis représenter le mécanisme réactionnel de la deuxième
étape de cette
transformation.
3. Donner la formule topologique de l'intermédiaire obtenu après la première
étape de la
transformation 7 4.
4. À l'aide de l'Annexe 1, montrer que les données de spectroscopie RMN du
composé 4 fournies
dans le Tableau 1 sont compatibles avec la structure proposée dans la Figure 2.
Attribuer les
signaux A à I aux protons portés par les atomes selon la numérotation de la
Figure 2.
Référence du signal
A
B
C
D
E
F
G
H
I
Déplacement chimique
(ppm)
1,81
2,07
2,93
3,06
3,56
5,81
7,04
7,17 7,69
8,60
Nature du signal et
couplage éventuel (Hz)
d (6,3)
br s
t (6,9)
br t (6,9)
s
q (6,3)
s
m
br s
Intégration
3
1
2
2
2
1
1
4
1
Tableau 1 Spectre RMN du proton du composé 4.
Abréviations : s = singulet, d = doublet, t = triplet, q = quadruplet, m =
multiplet, br = large.
La synthèse du précurseur 5 se fait, elle, en 2 étapes (Figure 3).
3 / 23
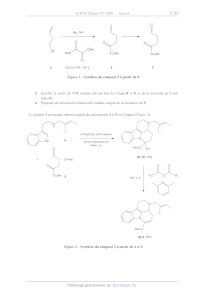
Figure 3 Synthèse du composé 5 à partir de 8.
5. Justifier le choix du THF comme solvant lors de l'étape 8 9, et de la
nécessité qu'il soit
anhydre.
6. Proposer un mécanisme réactionnel rendant compte de la formation de 9.
Le produit 3 est ensuite obtenu à partir des précurseurs 4 et 5 en 2 étapes
(Figure 4).
Figure 4 Synthèse du composé 3 à partir de 4 et 5.
4 / 23
7. Donner le schéma de Lewis de l'espèce (PhO)2PO2H, ainsi que la géométrie
locale de l'atome
de phosphore.
La réaction menant à (±)-10 est une réaction de Pictet-Spengler. Cette dernière
a été découverte en 1911
et reste très utilisée lors de la synthèse des alcaloïdes et des produits
pharmaceutiques. Lors de cette
réaction chimique, une -aryléthylamine comme la tryptamine (±)-10 est produite
par une réaction de
fermeture de cycle après une condensation avec un composé carbonylé.
8. Donner la signification du signe (±) dans le nom du produit (±)-3.
9. Identifier, en justifiant dans les deux cas, le site le plus nucléophile de
la molécule 4 et les sites
électrophiles de la molécule 5 en les classant par ordre croissant
d'électrophilie.
10. La 2,6-diméthylpyridine intervient lors de la transformation (±)-10 (±)-3.
Donner son rôle
lors de cette transformation.
11. Indiquer pourquoi l'on se place à 0 °C dans cette transformation. Donner le
nom de ce type de
réaction chimique.
12. L'hétérocycle hydroxylé de la molécule (±)-10 est un cycle à 6. On observe
expérimentalement
qu'il n'adopte pas une conformation de type « chaise », mais une géométrie
quasi-planaire.
Proposer une explication à cette observation.
II Deuxième stratégie de synthèse
Après les 8 étapes décrites dans la première partie, l'équipe de recherche
n'est pas parvenue à obtenir
d'alcaloïdes. Suite à cet échec, l'équipe a décidé d'établir un nouveau schéma
rétrosynthétique (Figure
5).
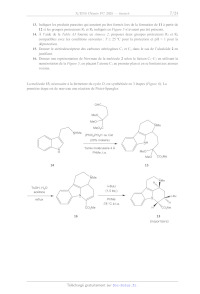
Figure 5 Schéma rétrosynthétique de la synthèse des alcaloïdes 1 (R1 = CO2Me
et R2 = H) et 2
(R1 = H et R2 = CO2Me) à partir du précurseur 12.
5 / 23
13. Indiquer les produits parasites qui auraient pu être formés lors de la
formation de 11 à partir de
12 si les groupes protecteurs R3 et R4 indiqués en Figure 5 n'avaient pas été
présents.
14. À l'aide de la Table A3 fournie en Annexe 2, proposer deux groupes
protecteurs R3 et R4
compatibles avec les conditions suivantes : T 25 °C pour la protection et pH >
1 pour la
déprotection.
15. Donner le stéréodescripteur des carbones stéréogènes C1 et C2 dans le cas
de l'alcaloïde 2 en
justifiant.
16. Donner une représentation de Newman de la molécule 2 selon la liaison C1C2
en utilisant la
numérotation de la Figure 5, en plaçant l'atome C1 au premier plan et en se
limitant aux atomes
voisins.
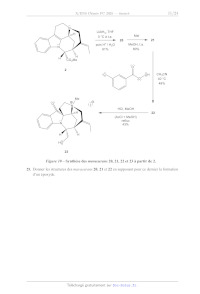
La molécule 13, nécessaire à la fermeture du cycle D, est synthétisée en 3
étapes (Figure 6). La
première étape est de nouveau une réaction de Pictet-Spengler.
14
15
16
13
(majoritaire)
6 / 23
Cat
Figure 6 Synthèse du composé 13 et détail de l'espèce Cat.
17. Le nom du produit 14 en nomenclature IUPAC est :
2-(1H-indol-3-yl)-N-méthyléthan-1-amine.
Déduire de ce nom la structure d'un noyau de type indole.
18. L'emploi de l'espèce Cat permet d'obtenir le composé 15 dans un mélange de
proportion 80/20
des énantiomères R et S, respectivement. Expliquer et justifier le rôle de Cat.
19. Proposer une méthode expérimentale pour séparer les différents
stéréoisomères de 15.
20. Le passage du composé 14 à 13 s'effectue en 3 étapes qui peuvent être
suivies chacune par
spectroscopie IR. Analyser, en s'aidant de l'Annexe 1, ces 3 étapes en
reproduisant et en
remplissant le tableau ci-après :
Étape
Nature
Rôle
Exemple
(ex : oxydation,
réaction acidobasique,
cyclisation...)
(ex : protection,
déprotection,
activation,
aménagement
fonctionnel, ...)
Bande(s) à suivre en
IR (zone en cm-1)
Liaison CC
(1000 1250 cm-1)
Évolution de la (des)
bande(s) en IR
Disparition /
Apparition /
Déplacement
14 15
15 16
16 13
21. Nommer les deux types de sélectivité observés lors de l'ajout de n-BuLi sur
16.
L'addition 1,4 observée lors de l'ajout de n-BuLi sur 16 est inhabituelle en
chimie organique. L'équipe
de recherche a montré lors d'un travail complémentaire que la sélectivité de la
réaction dépend de la
nature du solvant. Ils ont notamment montré par calculs de chimie quantique que
la formation d'un
complexe tétraédrique formé de 4 molécules de n-BuLi autour de l'azote de
l'amine tertiaire la plus
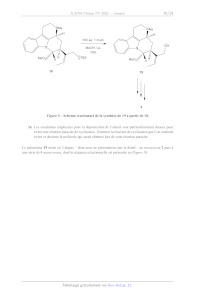
accessible de 16 est nécessaire pour amener à cette addition 1,4 (Figure 7).
22. Entre le THF et le toluène, déterminer quel est le solvant plus favorable à
la formation du
complexe tétraédrique de n-BuLi. Justifier à l'aide des formules topologiques
des deux solvants
données en Annexe 3.
23. En s'appuyant sur la Figure 7, justifier la plus faible énergie associée à
l'état de transition TSAB
par rapport à celui TSAB'.
7 / 23
Figure 7 Profil d'énergies relatives à l'addition de n-BuLi sur 16 pour
former 13. Les énergies
sont calculées pour les complexes A (qui sert ici de référence) et B, ainsi que
pour les états de
transition TSAB et TSAB'. Énergies en kcal·mol1 ; les atomes d'hydrogène sont
omis. Li : violet ;
O : rouge ; N : bleu ; C : gris.
Cette étude détaillée a permis à l'équipe de recherche d'utiliser l'addition
1,4 pour obtenir la molécule
18 en une étape (Figure 8).
Figure 8 Schéma réactionnel de la synthèse de 18 à partir de 16 et 17.
Le précurseur 18 permet d'obtenir des mavacurans. L'étape de déprotection de
l'alcool détaillée en
Figure 9 requiert quelques précautions expérimentales.
8 / 23
Figure 9 Schéma réactionnel de la synthèse de 19 à partir de 18.
24. Les conditions employées pour la déprotection de l'alcool sont
particulièrement douces pour
éviter une réaction parasite de cyclisation. Nommer la réaction de cyclisation
que l'on souhaite
éviter et dessiner la molécule qui serait obtenue lors de cette réaction
parasite.
Le précurseur 19 mène en 3 étapes dont nous ne présenterons pas le détail
au mavacuran 2 puis à
une série de 4 mavacurans, dont la séquence réactionnelle est présentée en
Figure 10.
9 / 23
Figure 10 Synthèse des mavacurans 20, 21, 22 et 23 à partir de 2.
25. Donner les structures des mavacurans 20, 21 et 22 en supposant pour ce
dernier la formation
d'un époxyde.
10 / 23
Partie 2
Autour du norbornadiène
Le norbornadiène (NBD, de formule moléculaire C7H8) est un hydrocarbure
bicyclique capable de se
transformer en l'un de ses isomères, le quadricyclane (QC), sous l'effet d'une
irradiation par lumière
UV, comme illustré sur la Figure 11. Le quadricyclane est un hydrocarbure
polycyclique présentant une
forte tension de cycle, ce qui le rend instable. Par conséquent, il se
reconvertit spontanément en
norbornadiène par une réaction exothermique de cinétique d'ordre 1, présentée
sur la Figure 11.
NBD
QC
Figure 11 Structure des composés NBD et QC et réaction d'isomérisation.
Le système NBD-QC est étudié pour ses applications potentielles dans le
stockage et la conversion de
l'énergie solaire en énergie thermique. Dans cette étude, nous nous intéressons
au norbornadiène non
substitué (NBD) ainsi qu'à un dérivé, noté NBD1, capable de subir une
transformation similaire tout en
présentant une meilleure réactivité sous irradiation solaire. Les structures
des composés NBD1 et QC1
sont représentées sur la Figure 12.
QC1
NBD1
Figure 12 Structure des composés NBD1 et QC1.
L'ensemble de ces composés est solide à température et pression ambiantes.
I Généralités
26. En détaillant le raisonnement, exprimer l'enthalpie standard de la réaction
QC(s) NBD(s) en
fonction des enthalpies standard de sublimation des deux composés ainsi que des
enthalpies
standard de dissociation des liaisons CC et C=C.
Le terme de différence des enthalpies de sublimation est négligeable dans le
cas de ces composés.
27. En déduire la valeur de l'enthalpie standard attendue pour la réaction
QC(s) NBD(s).
28. Citer une technique pour la détermination expérimentale de la valeur de
cette enthalpie standard
de réaction.
11 / 23
On obtient une valeur expérimentale de 113 ± 1 kJmol-1 à 298 K.
29. Proposer une explication justifiant l'écart entre la valeur calculée
précédemment et la valeur
déterminée expérimentalement.
Pour la suite du problème, on utilisera uniquement les valeurs déterminées
expérimentalement.
II Étude de la cyclisation
La transformation photochimique du norbornadiène en quadricyclane est un
processus d'isomérisation
induit par la lumière, reposant sur une cycloaddition [2+2]. Pour mieux
comprendre cette réaction, on
peut modéliser les deux doubles liaisons du NBD en les représentant par deux
molécules d'éthène
isolées.
Avant d'étudier plus en détail cette cycloaddition, on se propose de construire
le diagramme d'orbitales
moléculaires de l'éthène. Ce dernier peut être obtenu en faisant interagir deux
fragments CH, dont les
orbitales de fragment, notées a à f, se combinent deux à deux, comme illustré
ci-dessous sur la Figure
13.
Figure 13 Diagramme d'orbitales moléculaires de l'éthène et orbitales
moléculaires du
fragment CH2.
30. Représenter les orbitales moléculaires de l'éthène numérotées de 4 à 7 sur
la Figure 13, réaliser
le remplissage électronique et identifier la HO et la BV.
31. Identifier les orbitales moléculaires du système de l'éthène, en
justifiant.
Des calculs quantiques donnent l'énergie des HO et BV de l'éthène
respectivement à 10,5 et +1,4 eV.
12 / 23
32. Indiquer pourquoi la cycloaddition [2+2] de l'éthène sur lui-même n'a pas
lieu spontanément.
33. Représenter le diagramme d'OM du système du premier état excité de
l'éthène.
34. Calculer l'ordre de liaison de cet état excité et proposer une structure de
Lewis associée.
35. Identifier la ou les interaction(s) orbitalaire(s) à deux électrons
possible(s) entre deux molécules
d'éthène à l'état excité. Indiquer lesquelles respectent les critères de
recouvrement et
énergétique.
36. En déduire que la cycloaddition [2+2] peut avoir lieu par irradiation
lumineuse.
37. Proposer une expression littérale de la longueur d'onde nécessaire pour
réaliser la cycloaddition
de l'éthène sur lui-même, puis faire l'application numérique et indiquer le
domaine du spectre
électromagnétique auquel appartient cette radiation.
III Étude de la libération d'énergie
Suivi cinétique :
On se propose de réaliser un suivi cinétique de la réaction modèle QC NDB.
Pour cela, on cherche à
suivre la concentration en espèces au cours du temps, en milieu thermostaté.
Parmi les nombreuses techniques de suivi possible, on peut envisager le tracé
des courbes intensitépotentiel à différents instants. En effet, les composés QC
et NBD sont électroactifs et peuvent être
oxydés en QC+ et NBD+ et les potentiels standard des couples sont donnés en
Annexe 3. Les deux couples
sont des couples rapides et on considèrera que les coefficients de diffusion
des espèces sont égaux.
38. Représenter le montage expérimental légendé permettant de tracer les
courbes intensitépotentiel.
39. Identifier une grandeur issue des courbes intensité-potentiel permettant de
suivre facilement
l'évolution des concentrations en NBD et QC.
40. Tracer schématiquement un faisceau de trois courbes enregistrées au cours
de la cinétique en
partant d'une solution pure de QC aux temps t0, t1/2 et t. On négligera les
effets du solvant.
En pratique, le composé QC+, formé lors de l'acquisition des courbes, peut
également se transformer en
NBD+ avec une constante de vitesse différente de QC, et générer un effet dit «
cascade » schématisé cidessous sur la Figure 14 :
Figure 14 Schéma de l'effet cascade redox.
Le temps caractéristique de cet effet cascade est analogue à la durée
d'acquisition d'une courbe intensitépotentiel.
13 / 23
41. Estimer la valeur de la constante thermodynamique d'équilibre à 298 K de la
réaction notée (1)
dans la Figure 14 et commenter cette valeur.
42. Dessiner l'allure réelle de la vague d'oxydation de QC en QC+, en partant
d'une solution
contenant uniquement la forme QC.
43. Commenter alors la pertinence de l'électrochimie pour suivre la cinétique
QC NBD.
44. Proposer une autre technique expérimentale possible pour réaliser ce suivi
cinétique.
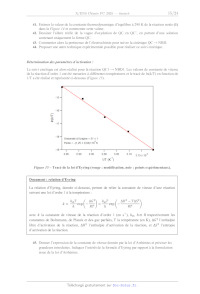
Détermination des paramètres d'activation :
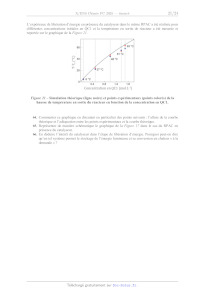
Le suivi cinétique est alors réalisé pour la réaction QC1 NBD1. Les valeurs de
constante de vitesse
de la réaction d'ordre 1 ont été mesurées à différentes températures et le
tracé de ln(k/T) en fonction de
1/T a été réalisé et représenté ci-dessous (Figure 15).
Figure 15 Tracé de la loi d'Eyring (rouge : modélisation, noir : points
expérimentaux).
Document : relation d'Eyring
La relation d'Eyring, donnée ci-dessous, permet de relier la constante de
vitesse d'une réaction
suivant une loi d'ordre 1 à la température :
=
!
!
-
exp +-
0=
exp +-
0
avec la constante de vitesse de la réaction d'ordre 1 (en s1), ! , et
respectivement les
constantes de Boltzmann, de Planck et des gaz parfaits, la température (en K),
l'enthalpie
libre d'activation de la réaction, l'enthalpie d'activation de la réaction, et
l'entropie
d'activation de la réaction.
45. Donner l'expression de la constante de vitesse donnée par la loi
d'Arrhénius et préciser les
grandeurs introduites. Indiquer l'intérêt de la formule d'Eyring par rapport à
la formulation
issue de la loi d'Arrhénius.
14 / 23
46. Déduire de la Figure 15 les valeurs approximatives de H et S et commenter
le signe de
cette dernière valeur.
Suivi calorimétrique en réacteur fermé (modèle 1) :
On cherche à déterminer l'augmentation de température atteinte lors de la
réaction retour en fonction du
temps. Pour cela, on place dans une enceinte calorifugée idéale 10 mL d'une
solution de NBD1 dans du
toluène à la concentration c0 = 1,1 molL1. Une irradiation à 365 nm permet de
convertir
quantitativement NBD1 en QC1, puis le mélange est laissé dans le noir et la
température est mesurée au
cours du temps. On note c(t) la concentration en NBD1 formé à chaque instant et
C la capacité
calorifique massique des composés NBD1 et QC1, considérées identiques pour les
deux isomères.
47. En justifiant précisément le raisonnement, montrer qu'à chaque instant, on
a :
() = # -
% °
()
où K est une constante à exprimer en fonction de la masse volumique du toluène
(Tol), sa
capacité calorifique massique (CTol), la capacité calorifique massique de NBD1
et QC1 (C),
leur masse molaire (M) et leur concentration totale (c0).
48. En déduire que la température est solution d'une équation différentielle de
la forme :
'
= & ( [ + ]
où les constantes , et sont à exprimer en fonction des données du problème.
49. En déduire que la hausse de température maximale atteinte dans le réacteur
T vaut :
T) = -
*! " ,°
.
.
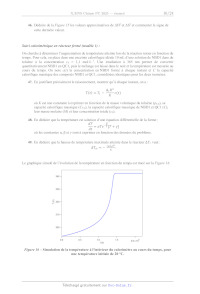
Le graphique simulé de l'évolution de la température en fonction du temps est
tracé sur la Figure 16.
Figure 16 Simulation de la température à l'intérieur du calorimètre au cours
du temps, pour
une température initiale de 20 °C.
15 / 23
50. Commenter l'évolution de la température à l'intérieur du calorimètre ainsi
que l'ordre de
grandeur du temps nécessaire pour atteindre la température maximale et discuter
de la possibilité
d'atteindre cette température expérimentalement dans le calorimètre.
Suivi de la température en réacteur ouvert (modèle 2) :
L'expérience de libération d'énergie, avec la même solution de NBD1 dans le
toluène, est faite dans un
deuxième temps en réacteur ouvert calorifugé modélisé par un réacteur
parfaitement agité continu
(RPAC) avec les caractéristiques suivantes :
Débit volumique : Dv = 5 mLh1
Réacteur : cylindre de diamètre 0,1 cm et de longueur 1 cm
Concentration d'entrée du réactif : / = 1,1 molL1
Température d'entrée du réacteur Te : 20 °C
On cherche à déterminer la température atteinte dans le réacteur, notée T.
51. On note le temps de passage de la solution dans le réacteur. Exprimer et
estimer en fonction
des caractéristiques du réacteur.
52. Exprimer la vitesse v de réaction de QC1 vers NBD1 en fonction du taux de
conversion de QC1
noté , de la constante de vitesse k et de la concentration / .
53. Par un bilan de matière, montrer que : / - = / (1 - )
54. En déduire l'expression de X en fonction de k et uniquement, puis en
fonction de T, et de
toute autre donnée du problème jugée pertinente.
.
55. En effectuant un bilan thermique, montrer que =
(1 - ).
*! 0" ,°
Le code Python incomplet ci-dessous permet de tracer les deux courbes
(cinétique et thermodynamique)
déterminées précédemment.
1 import numpy as np
2 import matplotlib.pyplot as plt
3 import scipy.constants as constants
4
5 # Définition des paramètres :
6 DHact = %
7 DSact = %
8 kB = constants.k # constante de Boltzmann en Unités du Système International
(USI)
9 R = constants.R # constante des gaz parfaits en USI
10 h = constants.h # constante de Planck en USI
11 d = 0.001 # m
12 l = 0.01 # m
13 D = 5e-6/3600 # m^3/s
14 tau = %
15 rhotol = 867 # kg/m^3
16 Ctol = 1800 # J/K/kg
17 C0 = 1.1e+3 # mol/m^3
18 C = 1660 # J/K/kg
19 M = 223e-3 # kg/mol
20 K = %
21 DrH = -88.5e3 # J/mol
22 Te = 20 + 273 # K
23
24 # Définition de la constante de vitesse
25 def k(T):
26
16 / 23
27
28 # Définition de la courbe cinétique
29 def Xcin(T):
30
31
32 # Définition de la courbe thermo
33 def Xtherm(T):
34
return (K/C0/DrH*(Te-T))
35
36 T = np.linspace(Te-20, Te+210, 1000)
37
38 y1 =
39 y2 =
40
41 plt.axis([Te-20, Te+210, 0,1])
42
43 plt.plot(T, y1, 'b', label="courbe cinétique")
44 plt.plot(T, y2, 'b', linestyle="--", label="courbe thermochimique")
45 plt.xlabel('T (K)')
46 plt.ylabel('X')
47 plt.legend()
48 plt.show()
56. Compléter les lignes 26, 30, 38 et 39 du code Python précédent.
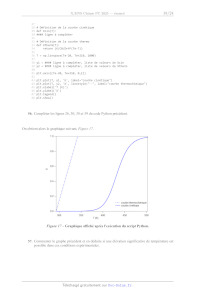
On obtient alors le graphique suivant, Figure 17.
Figure 17 Graphique affiché après l'exécution du script Python.
57. Commenter le graphe précédent et en déduire si une élévation significative
de température est
possible dans ces conditions expérimentales.
17 / 23
58. Identifier deux paramètres expérimentaux sur lesquels jouer pour obtenir
une élévation de
température plus importante.
Modification du procédé par ajout d'un catalyseur :
Ainsi, pour pallier la cinétique lente de la réaction QC1NDB1, le processus se
fait en présence d'un
catalyseur au cobalt, immobilisé sur une surface de charbon.
On donne ci-dessous la structure du catalyseur (Figure 18) :
Figure 18 Structure du catalyseur.
59. Écrire en justifiant la configuration électronique du cobalt (Z = 27),
ainsi que celle de l'ion Co2+.
60. Discuter de l'influence du catalyseur sur la hausse de température maximale
atteinte T , en
regard des questions 49 et 50.
On peut représenter le mécanisme catalysé selon le schéma cinétique suivant où
C est le catalyseur et I
l'intermédiaire réactionnel :
61. En précisant les approximations effectuées, exprimer la vitesse de
formation de NBD dans le
cas du mécanisme catalysé, en fonction des concentrations en catalyseur et QC
et des différentes
constantes de vitesse.
Une étude de chimie quantique a permis de déterminer les structures et les
énergies de l'intermédiaire
et des états de transition (ET) associés à chaque acte élémentaire. L'ensemble
des résultats est reporté
ci-dessous sur la Figure 19.
18 / 23
Figure 19 Diagramme d'énergie de la réaction en présence du catalyseur.
62. En déduire une simplification de la loi de vitesse déterminée précédemment
ne faisant apparaître
qu'une seule des trois constantes de vitesse.
Dans le cas du composé substitué QC1, il existe quatre isomères de
l'intermédiaire I dont les énergies
ont chacune été calculées et reportées ci-dessous dans la Figure 20 :
Figure 20 Énergie et structure des différents isomères de l'intermédiaire
réactionnel (en gris
carbone, rouge oxygène, blanc hydrogène, bleu foncé azote, bleu clair cobalt).
63. Commenter les énergies relatives de ces 4 isomères et représenter le
mécanisme le plus probable
dans le cas du composé QC1, sous forme d'un cycle catalytique.
19 / 23
L'expérience de libération d'énergie en présence du catalyseur dans le même
RPAC a été réalisée pour
différentes concentrations initiales en QC1 et la température en sortie de
réacteur a été mesurée et
reportée sur le graphique de la Figure 21.
Figure 21 Simulation théorique (ligne noire) et points expérimentaux (points
colorés) de la
hausse de température en sortie du réacteur en fonction de la concentration en
QC1.
64. Commenter ce graphique en discutant en particulier des points suivants :
l'allure de la courbe
théorique et l'adéquation entre les points expérimentaux et la courbe théorique.
65. Représenter de manière schématique le graphique de la Figure 17 dans le cas
du RPAC en
présence du catalyseur.
66. En déduire l'intérêt du catalyseur dans l'étape de libération d'énergie.
Pourquoi peut-on dire
qu'un tel système permet le stockage de l'énergie lumineuse et sa conversion en
chaleur « à la
demande » ?
20 / 23
Annexe 1 Données spectroscopiques (IR et RMN)
Table A1 Bandes caractéristiques en spectroscopie infrarouge.
Table A2 Déplacements chimiques de quelques groupes caractéristiques en
spectroscopie RMN
du proton.
21 / 23
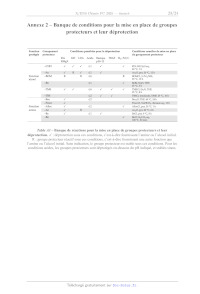
Annexe 2 Banque de conditions pour la mise en place de groupes
protecteurs et leur déprotection
Table A3 Banque de réactions pour la mise en place de groupes protecteurs et
leur
déprotection. : déprotection sous ces conditions, c'est-à-dire fournissant
l'amine ou l'alcool initial.
R : groupe protecteur réactif sous ces conditions, c'est-à-dire fournissant une
autre fonction que
l'amine ou l'alcool initial. Sans indication, le groupe protecteur est stable
sous ces conditions. Pour les
conditions acides, les groupes protecteurs sont déprotégés en-dessous du pH
indiqué, et stables sinon.
22 / 23
Annexe 3 Quelques données physico-chimiques
Formules topologiques du THF et du toluène :
Enthalpies standard de dissociation de liaisons à 298 K :
CC : 350 kJmol-1
C=C : 620 kJmol-1
Enthalpies standard de réaction à 298 K :
QC(s) NBD(s) : 113 kJmol1
QC1(s) NBD1(s) : 89 kJmol1
Potentiels standard à 298 K :
E°(QC+/QC) = 0,56 V
E°(NBD+/NBD) = 1,17 V
Ces potentiels standard sont donnés par référence au couple Fc+/Fc
(ferrocénium/ferrocène) dans le
dichlorométhane.
Numéro atomique du cobalt : Z(Co) = 27
Constante de Boltzmann : kB = 1,38 1023 J·K1
Constante de Planck : h = 6,63 1034 J·s
Constante des gaz parfaits : R = 8,31 J·mol1·K1
Vitesse de la lumière : c = 3,00 108 m·s1
Charge élémentaire : e = 1,60 1019 C
ln(kB/h) = 23,8
RT ln(10) / F = 0,059 V à 298 K
23 / 23
