X/ENS Chimie PC 2021
| Thème de l'épreuve | La tétracyclone et quelques dérivés. Recyclage de cellules photovoltaïques. |
| Principaux outils utilisés | solutions aqueuses, cinétique chimique, oxydoréduction, courbes courant-potentiel, chimie organique |
| Mots clefs | tétracyclone, hexabenzocoronène, triyne, complexe de Shvo, Shvo, ruthénium, cycle catalytique, membrane, Nafion, CEI, panneaux photovoltaïques, indium, gallium, électrodéposition |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)








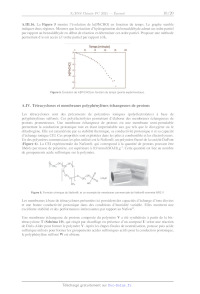
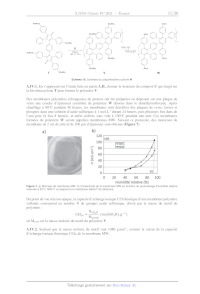








Rapport du jury
(télécharger le PDF)




Énoncé obtenu par reconnaissance optique des caractères
ECOLE POLYTECHNIQUE - ESPCI ECOLES NORMALES SUPERIEURES CONCOURS D'ADMISSION 2021 MARDI 13 AVRIL 2021 14h00 - 18h00 FILIERE PC - Epreuve n° 4 CHIMIE A (XEULC) Durée : 4 heures L'utilisation des calculatrices n'est pas autorisée pour cette épreuve Le sujet se compose d'un problème A et d'un problème B totalement indépendants. Le problème A porte sur la synthèse et l'utilisation de la tétracyclone, un composé de formule brute C29H200 qui est un synthon de base pour de nombreuses espèces organiques et organométalliques. Après la synthèse de la tétracyclone, l'étude se prolonge à celles de plusieurs de ses dérivés : d'abord un macrocycle, l'hexa-péri-hexabenzocoronène, puis un dérivé organométallique, le complexe de Shvo, et enfin des dérivés polymères développés pour la synthèse de membranes échangeuses de protons utilisées dans les piles à combustible. Le problème B traite du recyclage de cellules photovoltaïques. Dix pour cent des panneaux solaires du marché, dits « à couches minces », contiennent des semi-conducteurs complexes composés d'indium, de gallium et de sélénium en particulier. À la différence des panneaux solaires à base de silicium cristallin, recyclables par simple broyage et séparation des différents matériaux (verre, cuivre, silicium), le processus de recyclage des panneaux à couches minces nécessite un traitement électrochimique. Le problème B porte sur la séparation par électrodéposition d'un mélange de cuivre, d'indium et de gallium obtenu après recyclage de panneaux photovoltaïques. Des données utiles sont rassemblées à la fin de chaque problème. Un tableau périodique des éléments est fourni à la toute fin du sujet. Problème A La tétracyclone et quelques dérivés Un soin particulier est attendu dans l'écriture des mécanismes réactionnels ; les représentations devront être des représentations topologiques et faire apparaître les doublets non liants et les formes mésomères des intermédiaires réactionnels s'1l y a lieu. Une représentation simplifiée des molécules ou des ions peut être utilisée dans l'écriture des mécanismes réactionnels ou des équations de réaction mais doit être clairement explicitée. A.[L. Synthèse de la tétracyclone La synthèse de la tétracyclone K (Figure 1) peut être initiée à partir du bromobenzène A (Schéma 1). O (1 () CL Figure 1. Tétracyclone K Cinq étapes conduisent à la formation d'un premier synthon K. Br 1) COzsy -40°C .. + H CN° Mg ii) H30°7/H,0 ----% BB ----% CC -- = Et,0 reflux H,0, EtOH OH A D E Schéma 1. Synthèse du synthon F A.[L.1. Le bromobenzène A est mis à réagir avec du magnésium M£g dans de l'éther diéthylique, EtO, anhydre. Donner la structure de B. A.[L.2. Discuter du choix de l'éther comme solvant, et de la nécessité qu'il soit anhydre. A.[L.3. Donner la structure du composé C. A.[L.4. Indiquer la nature de la réaction qui permet de passer de EUR à D. Préciser quel sous-produit pourrait aussi apparaître. Pour former le composé E, on réalise une condensation de l'aldéhyde D par réaction avec des ions cyanure CN en milieu HO/EtOH. Un mécanisme réactionnel en sept actes élémentaires est proposé sur le Schéma 2. D HO--H a) U A io! cl HO c-- H ZO\ CT 1 Cr 2 y" NE LE Te ICNI | 1: NI RS, [OH Schéma 2. Mécanisme réactionnel proposé pour la synthèse de E à partir de D A.[L.5. Indiquer la nature de chacun des sept actes élémentaires. A.[L.6. Préciser ce qui favorise le départ du proton en alpha du groupement cyano à l'étape 3. A.L.7. Préciser le rôle des ions cyanure. A.LS. Indiquer la nature de la réaction modélisant la transformation du composé E en composé KE et écrire l'équation de la réaction correspondante. Le deuxième synthon J utilisé pour former la tétracyclone K est obtenu à partir de l'acide phénylacétique G (Schéma 3). En le chauffant en présence d'anhydride acétique (CH3CO)O et d'acétate de sodium CH3CO:Na, le composé G forme intermédiairement un composé H, qui lui-même réagit sur G à chaud en présence d'acétate de sodium pour former le composé I. Après décarboxylation de I, on obtient deux composés J et J". G - CO» : > Cao ---------- | ---- + J CH3CO,Na CH3CO,Na chauffage H chauffage Schéma 3. Synthèse du synthon J A.L.9. Indiquer le rôle de l'acétate de sodium dans la transformation du composé G en composé H. Identifier un site électrophile sur l'anhydride acétique. En déduire la structure du composé H. À.1.10. Expliquer pourquoi on utilise l'acétate de sodium et non l'hydroxyde de sodium pour la réaction donnant H à partir de G. A.L.11. Le composé H réagit à nouveau avec l'acide phénylacétique G en chauffant le mélange en présence d'acétate de sodium. Indiquer le produit intermédiaire I obtenu en écrivant le mécanisme impliqué. A.[L.12. Après décarboxylation de [, on obtient deux produits isomères J et J' en équilibre. Nommer J en nomenclature systématique. Donner la structure de l'isomère J" obtenu et indiquer le nom de l'équilibre qui lie J et J". Enfin, les composés F et J réagissent en présence de potasse pour former la tétracyclone K (Schéma À). L ou AO re TU FR K Schéma 4. Synthèse de la tétracyclone K A.[L.13. Proposer un mécanisme réactionnel rendant compte de la formation du composé K à partir des composés J et K. A.[L.14. Indiquer en le justifiant si la tétracyclone K est une molécule plane. En utilisant le modèle de l'oscillateur harmonique pour la liaison entre deux atomes, la loi de Hooke permet de relier le nombre d'onde v mesuré en spectroscopie d'absorption infrarouge à des grandeurs caractéristiques de la liaison : 1 jk ES Z2TC | & MM OÙ U = M +M est la constante de raideur de la liaison. Dans cette loi, c est la célérité de la lumière dans le vide. est la masse réduite, avec m, et m masses des deux atomes engagés dans la liaison, et k Le spectre infrarouge en transmission (pastille de bromure de potassium KBr) du composé F présente deux absorptions à 1677 cm! et 1662 cm! alors que les composés J et K présentent chacun un seul signal, respectivement à 1720 cm ! et 1710 cm. A.[.15. Indiquer à quel groupe caractéristique correspondent ces signaux infrarouges. A.[.16. Interpréter l'écart entre les nombres d'onde de F et ceux des composés J et K. Le raisonnement s'appuiera, entre autres, sur la loi de Hooke. Le composé J a été synthétisé avec un enrichissement en isotope O, puis le spectre infrarouge du composé enrichi a été enregistré. A.[.17. En supposant que la constante de force associée à la liaison C=O ne change pas avec v(C= 0) . . . . À V l'enrichissement isotopique, exprimer le rapport des fréquences 5(C= 180) en fonction des masses molaires des isotopes. A.I.18. Sachant que la résolution du spectrophotomètre est de 1 cm'!, déterminer si le spectre infrarouge permet de repérer le composé enrichi. A.1.19. Indiquer l'intérêt d'enrichir en *O le composé J dans le cadre de l'étude de la synthèse de K. A.IL. Synthèse de l'hexa-péri-hexabenzocoronène La tétracyclone K est un intermédiaire réactionnel permettant d'obtenir des monomères et dimères d'hexa-péri-hexabenzocoronène. L'hexa-péri-hexabenzocoronène fait partie de la famille des hydrocarbures aromatiques polycycliques (HAP). Les HAP désignent des composés dont la structure comprend au moins deux cycles benzéniques fusionnés et 1ls sont classés en fonction du nombre de cycles présents. Ils trouvent leur origine naturelle dans la combustion de matières fossiles. L'hexa-péri- hexabenzocoronène (noté P) est un hydrocarbure macrocyclique constitué d'une molécule centrale de coronène portant six noyaux benzéniques supplémentaires fusionnés entre chaque paire d'anneaux adjacents (Figure 2). Ses dérivés trouvent des applications en électronique et photovoltaïque organique, ainsi que comme sondes fluorescentes en biologie. Certains dimères d'hexa-péri-hexabenzocoronène donnent lieu à du mécanochromisme, un phénomène dans lequel un changement de couleur est provoqué par des actions mécaniques externes telles que le broyage ou l'étirement. a) b) Figure 2. a) Coronène. b) Hexa-péri-hexabenzocoronène P P est synthétisé à partir de la tétracyclone K et d'un deuxième synthon noté N. Ce précurseur N peut être obtenu à partir du benzaldéhyde D. Une première réaction conduit à un mélange d'isomères L et L", lesquels en présence d'un agent bromant produisent l'intermédiaire M. Par chauffage en présence d'hydroxyde de potassium, on obtient le synthon N, caractérisé par une bande vers 2120 cm'! dans le spectre infrarouge. (Schéma 5). L H ? agent bromant KOH -- + + ------------+ chauffage Br Br L' Schéma 5. Synthèse du synthon N A.ITI.1. Proposer un réactif pour former les composés L et L' en une étape à partir de D. Écrire l'équation de la réaction correspondante et donner son nom. A.II.2. Préciser la relation stéréochimique entre L et L". A.IL.3. Donner la structure du composé N. Pour obtenir l'hexa-péri-hexabenzocoronène P, on fait réagir N sur la tétracyclone K, selon une réaction de Diels-Alder suivie d'un dégagement de monoxyde de carbone CO (Schéma 6). - CO FC] FeCl;/CH3NO; + N -------- + CH,Cl K O Schéma 6. Synthèse de l'hexa-péri-hexabenzocoronène P A.IIL.4. Indiquer le rôle respectif de N et K dans la réaction de Diels-Alder conduisant à la formation du composé O. A.IL.5. Dessiner le composé intermédiaire résultant de la réaction de Diels-Alder entre K et N, avant la libération de CO. Pour simplifier, on représentera les cycles phényle par Ph. A.IT.6. Schématiser par des flèches sur le schéma de ce composé intermédiaire, le mécanisme de départ de CO qui conduit à la formation du composé ©. A.IL.7. Donner la nature de la réaction qui permet de passer de l'hexaphénylbenzène O à l'hexa-péri- benzocoronène P. Indiquer le nombre d'électrons et de H* échangés lors de cette réaction. S1 à la place de N, on étudie la réaction de la tétracyclone K sur des dérivés triynes portant des groupements notés --R! (Schéma 7), on obtient deux produits Q et Q° en proportion variable selon la nature de --R1. + R-------- -- ----Rj > Q+Q' K Schéma 7. Réaction d'un triyne portant des groupements --R] avec la tétracyclone K A.IL.8. Donner la structure des deux produits possibles Q et Q" que l'on peut obtenir entre la tétracyclone K et le triyne représenté sur le Schéma 7. Pour simplifier l'écriture, on représentera les phényles par Ph. A.II.9. Donner la structure, en le justifiant, du produit majoritaire obtenu si --R! est le groupement --Si( Pr), où Pr représente le groupement isopropyle -CH(CH:). A.IIT. Un complexe de ruthénium et de tétracyclone : le complexe de Shvo La tétracyclone K est également utilisée pour la synthèse du complexe de Shvo, un complexe organométallique à base de ruthénium Ru, efficace pour certaines réactions d'hydrogénation. L'étude cinétique de l'hydrogénation du benzaldéhyde D en présence du complexe de Shvo sera abordée ici. On obtient le complexe de Shvo sous forme d'un dimère appelé [2-Rul], en deux étapes réactionnelles : [0-Ru] est formé par réaction de la tétracyclone K avec Ru3(CO), puis [2-Rul] est obtenu par réaction de [0-Rul] avec le propan-2-ol (Schéma 8). OH Oo 1 Ph _o À K " Oo, 0 FN Ph Ph H H Rus(CO)2 A 2 h e | \ RU---__,,_---- u Ph ---------- Ru --_ . H Toluène ph DA Ù Ko ph £ « £ Xe Ph 7 \ o N Ph Ph 0 Y 9 O O K [0-Ru] [2-Ru] Complexe de Shvo Schéma 8. Synthèse du complexe de Shvo A.IIL.1. Le complexe Ru:(CO):2 indiqué sur le Schéma 8 est obtenu en faisant réagir du trichlorure de ruthénium RuCl avec du monoxyde de carbone CO et du méthanol CH3OH. Écrire l'équation de la réaction modélisant la formation du complexe, sachant que les autres produits de la réaction sont le méthanal et le chlorure d'hydrogène. Le Schéma 9 présente les étapes élémentaires d'un cycle catalytique d'hydrogénation utilisant le complexe de Shvo. Le complexe de Shvo [2-Ru] est en équilibre avec deux complexes monomères [1-Ru(H)] et [1-Ru|. OQ-H:<0 Ph Ph Ph Ph Ph PSS. Ti--2[i-Ru(H)] K= 7,9 à 60°C Exprimer la constante d'équilibre Ken fonction de ki, k:, k1 et k2, puis donner l'expression de k2/k:1. Estimer ce rapport en utilisant les données reportées dans la Table 2. A.IIT.12. En s'appuyant sur la Figure 3, analyser l'évolution des concentrations en [2-Ru] et [1-Ru(Hb)]. A.IIL.13. La concentration de [1-Ru(Eb)] à t = 0 n'est pas nulle en raison de l'équilibre de dissociation de [2-Ru]. Déterminer la concentration initiale de [1-Ru(H)] en utilisant les données et la loi cinétique de consommation du benzaldéhyde dans l'acte élémentaire décrit à la question A.IIT.4. A.IIL.14. Exprimer, puis déterminer la valeur de v1, vitesse initiale de disparition de [2-Rul]. A.IIL.15. Exprimer le nombre N de tours de cycles réalisés pour chaque dissociation de [2-Ru], en fonction de v. et v3. Déterminer la valeur de N et commenter. A.IIL.16. La Figure 5 montre l'évolution de In[PhCHO\] en fonction du temps. Le graphe semble indiquer deux régimes. Montrer que la réaction d'hydrogénation du benzaldéhyde admet un ordre partiel par rapport au benzaldéhyde en début de réaction et déterminer cet ordre partiel. Proposer une méthode permettant d'avoir accès à l'ordre partiel par rapport à Hb. Temps (minute) 0 20 40 60 80 100 In[PhCHO] 5 ? -6 Figure 5. Évolution de InPhCHO] en fonction du temps (points expérimentaux). A.IV. Tétracyclones et membranes polyphénylènes échangeuses de protons Les tétracyclones sont des précurseurs de polymères ioniques (polyélectrolytes) à base de polyphénylènes sulfonés. Ces polyélectrolytes permettent d'élaborer des membranes échangeuses de protons prometteuses. Une membrane échangeuse de protons est une membrane semi-splitéable permettant la conduction protonique tout en étant imperméable aux gaz tels que le dioxygène ou le dihydrogène. Elle est caractérisée par sa stabilité thermique, sa conductivité protonique © et sa capacité d'échange ionique CET. Ces propriétés sont exploitées dans les piles à combustible et les électrolyseurs. Un des polymères commerciaux les plus utilisés est le Nafion®, un polymère fluoré de la société DuPont (Figure 6). La CET expérimentale du Nafion®, qui correspond à la quantité de protons pouvant être libérés par masse de polymère, est supérieure à 0,9 mmol(SO:H).£ !. Cette quantité est liée au nombre de groupements acide sulfonique sur le polymère. -CF2| cal. Ke: Ver - O Cr Î È 2. O CFa FC Sc Su x H20 -- < VS | 4 { "o CF: HO Figure 6. Formule chimique du Nafion®, et un exemple de membrane commerciale de Nafion® nommée NR211 Les membranes à base de tétracyclones présentées ici possèdent des capacités d'échange d'ions élevées et une bonne conductivité protonique dans des conditions d'humidité variable. Elles montrent une excellente stabilité et des performances intéressantes par rapport au Nafion*. Une membrane échangeuse de protons composée du polymère V a été synthétisée à partir de la bis- tétracyclone T (Schéma 10), qui réagit par chauffage en présence d'un composé U selon une réaction de Diels-Alder pour former le polymère V. Après les étapes finales de neutralisation, potasse puis acide sulfurique utilisés pour former les groupements acides sulfoniques actifs pour la conduction protonique, le polyphénylène sulfoné W est obtenu. SO;NEt; PhNO; T SO;NEt; V W Schéma 10. Synthèse du polyphénylène sulfoné W A.IV.1. En s'appuyant sur l'étude faite en partie A.IT., donner la structure du composé U qui réagit sur la bis-tétracyclone T pour former le polymère V. Des membranes polymères échangeuses de protons ont été préparées en déposant sur une plaque de verre une couche d'épaisseur contrôlée du polymère W dissous dans le diméthylsulfoxyde. Après chauffage à 80°C pendant 48 heures, les membranes sont décollées des plaques de verre, lavées et plongées dans une solution d'acide sulfurique à 1 mol.L:' durant 24 heures, puis plusieurs fois dans de l'eau pure (4 fois 8 heures), et enfin séchées sous vide à 100°C pendant une nuit. Ces membranes formées du polymère W seront appelées membranes MW. Suivant ce protocole, des morceaux de membrane de 2 cm de côté et de 100 um d'épaisseur sont obtenus (Figure 7). a) b) 120 X "NN 100 : ' 80 : = 60 : / 7 40 : si S 20 | Au" O TT 95 O 20 40 60 80 100 Humidité relative (%) Figure 7. a) Morceau de membrane MW. b) Conductivité de la membrane MW en fonction du pourcentage d'humidité relative mesurée à 30°C. NR211 correspond à la membrane Nafion® de référence. 6 (mS.cm'{) »- Du point de vue microscopique, la capacité d'échange ionique CEI théorique d'une membrane polymère sulfonée correspond au nombre N de groupes acide sulfonique, divisé par la masse du motif du polymère : Nso,H CEl,:n = (mol(SO;,H).g71) motif OÙ Mhotir est la masse molaire du motif du polymère V. A.IV.2. Sachant que la masse molaire du motif vaut 1080 g.mol'!, estimer la valeur de la capacité d'échange ionique théorique CEl: de la membrane MW. 10 Au niveau microscopique, la CET peut être déterminée expérimentalement par titrage acido-basique à l'aide d'une solution d'hydroxyde de sodium, qui permet de titrer les protons labiles de la membrane échangeuse d'ions. La CEl:,, se calcule alors en fonction de la masse m de membrane sèche utilisée pour la mesure. Pour mesurer la valeur de la capacité d'échange ionique CET.;, de la membrane MW, on utilise les carrés de 2 cm x 2 cm de 100 1m d'épaisseur, que l'on plonge dans une solution de chlorure de sodium à 2 mol.L'! pendant une nuit. On titre ensuite la solution obtenue avec de l'hydroxyde de sodium. Il faut ajouter 17,0 mL de soude de concentration 1,00x107 mol.L'! pour atteindre l'équivalence. La masse volumique de la membrane sèche est égale à 1,25 g.cm*. A.IV.3. À partir de la définition de la concentration d'échange ionique, exprimer la CELL en fonction des données du titrage acido-basique et de la masse de membrane sèche. A.IV.4. Déterminer la valeur de la capacité d'échange ionique expérimentale CEl.;, de la membrane MW et la comparer à la valeur théorique. Commenter. A.IV.5. Expliquer pourquoi la membrane est plongée pendant une nuit dans une solution aqueuse concentrée de chlorure de sodium avant de mesurer expérimentalement sa capacité d'échange ionique CElexp. A.IV.6. En pratique dans les piles à combustible, ces membranes sont utilisées en milieu humide. En s'appuyant sur les informations fournies sur les membranes, proposer une explication. A.IV.7. Donner l'expression de la CEI volumique, c'est-à-dire de la concentration volumique en groupements acide sulfonique, [SO3H], dans le cas d'une membrane humide. Donner sa valeur dans le cas d'une membrane ayant un volume humide double de celui de la membrane sèche. A.IV.8. Proposer une raison pour laquelle la CEI volumique est plus pertinente comme caractéristique que la CEI massique pour une utilisation comme membrane échangeuse d'ions. A.IV.9. Comparer les propriétés de la membrane MW à celles d'une membrane commerciale Nafion® NR211. Conclure. *K %K % 11 Données utiles pour le problème A Différentes constantes : Constante d'Avogadro : NA = 6x107* mol'! pKa (R-SO:H/R-SO;) < 0 Données spectroscopiques : 1) Sélection de bandes infrarouge : Liaison Groupe d'atomes Fonction ou famille Nombre d'onde Intensité caractéristique (cm1) O-H (libre) C-OH Alcool 3580-3670 Forte O-H (lié par liaison H) C-OH Alcool 3200-3400 Forte Carbonyle -COOH Acide carboxylique 3200-3400 Forte N-H C-NH- Amine, Amide 3100-3500 Moyenne C-H Cycle benzénique Composés 3030-3080 Moyenne --CéHs aromatiques Alcane 2810-3000 Forte Alcène 3000-3100 Moyenne C=C Alcyne 2250-2100 Faible C=O Carbonyle Aldéhyde, cétone 1650-1730 Forte Carbonyle Acide 1680-1710 Forte CO-O-C Ester 1700-1740 Forte CO-N Amide 1650-1730 Forte C=C Alcène 1625-1680 Moyenne C-O Alcool, acide, ester 1050-1450 Forte C-C Alcane 1000-1250 Forte Table IR en cm' 2) Déplacements chimiques moyens caractéristiques de groupes d'atomes NcH OH f O | --C=--= C--H CÇ H O FRS Ke | R N CH -- NH, C : sn À | FX CH -- 9 RO À -- CH -- CI (Br) 1 CH -- NR O | : O F4 " die." R H H | R ne C--C ST w \ R y | 12 10 | 8 6 4 : ô, ppm Table de déplacements chimiques en ppm en RMN du proton Aides aux calculs : [22 = 1.025 : 72 21678 : 7" = 0,88 : © = 2,36 : 20 1,025 4X9,65 144 0x 34=21,25 : 20 24988 8 2,125 1 12 7995.10: 080 Problème B Séparation par électrodéposition d'un mélange d'ions Cu(Il), In(IIT) et Ga(IID) obtenu après recyclage de panneaux photovoltaïques Le CIGS, de l'anglais « Copper Indium Gallium Selenide » (séléniure de cuivre, d'indium et de gallium), est un composé chimique de formule générique Culn,;Ga:,Se2. Il s'agit d'un semi-conducteur utilisé pour réaliser des cellules photovoltaïques à couches minces de haute efficacité. Une cellule photovoltaïque, ou cellule solaire, est composée d'un matériau semi-conducteur qui absorbe l'énergie lumineuse et la convertit en courant électrique (effet photo-électrique). Les cellules de première génération utilisent le silicium sous forme cristalline comme matériau semi-conducteur. Pour ce faire, le silicium est fondu puis refroidi afin d'obtenir un cristal, découpé ensuite en fines tranches appelées « Wafers ». Cette méthode de production est très énergivore. Les cellules solaires à couches minces constituent la seconde génération de technologie photovoltaïque. Dans ce cas, une couche de semi- conducteur est directement déposée sur un substrat comme du verre ou du plastique. La production de ce type de cellules est moins coûteuse que celle de première génération car elle consomme moins de matériau semi-conducteur et ne nécessite pas de passer par l'étape de transformation en « wafers ». Parmi les semi-conducteurs utilisés pour la technologie à couches minces, le CIGS présente l'avantage de pouvoir être déposé sur des surfaces flexibles afin de réaliser des panneaux solaires souples et légers. Pour assurer les ressources en indium et en gallium, le CIGS doit être recyclé. Le recyclage de ces déchets implique un traitement hydrométallurgique qui comprend la dissolution, la précipitation et l'extraction par solvant pour la séparation des éléments. Après cette séparation, l'électrodéposition peut être utilisée pour la récupération de l'indium, du cuivre et du gallium. B.1. Écrire la configuration électronique de l'atome de cuivre dans son état fondamental, selon la règle de Klechkowski. En réalité, la dernière sous-couche s n'est occupée que par un électron. Proposer une explication. B.2. Donner les configurations électroniques des ions Cu* et Cu"*. B.3. La masse molaire atomique du cuivre est égale à 63,546 g.mol'!. Justifier le fait que cette valeur n'est pas un nombre entier. On considère d'abord une solution contenant un mélange modèle d'ions Cu** dans une solution aqueuse d'acide perchlorique HCIO, de concentration 1 mol.L''. La courbe courant-potentiel enregistrée avec une électrode de cuivre (Figure 8, courbe en tirets) montre une seule vague de réduction. L'acide perchlorique HCIO: est un acide fort, et on supposera l'ion perchlorate CIO4 non complexant. 11 électrode de électrode l |: cuivre de carbone 1 . vitreux 1 \ 0,31V 1,0V 0,5V O12V 1 05V 4 + + + - | 1 [I E [039 v Î 1 1 Figure 8. Courbe courant-potentiel en régime stationnaire à 25°C pour Cu(il) en solution aqueuse d'acide perchlorique HCIO: à 1 mol.L'' (courbe en tirets, électrode de cuivre) ou en solution aqueuse de HCI à 1 mol.L'' (courbe en trait plein, électrode de carbone vitreux). Les flèches indiquent le sens du tracé. Le potentiel est mesuré par rapport à l'électrode normale à hydrogène, ENH. 13 B.4. Donner une représentation de Lewis de l'ion perchlorate. Indiquer, en le justifiant, la géométrie autour de l'atome de chlore. B.5. Montrer que l'ion Cu* n'est pas stable dans la solution aqueuse d'acide perchlorique à 1 molL. Écrire l'équation de la réaction correspondante et donner son nom. B.6. Indiquer, en le justifiant, si le couple Cu"*/Cu est rapide ou lent sur électrode de cuivre dans la solution aqueuse d'acide perchlorique à 1 mol.L. B.7. Décrire la courbe courant-potentiel observée sur la Figure 8 dans la solution aqueuse d'acide perchlorique (courbe en tirets) et écrire les réactions électrochimiques associées aux différentes parties de la courbe. B.8. En déduire la concentration en ions Cu"* dans la solution modèle. B.9. Expliquer pourquoi on n'observe pas de palier de diffusion en oxydation sur la courbe courant- potentiel. La Figure 8 présente également la courbe courant-potentiel d'un mélange d'ions Cu** dans une solution aqueuse d'acide chlorhydrique à 1 mol.L'!, sur électrode de travail en carbone vitreux (courbe en trait plein). Pour simplifier, on supposera qu'en milieu acide chlorhydrique à 1 mol.L'}, tout le Cu(ID est sous la forme CuCT* et le Cu(l) sous la forme CuCl:.. L'étude porte ici sur l'électrodéposition du cuivre à partir de la solution d'ions Cu** en milieu acide chlorhydrique. B.10. Reproduire sur la copie le schéma suivant d'un montage d'électrolyse d'une solution d'ions Cu** en solution aqueuse d'acide chlorhydrique, en indiquant : lectrode de C O © É LE Q Électrode de C Dépôt de cuivre a. les pôles du générateur, b. le nom des électrodes. c. le sens de circulation du courant dans le circuit, d. la nature et le sens de déplacement des porteurs de charge lors de l'électrolyse. L'équation de la réaction d'oxydo-réduction modélisant la transformation se déroulant lors de l'électrolyse, si la tension entre les électrodes est suffisante, s'écrit : CuCT (ao) + CT(ac) > Cu + Cl(e) B.11. Déterminer l'enthalpie libre standard de cette réaction à 298 K puis exprimer, sans la calculer, la constante d'équilibre associée. Indiquer s1 la réaction est favorisée ou non, et commenter. B.12. En déduire une expression du potentiel standard du couple CuCT*/Cu. Estimer sa valeur. B.13. La courbe courant-potentiel mesurée montre deux vagues successives en milieu acide chlorhydrique, alors qu'en milieu HCIO: il n'y a qu'une seule vague. Expliquer cette différence en s'appuyant sur la question B.5. B.14. Écrire les équations des réactions électrochimiques ayant lieu à la cathode de carbone vitreux pour un potentiel imposé de -0,30 V/ENH. B.15. Écrire les équations des deux réactions électrochimiques pouvant avoir lieu à l'anode lors de l'électrolyse. 14 On va s'intéresser par la suite à une solution électrolytique contenant un mélange d'ions Cu(IT), In(IIT) et Ga(IIT) en milieu acide chlorhydrique à 1 mol.L'', obtenu lors du recyclage de panneaux photovoltaïques, après les étapes de dissolution, précipitation et extraction. Le cuivre est d'abord récupéré par électrolyse en utilisant une cathode en carbone vitreux avec un potentiel imposé de -0,30 V/ENH. Après avoir récupéré le cuivre et nettoyé la cathode, une seconde électrolyse avec un potentiel appliqué de -0,90 V/ENH permet d'obtenir l'indium. L'électrolyse des ions gallium n'est pas possible dans ce milieu. On considèrera que les contre-1ons des ions métalliques sont des 1ons chlorures CT et que les formes majoritaires de In(IIT) et de Ga(IIT) sont, respectivement, InCl et GaCl4. B.16. Donner deux raisons pour lesquelles on ajoute de l'acide chlorhydrique HCTI dans le mélange Cu(ID), In(IT) et Ga(I) issu du recyclage, avant de démarrer l'électrolyse. La courbe courant-potentiel mesurée avant la première électrolyse (celle de Cu(ID)), pour le mélange d'ions Cu(ID), In(IIT) et Ga(IIT) issu du recyclage, est donnée sur la Figure 9. On n'observe pas d'intermédiaires In(Il) ou In(l) lors de la réduction de In(IT). Le couple Ga(IT)/Ga est lent avec une surtension cathodique importante sur carbone vitreux et n'est pas observé. La concentration en Cu(Il) est celle déterminée à la question B.8. 4 2 | I | | | Electrode .... | | de C 110 V 0/5 V 0,12 V 05 v | } ++ us L ke 10,43 V | E In(IT) | Figure 9. Courbe courant-potentiel sur électrode de carbone vitreux pour un mélange d'ions Cu(ll), In(ll) et Ga(lll) en milieu acide chlorhydrique à 1 mol.L", enregistrée avant la première électrolyse. B.17. Écrire les équations des réactions électrochimiques qui se déroulent à la cathode de carbone vitreux pour un potentiel imposé de -0,90 V/ENH. B.18. Par une résolution graphique, exprimer la concentration initiale de In(IID) en fonction de celle de Cu(ID), en supposant que tous les coefficients de diffusion sont identiques. La Figure 10 montre l'évolution temporelle du courant cathodique d'électrolyse pour une tension imposée de -0,30V/ENH (Figure 10a). Le cuivre se dépose à la surface de la cathode sous forme de fragiles dendrites (Figure 10b). 15 C) 0.15 --0.20 - Courant (A) --0.25 - ne F ET Er" s 2 7 T T 0 2 À 6 Temps (heure) --0.35 - Figure 10. Séparation électrochimique du Cu(Il) et de lIn(Ill) du mélange Cu(ll), In(Hl), Ga(I) : a) courant traversant le circuit en fonction du temps au cours de l'électrolyse pour un potentiel imposé à la cathode de E = -0,30 V/ENH. b) Photo du dépôt de cuivre sur l'électrode de carbone vitreux. c) Photo du dépôt d'indium sur l'électrode de carbone vitreux après électrolyse à un potentiel imposé de E = -0,90 V/ENH. B.19. Expliquer pourquoi l'intensité du courant mesuré au cours de l'électrolyse devient nulle à partir d'une certaine durée (Figure 10a). Lors de l'électrolyse à potentiel imposé à la cathode égal à -0,30 V/ENH, on obtient une masse de cuivre mc déposée sur l'électrode de 0,29 g. Par intégration de la courbe I = f{t), la quantité d'électricité mesurée Q vaut 1000 EUR avec un rendement faradique de 91 %. B.20. Donner la définition du rendement faradique de cette électrolyse et l'exprimer en fonction de n, F, Q, mcu et Mu, où n est le nombre d'électrons échangés, F la constante de Faraday, ma la masse de cuivre déposée, Mc la masse molaire atomique du cuivre. À partir de la solution issue de la première électrolyse, une seconde électrolyse au potentiel imposé à la cathode de -0,90 V est menée avec l'électrode de carbone vitreux nettoyée. L'indium se dépose sur la cathode (Figure 10c). On obtient une masse d'indium mm de 0,46 g à partir d'un mélange de volume 50 mL et de concentration initiale 0,1 mol.L'! en ions In(H). B.21. Exprimer, puis calculer le rendement électrochimique pour l'électrolyse de l'In(IIT) dans Île mélange. Proposer une raison pouvant expliquer que ce rendement électrochimique est inférieur à 100%. Le raisonnement pourra s'appuyer entre autres sur la Figure 10c. B.22. La Figure 9 montre la courbe courant-potentiel avant la première électrolyse, c'est-à-dire t=0 t ° ? N \ D) °° ? n nn ° enregistrée à x = 0 où x est le taux d'avancement de la première électrolyse QE). Recopier Cu(I1) l'allure de cette courbe sur la copie et rajouter sur ce graphe l'allure des courbes courant-potentiel attendues au cours de la première électrolyse pour deux valeurs du taux d'avancement, x = 0,5 etx= 1. Pour pouvoir électrolyser le Ga(IIT), on change d'électrolyte-support et de pH. On se place en solution aqueuse de NaC10O:4 à 4 mol.L'' et de HCIO: à 0,02 mol.L'!, et on mesure dans un premier temps la courbe courant-potentiel en régime stationnaire d'une solution ne contenant que des ions Ga* à la concentration c = 0,001 mol.L'!. On ajoute un excès de thiocyanate de sodium NaSCN (2 mol.L'!) qui conduit à la formation du complexe Ga(SCN):*, puis on retrace une nouvelle courbe courant-potentiel (Figure 11). Les parties correspondant aux courants positifs des courbes sont liées à la méthode de mesure et ne seront pas prises en compte dans l'étude. 16 Figure 11. Courbe courant-potentiel en régime stationnaire pour une solution de Ga(lll) de concentration 0,001 mol.L'' en solution aqueuse de NaCIO, à 4 mol.L'' et de HCIO., à 0,02 mol.L?. La courbe courant-potentiel en trait plein correspond à la solution de Ga** avant l'ajout du thiocyanate de sodium NaSCN ; la courbe en tirets pointillés correspond à l'enregistrement après ajout d'un excès de thiocyanate de sodium (2 mol.L'\). Remarque : l'échelle prise pour l'axe du courant n'est pas la même que celle des figures précédentes. B.23. Écrire les équations des réactions électrochimiques de réduction du Ga(IIT) en Ga(s) en l'absence et en présence d'ions thiocyanate SCN.. B.24. Exprimer, puis déterminer la valeur du potentiel standard du couple Ga(SCN):"/Ga(s). B.25. Indiquer les conditions de potentiel à imposer à la cathode pour réaliser l'électrodéposition de gallium en présence de thiocyanate de sodium. B.26. Conclure sur l'intérêt d'ajouter des ions thiocyanate dans le milieu pour l'électrodéposition du gallium. *K %K % 17 Données utiles pour le problème B Les données suivantes sont toutes exprimées à 298 K : - Potentiels redox de différents couples : redox E° / ENH 1,36 1,23 redox Cu?* CuCl Cu°* E° (V) / ENH 0,34 0,24 0,17 - Enthalpies libres standard de formation en kJ.mol! : CuCF CF -69,81 -131,2 - Constante d'équilibre 2 de formation de Ga(SCN):: : Ga** + 2SCN = Ga(SCN h* : log B2 = 5,60 - Constante de Faraday : F = 10° C.mol'! 2,3RT = 0,06 V Aide au calcul : 0,46 = (0,81 0,57 18 PÉRIODE LA *_4 LA CUS 1 IA RU LR LIT TA 7000007 UT A PR) on: _ _--_--_ Le Mac PRT ie du à Der ss RS US ER SR SUN EC PE 5 108116 12011]7 14007|8 15990|9 18908|10 20.180 DBFRR:T NON ENTER EE ES PCR ET : CIN o RENE TRE DAS :3 ÉCRIRE UE 18 SR ME AIPErS sore ... | OP ETS ETAT CEE TS BP EU . NIET ÉRSTUIE 4 NBS VB 6 VB7 VIB 8 Tr CRE ET RUE RIRE 19 3908620 40078 |21 44056 | 22 47867 | 23 soc? [24 s1.606| 25 54006 [26 s5a45|27 58053[28 56605/20 c3546[30 6530/31 60725/32 7264133 74022|34 7806|35 79004[36 6380 4/ K | Ca | Sc Ti) V | Cr Mn Fe Co] Ni Cu Zn | Ga Ge | As | Se | Br | Kr Dares CES RC SE OR SE OR UE CR UE CURE CRIE ETIENNE TE PC PO PET ET PORT OP OP EE EE PET EEE EEE UT S|Rb|Sr | Y | Zr | Nb Mo) Te | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe DE ane PS ue un CI OR ee CRC Eu RU SR HE CRIE EE PTS ETS ENT LP) ET 7 EEE EC EE PE CEE EEE ES PR ER ET 6, Cs | Ba |Lalu| Hf | Ta | W | Re | Os | Ir | Pt | Au Hg | TI | Pb | Bi | Po | At | Rn CÉSIUM EAU ni | HAFNIUM_|_TANTALE | TUNGSTÈNE| RHÉNIUM CU IRIDIUM RUES OR MERCURE _|_THALLIUM are BISMUTH_| POLONIUM | ASTATE Lau 87 (23)|88 (22)| 89103 |104 (261)|105 (262)/106 (266) 107 (262)/108 (277) | 109 (268)| 110 (281) | 111 (272)| 112 (285) 114 (89) AR: ur " r RIAD TRES DCR BU LUE AE FRANCIUM | RADIUM rl [RUTHERFORDUN| DUBNIUM |SEABORGIUM| BOHRIUM | HASSIUM | MEITNERIUM| UNUNNILIUM| UNUNUNIUM| UNUNBIUM Enr Comp © 1892002 En (en Qi RECETTE CO PES CECI PE CE CES CECILE T0 PTT EC ET pee Pro DT CRE DC DE OCEE S SD)" SRG ES OTRR CT REED) AROUND TS PT RE EC CCE CDR OU re pe EE Actinides CRIE IDETI PET ENT PRE PR D EE OO OT R Lo LA a Nr CORRE TERRE TR EN (( S | Fm | Mid | No | La PTT COTE at ou te en
