Mines Chimie PC 2008
| Thème de l'épreuve | Propriétés physico-chimiques du monoxyde d'azote. Synthèse de prostaglandines. |
| Principaux outils utilisés | thermochimie, cinétique, oxydoréduction, orbitales moléculaires, chimie organique |
| Mots clefs | monoxyde d'azote, Diels-Alder, racémique (résolution), transfert d'électron ligand-métal, prostaglandines, Corey, ruthénium (complexe du) |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)













Rapport du jury
(télécharger le PDF)


Énoncé obtenu par reconnaissance optique des caractères
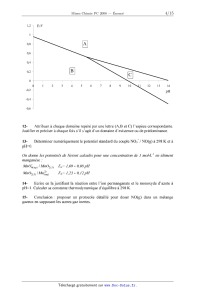
A 2008 Chimie PC ÉCOLE NATIONALE DES PONTS ET CHAUSSÉES, ÉCOLES NATIONALES SUPÉRIEURES DE L'AÉRONAUTIQUE ET DE L'ESPACE, DE TECHNIQUES AVANCÉES, DES TÉLÉCOMMUNICATIONS, DES MINES DE PARIS, DES MINES DE SAINT-ETIENNE, DES MINES DE NANCY, DES TÉLÉCOMMUNICATIONS DE BRETAGNE ÉCOLE POLYTECHNIQUE (FILIÈRE TSI) CONCOURS D'ADMISSION 2008 CHIMIE Filière : PC (Durée de l'épreuve : 4 heures) Sujet mis à disposition des concours : ENSTIM, Télécom SudParis (ex INT), TPE-EIVP Les candidats sont priés de mentionner de façon apparente sur la première page de la copie CHIMIE 2008 - Filière PC L'usage d'ordinateur ou de calculette est interdit. L'énoncé de cette épreuve, particulière aux candidats de la filière PC, comporte 15 pages. · Les candidats pourront admettre tout résultat fourni dans l'énoncé, qu'ils n'auraient pas établi, mais qui serait utile dans la poursuite de l'épreuve. · Les candidats ne devront pas hésiter à formuler des commentaires succincts qui leur sembleront pertinents, même si l'énoncé ne le demande pas explicitement, à condition qu'ils s'inscrivent dans le programme du concours et soient en rapport avec le problème posé. · Le barème tiendra compte de la longueur de l'énoncé. · Si, au cours de l'épreuve, le candidat repère ce qui lui semble être une erreur d'énoncé, il le signale sur sa copie et poursuit sa composition en expliquant les raisons des initiatives qu'il est amené à prendre. Page 1/15 Tournez la page S.V.P. Chimie 2008 Filière PC DEBUT DE L'ENONCE Partie A : quelques propriétés physico-chimiques des dérivés oxygénés de l'azote On s'intéresse dans ce problème à quelques caractéristiques physico-chimiques du monoxyde d'azote et de ses dérivés. Formation du monoxyde d'azote Le chlorure de nitrosyle NOCl(g) se décompose en fournissant du monoxyde d'azote selon l'équation : 2 NOCl (g) = 2 NO (g) + Cl2 (g) 1Proposer une structure de Lewis pour NOCl et étudier la géométrie de l'édifice par la méthode VSEPR (N est l'atome central). 2En considérant les données à la fin de l'énoncé et l'approximation d'Ellingham, à quelle température T1 (on se contentera d'une précision à 10 degrés près) la constante d'équilibre vaut-elle K(T1) = 0,2 ? Quelle est l'influence de la température sur cette constante K? 3On se place désormais à cette température T1. En supposant que l'on parte de n0 moles de NOCl(g) pur, établir la composition à l'équilibre pour une pression totale P=0,2 bar. 4Etudier par un calcul différentiel l'influence d'une légère diminution isotherme de la pression sur la position de l'équilibre. 5Conclusion : quelles sont les conditions expérimentales qui favorisent la synthèse de monoxyde d'azote ? Le monoxyde d'azote, intermédiaire réactionnel. La décomposition thermique du pentaoxyde de diazote, réalisée en phase gazeuse dans un récipient de volume constant, conduit au dioxyde d'azote et au dioxygène suivant une réaction totale dont l'équation bilan est : N2O5 ! 2NO2 + " O2 Tous les gaz sont supposés parfaits. On introduit une mole de N2O5 dans un récipient de volume V = 10L maintenu à ! = 140°C à l'instant t = 0. La pression initiale Pi dans le récipient vaut Pi = 3,4 bar. 6- Quelle sera la pression dans le récipient pour un temps t infini ? Page 2/15 Chimie 2008 Filière PC ( ) On suit la cinétique de cette réaction en traçant la courbe ln PN 2O 5 /P 0 en fonction du 0 temps, où PN 2O 5 est la pression partielle en N2O5 dans le récipient et P la pression standard. Cette courbe est une droite. On constate d'autre part qu'il reste 0,5mol de N2O5 dans le récipient au temps t = 7s. 7- On suppose que la loi cinétique se met sous la forme v = k[N2O5]a. Déterminer l'ordre de la réaction et la valeur de la constante de vitesse k. (on prendra: ln2 = 0,7) 8- Etablir la loi donnant la pression totale P dans le récipient en fonction du temps. Afin de rendre compte des résultats expérimentaux, on propose le mécanisme suivant : k1 NO2 + NO3 (1) N2O5 k-1 (2) NO3 (3) NO + + k2 NO2 NO + O2 + NO2 k3 N2O5 3 NO2 L'équilibre (1) est rapide tandis que l'étape (2) est lente. 9- S'agit-il d'un mécanisme par stades ou en chaîne ? Justifier. 10- On suppose que l'étape (2) est l'étape cinétiquement déterminante. Montrer que le mécanisme est compatible avec l'ordre expérimental déterminé et exprimer la constante de vitesse k en fonction des constantes de vitesse ki des réactions élémentaires. Titrage du monoxyde d'azote en solution aqueuse On étudie le comportement des espèces oxygénées de l'azote en solution aqueuse. Les espèces considérées sont : NO(g), HNO2 (acide nitreux), NO2 (ion nitrite) et NO3 (ion nitrate). 11- Préciser le nombre d'oxydation de l'azote dans chacun de ces composés. On donne ci-après le diagramme potentiel-pH pour les espèces oxygénées de l'azote considérées. La concentration de tracé est prise égale à 0,1 mol·L-1 et la pression de tracé est prise égale à 0,1 bar. Page 3/15 Tournez la page S.V.P. Chimie 2008 Filiere PC 12 E/ V 12- Attribuer à chaque domaine repéré par une lettre (AB et C) l'espèce correspondante. Justifier et préciser à chaque fois s'il s'agit d'un domaine d'existence ou de prédominance. 13- Déterminer numériquement le potentiel standard du couple N03- / NO(g) à 298 K et à pH=O. On donne les potentiels de Nernst calculés pour une concentration de ] mol--L" en élément manganèse : MnO2(S) /Mn(2;q) E!): 1,23 - 0,12pH 14- Ecrire en la justifiant la réaction entre l'ion permanganate et le monoxyde d'azote à pH=l. Calculer sa constante thermodynamique d'équilibre à 298 K. 15- Conclusion: proposer un protocole détaillé pour doser NO(g) dans un mélange gazeux en supposant les autres gaz inertes. Page 4/15 Chimie 2008 Filière PC Diagramme d'orbitales moléculaires du monoxyde d'azote. 16Donner la configuration électronique des atomes O et N dans leur état fondamental. Citer avec précision chacune des règles permettant d'affirmer ce résultat. Distinguer les électrons de coeur et les électrons de valence dans les deux cas. 17- Proposer une formule de Lewis pour le monoxyde d'azote. On cherche à justifier simplement le positionnement énergétique relatif des couches de valence de l'oxygène et de l'azote. On utilise le modèle de Slater. 18Expliquer en quelques lignes en quoi consiste la modélisation de l'atome polyélectronique par la méthode de Slater. 19A l'aide des données fournies en fin d'énoncé, calculer numériquement les constantes d'écran pour les électrons de valence des atomes d'oxygène et d'azote ainsi que les numéros atomiques effectifs correspondants. En déduire lequel de ces deux atomes possède les orbitales atomiques de valence les plus basses en énergie. 20Corréler le résultat de la question précédente à la différence d'électronégativité entre l'oxygène et l'azote (il pourra être utile de situer O et N dans la classification périodique des éléments). On souhaite établir le diagramme d'orbitales moléculaires du monoxyde d'azote NO en utilisant la méthode CLOA (combinaison linéaire d'orbitales atomiques). Les seules orbitales atomiques retenues dans les combinaisons linéaires sont des orbitales atomiques correspondant aux électrons de valence (et celles de même nombre quantique n) conduisant à un recouvrement non nul. Les niveaux ns et np ne sont plus considérés comme étant à la même énergie. Dans un premier temps on néglige tout recouvrement entre orbitales s et orbitales p. 21Construire avec ces hypothèses le diagramme d'orbitales moléculaires du monoxyde d'azote. On pourra procéder par analogie avec la molécule O2. En réalité on ne peut pas négliger le recouvrement entre orbitales atomiques s et p. Le diagramme d'orbitales moléculaires est alors constitué de 8 orbitales "i (i=1 à 8) d'énergie croissante avec i, les orbitales "3 et "4 étant dégénérées, ainsi que "6 et "7. 22Préciser pour chaque orbitale !i les orbitales atomiques ayant servi à sa construction et sa symétrie " ou #. Donner la configuration électronique fondamentale du monoxyde d'azote. 23- Calculer l'indice de liaison de NO. Comment évolue la longueur de liaison N-O - + quand on passe de l'ion NO à la molécule NO puis à l'ion NO ? Justifier. Page 5/15 Tournez la page S.V.P. Chimie 2008 Filière PC La molécule de monoxyde d'azote absorbe un rayonnement infra-rouge de longueur d'onde !=5,26 µm, le monoxyde de carbone absorbe un rayonnement infra-rouge de longueur d'onde !=4,66 µm et le nombre d'onde d'une liaison C=O (groupement carbonyle) est approximé à 1700 cm-1 (soit !=5,88 µm). 24Classer les constantes de force k des oscillateurs harmoniques modélisant les liaisons NO du monoxyde d'azote, CO du monoxyde de carbone et CO du carbonyle. En supposant que la nature des éléments chimiques liés influe de façon négligeable sur la constante de force, corréler ce classement avec l'indice de liaison précédemment calculé. Propriétés complexantes du monoxyde d'azote Le monoxyde d'azote forme des complexes stables avec le ruthénium Ru, dont on propose ici une étude simplifiée. 25Le ruthénium se situe juste en dessous du fer dont le numéro atomique est Z=26 dans la classification périodique des éléments. Situer le ruthénium par ses numéros de ligne et de colonne. Indiquer le numéro atomique du ruthénium. 26Le ruthénium forme avec la pyridine (notée py) et l'ion chlorure un complexe de formule [Ru(py)4Cl2]. La formule de la pyridine est rappelée ci-après. Comment expliquer la formation de liaison entre le ruthénium et la pyridine ? Donner le degré d'oxydation du ruthénium dans le complexe. N Pyridine + Quelques opérations conduisent ensuite à la formation du complexe [Ru(py)4Cl(NO)] dans lequel le ligand NO remplace l'un des ligands chlorure. Une analyse par spectroscopie de rayons X montre que l'unité Ru-N-O est pratiquement linéaire, l'atome de ruthénium est lié au ligand par l'intermédiaire de l'atome d'azote. 27Proposer une structure de Lewis de l'unité Ru-N-O rendant compte de cette géométrie d'après la méthode VSEPR. L'unité NO est chargée dans cet édifice. Quel transfert d'électron est mis en évidence ? 28On donne pour le complexe [Ru(py)4Cl(NO)]+ les données structurales suivantes : la distance Ru-NO vaut 176 pm tandis que la distance Ru-py vaut 211 pm. Corréler ce résultat avec la structure de Lewis proposée à la question précédente. On cherche à expliquer la formation de la liaison Ru-NO par la méthode des orbitales moléculaires. On retient pour le monoxyde d'azote, dans cette approche simple, les orbitales correspondant aux deux derniers niveaux d'énergie occupés (un total de trois orbitales moléculaires). On retient pour le ruthénium les orbitales d correspondant aux électrons de valence. La forme et le nom des orbitales d sont rappelés ci-après. La liaison Ru-NO est orientée le long de l'axe z. Page 6/15 Chimie 2008 Filière PC z dz2 y dx2-y2 y x y dxy x x z z dyz dxz y x 29Quelles sont les orbitales d conduisant à un recouvrement non nul avec chacune des orbitales retenues sur le ligand NO ? 30Proposer un diagramme d'orbitales moléculaires simplifié pour l'entité Ru-NO à partir des orbitales d du ruthénium et des orbitales retenues sur le ligand NO. Procéder au remplissage des niveaux d'énergie de l'édifice Ru-NO. On considérera que le niveau d'énergie des orbitales d est situé entre les deux niveaux d'énergie considérés pour NO. 31- Conclusion : interpréter le transfert d'électron de la question 27- Page 7/15 Tournez la page S.V.P. Chimie 2008 Filière PC Partie B: synthèse de prostaglandines Ce problème est basé sur les travaux de E.J. COREY concernant les prostaglandines PGF2" et PGE2 (COREY, E.J. ; WEINSHENKER, N.M. ; SCHAAF, T.K. ; HUBER, W. J. Am. Chem. Soc. 1969, 91, 5675.) Les prostaglandines PGF2" et PGE2 appartiennent à une famille de molécules découvertes dans les années 30, mais dont les premières structures connues ont été proposées en 1966. HO H 6 5 1 COOH 2 PGF2! 10 8 4 9 3 HO O H 7 HO H H COOH HO PGE2 H HO H 32En supposant la stéréochimie des fonctions alcènes fixée, déterminer le nombre de stéréoisomères de configuration de la prostaglandine PGF2" . Préciser les descripteurs stéréochimiques (R ou S) adaptés C1* et C4*. La réponse sera justifiée par l'ordre de priorité de chacun des substituants des atomes asymétriques. Une numérotation des atomes est proposée par souci de clarté. La molécule de départ de la synthèse est le cyclopentadiène dont la structure est indiquée ici. Cyclopentadiène 33Le cylopentadiène a un pKA égal à 16. Représenter la base conjuguée et justifier la relative acidité de ce composé. Page 8/15 Chimie 2008 Filière PC Le cylopentadiène A est fraîchement distillé, puis mis en présence d'hydrure de sodium NaH dans le THF à -55°C. Du chlorométhoxyméthane est ajouté pour fournir la molécule B. 34La distillation préalable du cyclopentadiène a pour but d'éviter la présence de la substance A' ci-après. Proposer une explication à la formation de A'. Les orbitales moléculaires # du cyclopentadiène (assimilé au butadiène) sont précisées en données. Justifier la stéréochimie de A' en représentant dans l'espace le mode d'attaque conduisant à la molécule observée. H A' 35- H Indiquer la structure de B en précisant le mécanisme le plus probable. 36Indiquer le nombre de signaux et la forme des signaux a priori attendus lors de la réalisation du spectre RMN 1H de la molécule B. Justifier simplement. La suite de la synthèse est la suivante : H3CO H3CO Cl KOH/H2O CN B Cl DMSO C D CN O A H3CO E 1) NaOH/H2O MCPBA B 2) acidification légère O O D F E C 37Expliciter le mécanisme de formation de C sans chercher à justifier la stéréochimie (les stéréochimies précisées ci-dessus sont celles des produits souhaités). Cette réaction est Page 9/15 Tournez la page S.V.P. Chimie 2008 Filière PC menée plus rapidement en présence d'un acide de Lewis (Cu(BF4)2). Justifier simplement ce résultat. 38L'action de l'acide métachloroperbenzoïque (MCPBA) sur D en présence d'hydrogénocarbonate de sodium dans le dichlorométhane conduit à la formation de E. Représenter la structure de Lewis de l'acide métachloroperbenzoïque et proposer une réaction secondaire pouvant nuire au rendement de la réaction de formation de E. 39Proposer un mécanisme pour la réaction conduisant de E à F et indiquer le produit de réaction en utilisant le modèle de représentation proposé ci-dessus (le cycle à 5 atomes est considéré comme plan, indiquer les substituants du cycle en précisant clairement la stéréochimie). 40La molécule F est en réalité obtenue sous forme d'un mélange racémique. Où se trouve à votre avis l'origine de l'obtention de ce mélange dans la séquence réactionnelle ? 41Une méthode pour ne conserver que le stéréoisomère F souhaité et dessiné avant la question 37- consiste à faire réagir le mélange racémique contenant F avec la (+)-éphédrine dans le benzène (avec chauffage). Que signifie (+) ? A quelle réaction assiste-t-on ? Comment cette réaction permet-elle a priori une séparation de deux énantiomères ? CH3 HO N H (+)-éphédrine 42Le produit formé F' issu de F est un solide purifié par recristallisation. Expliquer en quoi consiste cette opération. 43- Comment achever le processus et obtenir F stéréochimiquement pur ? 44Rappeler le mécanisme d'addition du dibrome Br2 sur le cyclopentène. Quels sont les produits obtenus ? En quel nombre ? L'action du diiode sur F en milieu aqueux, en présence d'une base type hydrogénocarbonate HCO3 et à 0°C conduit à la formation de la molécule G représentée ci-après. Page 10/15 Chimie 2008 Filière PC O O G I OCH3 HO 45- Proposer un mécanisme pour rendre compte de ce résultat. L'action de l'anhydride éthanoïque sur G conduit à la formation de H. 46- Donner la structure de H. L'action de l'hydrure de tributylétain en présence d'une quantité catalytique d'azobisisobutyronitrile (AIBN) conduit au remplacement de la liaison C-I par C-H. On obtient alors la molécule I (lactone de Corey). Le clivage de la fonction éther-oxyde en alcool correspondant (et bromométhane) est effectué par action de tribromure de bore BBr3 à 0°C suivie d'hydrolyse. On obtient la molécule J. 47Donner la structure de Lewis de BBr3 et indiquer à quelle famille de composés il appartient. 48- Préciser la structure de J. J subit l'action du trioxyde de chrome en présence de deux équivalents de pyridine dans le dichlorométhane à 0°C. On obtient K. 49- Préciser la structure de K. La synthèse est poursuivie : O H3CO P OCH3 L NaH, 25°C K M + O La réaction est menée dans le 1,2-diméthoxyéthane comme solvant. La molécule L possède un hydrogène légèrement acide. Page 11/15 Tournez la page S.V.P. Chimie 2008 Filière PC 50Identifier cette acidité et indiquer la structure de la base conjuguée. Quel gaz se dégage lors de la synthèse ? 51On indique que dans les conditions de l'expérience, un alcène de configuration E est formé. Par analogie avec une réaction connue, engageant elle aussi un dérivé du phosphore, préciser la structure de M. 52Comment évolue la bande d'absorption C=O en infra-rouge lorsqu'on passe de L à M ? Justifier simplement. L'action du tétrahydruroborate de sodium NaBH4 sur M conduit à la formation de N sous forme de deux stéréoisomères (N1 et N2 ). 53Préciser quels sont ces deux stéréoisomères et indiquer la nature précise de la relation de stéréoisomérie qui les unit. Les deux stéréoisomères précédents sont séparés par chromatographie sur couche mince. 54Rappeler le principe d'une chromatographie sur couche mince, on s'attachera dans cette explication à utiliser les termes « adsorption », « phase stationnaire/mobile », « éluant ». 55Le stéréoisomère recherché N1 pour la suite de la synthèse possède une fonction alcool portée par un centre de descripteur stéréochimique S. Identifier le stéréoisomère N1. 56N2 (séparé par chromatographie) est oxydé par du dioxyde de manganèse MnO2 puis de nouveau réduit par NaBH4 avant de procéder à une nouvelle chromatographie. Commenter cette séquence oxydation-réduction, quel est le but recherché ? L'action du méthanol sur N1 en présence d'ions carbonate permet l'obtention d'un diol tout en conservant la présence de la lactone (ester cyclique). 57- Indiquer la structure du composé O obtenu. Comment s'appelle cette réaction ? Les deux fonctions alcools sont protégées par action du dihydropyrane (DHP) en milieu acide (acide paratoluène sulfonique). On cherche à étudier cette réaction. O DHP 58L'action d'un ion H+ sur le DHP conduit préférentiellement à un cation. Identifier ce cation et justifier son obtention préférentielle. Pourquoi préférer l'acide paratoluène sulfonique à un acide type acide sulfurique lors de cette synthèse ? 59Préciser le produit obtenu après action d'un alcool sur du DHP en milieu acide. Quelle est la nouvelle fonction chimique créée ? Page 12/15 Chimie 2008 Filière PC Dans la suite les fonctions alcools R-OH présentes dans O seront supposées protégées sous la forme R-OTHP (THP désigne un fragment tétrahydropyrane) dans une molécule appelée P. L'hydrure LiAlH(OEt)3 (triéthoxyaluminohydrure de lithium) est ajouté à la molécule P. Ce réactif est comparable à LiAlH4 mais permet de limiter la réaction à l'addition nucléophile d'un seul ion hydrure à un groupe ester. 60Quel est, dans ces conditions, le dérivé organique Q obtenu après ajout d'eau ? On écrira le mécanisme de la réaction en supposant que LiAlH(OEt)3 fournit un ion H nucléophile. Quelle fonction particulière vient d'être créée ? Avec quel composé monocylique R la molécule bicyclique Q est-elle en équilibre ? (dans cette terminologie, les cycles présents dans les motifs THP ne sont pas considérés). La molécule Q est mise à réagir dans le diméthylsulfoxyde avec la molécule R pour fournir la molécule S. COO Ph3P 61S. R La fonction alcène formée est de stéréochimie Z. Préciser la structure de la molécule Une acidification légère permet une déprotection des fonctions alcools et l'obtention de la prostaglandine PGF2" . 62- Proposer un mécanisme pour cette déprotection. 63Proposer une réaction parasite pouvant avoir lieu en absence de la séquence protection/déprotection proposée dans la synthèse. - 64L'action des ions dichromate Cr2O72 sur la molécule S en milieu acide conduit à une molécule T qui ne possède plus de fonction alcool. Quelle est cette molécule ? Ecrire l'équation-bilan convenablement équilibrée pour la transformation S-T. La déprotection des fonctions alcools permet alors l'obtention de la prostaglandine PGE2. Page 13/15 Tournez la page S.V.P. Chimie 2008 Filière PC Données Numéros atomiques : Z(H) = 1, Z(B) = 5, Z(C) = 6, Z(N) = 7, Z(O) = 8, Z(P) = 15, Z(Cl) = 17. Masses molaires (g·mol-1) : M(C) = 12 ; M(N) =14 ; M(O) =16 ; M(Cl) =35,5 . Facteurs d'écrantage selon les règles de Slater : Electron Contribution des autres électrons étudié Niveaux Niveau Autres électrons du niveau n (niveau n) n-2, n-3 , ... n-1 1s s et p d f 1s 0,30 ns np 1,00 0,85 0,35 0 0 nd 1,00 1,00 1,00 0,35 0 nf 1,00 1,00 1,00 1,00 0,35 Niveaux supérieurs 0 0 0 0 n : nombre quantique principal 1 2 3 4 5 6 n* : nombre quantique principal apparent 1 2 3 3,7 4,0 4,2 Orbitales moléculaires ! du cyclopentadiène 2 3 1 4 OM 1 OM 2 OM 3 OM 4 C1 0.372 0.602 0.602 0.372 C2 0.602 0.372 -0.372 -0.602 C3 0.602 -0.372 -0.372 0.602 C4 0.372 -0.602 0.602 -0.372 Energie $+1,618% $+0,618% $-0,618% $-1,618% Données thermodynamiques à 298 K : Enthalpies standard de formation : &fH°(NOCl(g))= 51,7 kJ·mol-1, : &fH°(NO(g))= 90,2 kJ·mol-1. Entropies molaires standard : S°m(NOCl(g))= 262 J·K-1·mol-1, S°m(NO (g))= 211 J·K-1·mol-1, S°m(Cl2(g))= 222 J·K-1·mol-1. Potentiels standard à 298 K et pH= 0 : E°(NO3 /NO2 ) = 0,85 V ; E°(NO3 /HNO2) = 0,94 V; Page 14/15 Chimie 2008 Filière PC - E°(NO2 /NO(g)) = 1,18 V ; E°(HNO2/NO(g)) = 0,99 V . - pKA(HNO2/NO2 ) = 3,3 à 298 K. Données numériques : ' 1 / 14 + 1 / 16 $ " ! 0,95. % & 1 / 12 + 1 / 16 # Rln(0,2)' -13 avec R constante des gaz parfaits. RT ln(10)/F = 0,06 V à 298 K. Fin de l'énoncé Fin de l'épreuve Page 15/15 Tournez la page S.V.P.
