ENS Chimie B PC (U) 2025
| Thème de l'épreuve | Le cofacteur flavine dans tous ses états. Synthèse de l'alliacol A. |
| Principaux outils utilisés | diagrammes E-pH, solutions aqueuses, cinétique chimique, chimie de coordination, orbitales moléculaires, chimie organique, informatique pour tous |
| Mots clefs | flavine, quinone, hydroquinone, FMN, fluorescence, flavoprotéine, riboflavine, lumiflavine, Michaelis-Menten, alliacol |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)









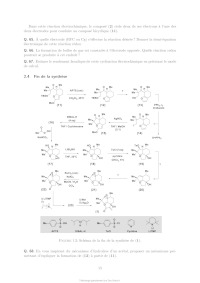





Rapport du jury
(télécharger le PDF)


Énoncé obtenu par reconnaissance optique des caractères
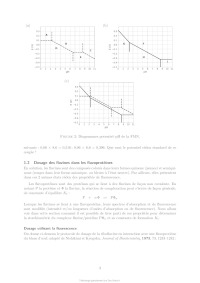
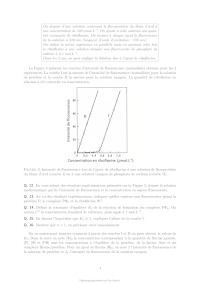
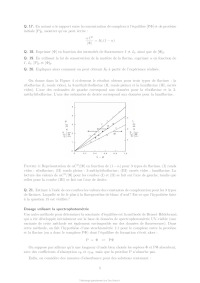
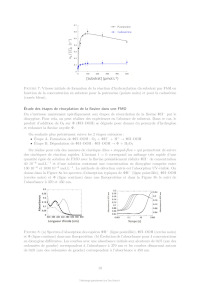
Le sujet comprend 21 pages numérotées de 1 à 21. Début du sujet Les parties 1 et 2 sont totalement indépendantes. Si au cours de l'épreuve un·e candidat·e repère ce qui lui semble être une erreur d'énoncé, il·elle le signale dans sa copie et poursuit sa composition en indiquant les raisons des initiatives qu'il·elle est amené·e à prendre. Une indication du poids relatif de chaque partie dans le barème total est donnée à la suite du titre de chaque partie. Un soin particulier est attendu dans l'écriture des mécanismes réactionnels ; les formules utilisées devront faire apparaître les doublets non liants, les lacunes électroniques et les formes mésomères des intermédiaires réactionnels s'il y a lieu. L'écriture des mécanismes pourra se faire sous une forme simplifiée (les parties de la molécule non impliquées dans le mécanisme réactionnel seront écrites avec les symboles R, R , R ... en précisant la simplification effectuée). Des données pertinentes pour les différentes parties sont fournies en annexe à la fin du sujet. 1 Première partie : Le cofacteur flavine dans tous ses états Cette partie représente environ 65% du total des points. Les flavines sont des cofacteurs très communs en biologie. On les retrouve dans de très nombreux processus (respiration, nombreuses réactions catalytiques), dans lesquels elles sont impliquées dans des réactions de transfert d'électron et de proton. Les flavines peuvent en effet échanger 2 électrons et 2 protons. La flavine possède trois degrés d'oxydation : la forme quinone, la plus oxydée ; la forme semi-réduite dite semiquinone ; et la forme totalement réduite hydroquinone. La formule semi-développée générique des flavines dans la forme quinone totalement déprotonée est reproduite sur la Figure 1. Cette forme sera notée par la suite . Les flavines possèdent toutes le même noyau isoalloxazine, constitué de trois cycles à 6, et diffèrent par la nature du groupement R. Certains atomes du cycle isoalloxazine ont été numérotés selon une numérotation standard qui sera utilisée dans la suite du problème. O 5 5a 9a N 3 4a 4 NH 10 N 10a N R O 1 Figure 1: Formule semi-développée générique des flavines dans la forme quinone totalement déprotonée. Le noyau isoalloxazine, commun à toutes les flavines, est lié à un groupement R qui distingue les différentes flavines. 1 1.1 Réactivité rédox de la flavine mononucléotide Dans cette partie on va s'intéresser aux différentes formes rédox et acido-basiques de la flavine mononucléotide (FMN). On utilisera la notation générique pour décrire la forme la plus oxydée et totalement déprotonée, telle que représentée sur la Figure 1. La forme hydroquinone doublement protonée est une forme neutre qui sera donc notée H2 . Différentes données thermodynamiques relatives aux couples rédox et acidobasiques de la FMN sont données en annexe. Dans cette partie, on travaille en phase aqueuse à 298 K et on précise que toutes les espèces sont solubles. Q. 1. Quels sont les deux sites de protonation envisageables sur le groupement isoalloxazine ? Justifier. Q. 2. Ces deux sites ne sont pas équivalents. En raisonnant sur la proximité avec les groupes CO, quel est celui qui est protoné le plus facilement ? Justifier. Q. 3. Quelles sont les 9 formes rédox et acido-basiques qu'on peut potentiellement imaginer entre les formes et H2 ? Les classer par état d'oxydation croissant. On ne demande pas d'écrire les formes semi-développées de ces espèces. Q. 4. En utilisant les données fournies en annexe, indiquer les espèces à considérer pour tracer le diagramme potentielpH pour un pH compris entre 0 et 11 (au-delà de pH = 11, l'atome N3 peut se déprotoner). Q. 5. Écrire les demi-équations électroniques des différents couples rédox possibles en considérant ces espèces, en indiquant le domaine de pH dans lequel elles sont à considérer. + Q. 6. Exprimer le potentiel rédox standard des couples /H, /H+ 2 , H/H2 et H2 /H2 en fonction des constantes thermodynamiques (potentiels rédox standards et pKa ) fournies. On donne les résultats numériques suivants : 0,06 × 8,6 = 0,516 ; 0,06 × 6,6 = 0,396 ; 0,06 × 2,3 = 0,138. Faire les applications numériques. Q. 7. Exprimer les équations des frontières du diagramme potentielpH pour les couples H+ 2 /H2 + et /H2 en fonction des données du problème. On considère qu'à la frontière la concentration des 2 espèces rédox en solution est égale. On donne dans la Figure 2 (page suivante) les diagrammes potentielpH obtenus pour la FMN. Dans les Figures 2a et 2b sont représentées les frontières pour les couples des formes quinone/semiquinone et semiquinone/hydroquinone. La Figure 2c correspond à la superposition de ces 2 diagrammes potentielpH. On considère qu'à la frontière entre 2 espèces rédox en solution leur concentration est égale. Q. 8. Attribuer, en justifiant, les figures (a) et (b) aux couples quinone/semiquinone et semiquinone/hydroquinone. Attribuer ensuite les différents domaines de prédominance aux espèces déterminées à la question 4 pour chacune des figures. Q. 9. En déduire qu'en solution la forme semiquinone de FMN n'est stable thermodynamiquement qu'à pH acide. Exprimer le pH limite en-dessous duquel la forme semiquinone de FMN peut être majoritaire. Déterminer (en indiquant votre raisonnement) graphiquement sa valeur (à 0,1 près en unité de pH). Vérifier cette valeur en faisant l'application numérique. On donne pour cela le résultat numérique suivants : 0,161 / 0,12 = 1,34. Q. 10. Écrire l'équilibre de dismutation de la forme semiquinone de la FMN à pH = 6, en considérant les espèces acido-basiques les plus stables à ce pH. On note Kdis la constante de cet équilibre. Exprimer log(Kdis ) en fonction des données du problème. Q. 11. Quel est ainsi le couple rédox à plutôt considérer pour la FMN en solution aqueuse à pH = 6 ? Écrire la demi-équation rédox correspondante. On donne les résultats numériques 2 (a) (b) (c) Figure 2: Diagrammes potentielpH de la FMN. suivants : 0,06 × 8,6 = 0,516 ; 0,06 × 6,6 = 0,396. Que vaut le potentiel rédox standard de ce couple ? 1.2 Dosage des flavines dans les flavoprotéines En solution, les flavines sont des composés colorés dans leurs formes quinone (jaunes) et semiquinone (rouges dans leur forme anionique, ou bleues à l'état neutre). Par ailleurs, elles présentent dans ces 2 mêmes états rédox des propriétés de fluorescence. Les flavoprotéines sont des protéines qui se lient à des flavines de façon non covalente. En notant P la protéine et la flavine, la réaction de complexation peut s'écrire de façon générale, de constante d'équilibre Kf : P + n Pn Lorsque les flavines se lient à une flavoprotéine, leurs spectres d'absorption et de fluorescence sont modifiés (intensité et/ou longueurs d'ondes d'absorption ou de fluorescence). Nous allons voir dans cette section comment il est possible de tirer parti de ces propriétés pour déterminer la stoechiométrie du complexe flavine/protéine Pn et sa constante de formation Kf . Dosage utilisant la fluorescence On donne ci-dessous le protocole de dosage de la riboflavine en interaction avec une flavoprotéine du blanc d'oeuf, adapté de Nishikimi et Kyogoku, Journal of Biochemistry, 1973, 73, 12331242 : 3 On dispose d'une solution contenant la flavoprotéine du blanc d'oeuf à une concentration de 520 nmol.L1 . On ajoute à cette solution une quantité croissante de riboflavine. On mesure à chaque ajout la fluorescence de la solution à 520 nm (longueur d'onde d'excitation : 370 nm). On réalise la même expérience en parallèle mais en ajoutant cette fois la riboflavine à une solution tampon non fluorescente de phosphate de sodium à 0,1 mol.L1 . Dans les 2 cas, on peut négliger la dilution due à l'ajout de riboflavine. La Figure 3 présente les courbes d'intensité de fluorescence (normalisée) obtenue pour les 2 expériences. La courbe I est la mesure de l'intensité de fluorescence (normalisée) pour la solution de protéine et la courbe II la mesure pour la solution tampon. La quantité de riboflavine en abscisse a été convertie en concentration. Figure 3: Intensité de fluorescence lors de l'ajout de riboflavine à une solution de flavoprotéine du blanc d'oeuf (courbe I) ou à une solution tampon de phosphate de sodium (courbe II). Q. 12. En vous aidant des résultats expérimentaux présentés sur la Figure 3, donner la relation mathématique qui lie l'intensité de fluorescence et la concentration en espèce fluorescente. Q. 13. Au vu des résultats expérimentaux, indiquer quelles espèces sont fluorescentes parmi la protéine P, le complexe Pn et la riboflavine ? Q. 14. Définir la constante d'équilibre Kf de la réaction de formation du complexe Pn . On notera C 0 la concentration standard de référence, prise égale à 1 mol.L-1 . Q. 15. En faisant l'hypothèse que Kf 1, expliquer l'allure de la courbe I. Q. 16. Montrer que n = 1, en précisant votre raisonnement. On va maintenant montrer comment à partir des courbes I et II on peut obtenir la valeur de Kf . Dans la suite on note []0 la concentration correspondant à la quantité de flavine ajoutée. [P], [] et [P] sont les concentrations à l'équilibre de la protéine, de la flavine libre et du complexe flavine/protéine. Pour un ajout de flavine []0 , on note I l'intensité de fluorescence de la solution de protéine et I0 l'intensité de fluorescence de la solution tampon. 4 Q. 17. En notant le rapport entre la concentration de complexe à l'équilibre [P] et de protéine initiale [P]0 , montrer qu'on peut écrire : C0 = Kf (1 - ) [] Q. 18. Exprimer [] en fonction des intensités de fluorescence I et I0 , ainsi que de []0 . Q. 19. En utilisant la loi de conservation de la matière de la flavine, exprimer en fonction de I, I0 , [P]0 et []0 . Q. 20. Expliquer alors comment on peut obtenir Kf à partir de l'expérience réalisée. On donne dans la Figure 4 ci-dessous le résultat obtenu pour trois types de flavines : la riboflavine (I, ronds vides), la 3-méthylriboflavine (II, ronds pleins) et la lumiflavine (III, carrés vides). L'axe des ordonnées de gauche correspond aux données pour la riboflavine et la 3méthylriboflavine. L'axe des ordonnées de droite correspond aux données pour la lumiflavine. Figure 4: Représentation de C 0 /[] en fonction de (1 - ) pour 3 types de flavines. (I) ronds vides : riboflavine ; (II) ronds pleins : 3-méthylriboflavine ; (III) carrés vides : lumiflavine. La lecture des valeurs de C 0 /[] pour les courbes (I) et (II) se fait sur l'axe de gauche, tandis que celles pour la courbe (III) se fait sur l'axe de droite. Q. 21. Estimer à l'aide de ces courbes les valeurs des constantes de complexation pour les 3 types de flavines. Laquelle se lie le plus à la flavoprotéine de blanc d'oeuf ? Est-ce que l'hypothèse faite à la question 15 est vérifiée ? Dosage utilisant la spectrophotométrie Une autre méthode pour déterminer la constante d'équilibre est la méthode de BenesiHildebrand, qui a été développée initialement sur la base de données de spectrophotométrie UV-visible (une variante de cette méthode est également envisageable sur des données de fluorescence). Dans cette méthode, on fait l'hypothèse d'une stoechiométrie 1:1 pour le complexe entre la protéine et la flavine (on a donc le complexe P) dont l'équilibre de formation s'écrit alors : P + P On suppose par ailleurs qu'à une longueur d'onde bien choisie les espèces et P absorbent, avec des coefficients d'absorption et P , mais que la protéine P n'absorbe pas. Enfin, on considère des mesures d'absorbance pour des solutions contenant : 5 · un mélange de protéine et de flavine de concentrations totales en protéine et flavine égales respectivement à [P]0 et []0 , dans des conditions de large excès de protéine. · uniquement de la flavine en concentration []0 . On notera A et A0 , respectivement, les absorbances de ces deux solutions, mesurées dans une cuve de chemin optique l. Q. 22. Dans les conditions expérimentales indiquées ici, exprimer [P] en fonction de []0 , [P]0 , C 0 et Kf . Q. 23. Exprimer alors A en fonction de []0 , [P]0 , C 0 , Kf , l, et P . Q. 24. En déduire l'expression suivante : A = A - A0 = A × Kf [P]0 0 C + Kf [P]0 On donnera l'expression de A et on en proposera une interprétation physique. Q. 25. Proposer un protocole permettant de déterminer la valeur de Kf (mesures expérimentales à effectuer et traitement des mesures collectées). 1.3 Structure électronique des flavines et réactivité On donne ci-dessous la représentation schématique de 4 orbitales moléculaires de la lumiflavine (R = CH3 ), prise comme modèle de flavine, et calculées par un logiciel de chimie quantique dans la forme hydroquinone totalement réduite H- , en supposant une géométrie plane de la molécule. Il s'agit des 2 OM les plus hautes occupées et des 2 plus basses vacantes, données dans la Figure 5. OMa OMb OMc OMd Figure 5: Représentation des 2 OM les plus hautes occupées et des 2 OM les plus basses vacantes de la lumiflavine dans sa forme H- . Les coefficients des orbitales atomiques 2pz impliquées significativement dans ces OM sont indiqués. Q. 26. Identifier le type ( ou ) de ces orbitales moléculaires. Q. 27. Justifier l'ordre énergétique suivant de ces orbitales : E(OMa ) < E(OMb ) < E(OMc ) < E(OMd ). En déduire les orbitales frontières HO et BV. 6 On donne les valeurs suivantes pour les longueurs de liaison C4a N5 et C4a C4 (selon la numérotation des atomes donnée dans la Figure 1) dans les formes réduite H- et semi-réduite H de la lumiflavine, obtenues par un calcul de chimie théorique : Forme de la lumiflavine H- H distance C4a N5 1,43 Å 1,36 Å distance C4a C4 1,45 Å 1,49 Å Q. 28. En utilisant les représentations des OM de H- fournies, justifier qualitativement l'évolution de ces longueurs de liaison entre les formes H- et H. Les mono-oxygénases sont des protéines qui permettent de catalyser l'oxydation de substrats organiques par addition d'un groupement hydroxyle, dont l'atome d'oxygène provient d'une molécule de dioxygène. Parmi ces protéines, certaines (notées par la suite FMO pour flavin monooxygenase) possèdent en leur sein un cofacteur flavine qui réagit intermédiairement avec la molécule de dioxygène pour former l'intermédiaire HOOH. La réaction se déroule en 3 étapes élémentaires : · Étape 1 : réaction d'oxydoréduction entre O2 et H- O2 + H- O- 2 + H · Étape 2 : addition de l'anion superoxyde sur H - O- 2 + H [HOO] · Étape 3 : protonation de [HOO]- [HOO]- + H+ HOOH Le diagramme d'orbitales moléculaires de la molécule de dioxygène est donné en annexe. Q. 29. Rappeler les 3 règles de remplissage d'un diagramme d'OM. Q. 30. Donner la configuration électronique fondamentale de O2 et de O- 2 . Justifier qu'on sym·- bolise parfois l'anion superoxyde par la notation O2 . On s'intéresse à l'étape 2 d'addition de O- 2 sur H, qu'on étudiera dans le cadre du modèle des orbitales frontières. On admettra que dans le cas de réaction entre deux radicaux, l'interaction orbitalaire à considérer est celle entre les orbitales moléculaires des réactifs à moitié remplies. Q. 31. Quelle est l'orbitale moléculaire de H impliquée (parmi OMa , OMb , OMc , et OMd présentées précédemment) ? Sachant que l'addition de O- 2 se fait sur un atome de carbone du cycle central, donner la formule topologique de HOOH attendue. Q. 32. Justifier que la molécule de O- 2 doit approcher en dehors du plan pour que la réaction soit efficace. Faisons l'hypothèse qu'on puisse stabiliser la flavine sous la forme radicalaire H et la faire réagir avec le radical NO au lieu de l'anion superoxyde O- 2 . On donne dans le tableau ci-dessous - les énergies (en eV) des OM de NO et de O2 . 7 OM O- 2 NO 1 l 37,91 35,78 2 al 25,52 21,88 3 l 16,34 16,10 1xl et 1yl 15,59 14,60 2xal et 2yal 4 al 12,67 11,05 8,96 26,71 Q. 33. Justifier qualitativement l'évolution énergétique des OM entre O- 2 et NO. Q. 34. En supposant une réactivité de H avec NO similaire à celle entre H et O- 2 , qu'obtiendraiton comme produit d'addition : HNO (addition par l'atome d'azote) ou HON (addition par l'atome d'oxygène) ? Détailler toutes les étapes du raisonnement. On ne demande pas de dessiner la formule topologique de la molécule obtenue. Q. 35. Sachant que l'énergie de l'orbitale réactive de H vaut -10,69 eV, pourrait-on prévoir une réaction moins ou plus rapide avec NO qu'avec O- 2 ? 1.4 Mécanisme catalytique d'une FMO FbSI est une monooxygénase flavine-dépendante qui s'associe de manière non-covalente à une molécule de flavine et qui catalyse l'hydroxylation d'amines primaires telles que la putrescine (1,4-diaminobutane) ou la cadavérine (1,5-diaminopentane) selon la réaction globale présentée sur la Figure 6 ci-dessous dans l'exemple de la putrescine : Figure 6: Réaction globale d'hydroxylation de la putrescine catalysée par la FbsI. Le NADPH est un cofacteur rédox (couple NADPH/NADP+ ) qui va dans un premier temps réduire la flavine contenue dans FbSI de sa forme totalement oxydée à sa forme totalement réduite H- . H- va ensuite réagir avec O2 pour donner [HOO]- qui se protone pour donner HOOH (voir partie précédente). Le proton impliqué dans la dernière réaction provient d'un acide aminé de la protéine situé à proximité de la flavine, ce qui rend cette réaction de protonation quasi-instantanée. En présence de putrescine, celle-ci est hydroxylée pour donner la N-hydroxyputrescine et une hydroxyflavine HOH. Le cycle catalytique se termine par la dégradation de HOH pour donner une molécule d'eau et redonner la flavine oxydée . Q. 36. Écrire les équations-bilan de l'ensemble des réactions impliquées dans le cycle catalytique ainsi que le bilan global (l'enzyme FbSI sera représentée dans ces équations uniquement au travers du cofacteur flavine ). Étude de la vitesse globale de la réaction Dans un premier temps, on s'intéresse à la vitesse globale de la réaction, définie par la vitesse de formation du produit. On réalise des mesures de la vitesse de la réaction dans une série d'expériences dont les conditions expérimentales sont résumées ci-dessous : [NADPH] (mol.L-1 ) [diamine] (mol.L-1 ) [FbSI] (mol.L-1 ) 0,5 10-3 10-5 à 500 10-6 10-6 8 On précise par ailleurs que la solubilité du dioxygène dans l'eau vaut environ 8 mg.L-1 dans les conditions expérimentales utilisées et que la solution est saturée en dioxygène. Q. 37. Quelle est la concentration molaire du dioxygène en solution dans les conditions expérimentales ? Q. 38. Justifier qu'on puisse considérer la réaction dans le cadre d'un mécanisme catalytique de type MichaelisMenten impliquant l'enzyme FbSI, notée par la suite E, avec pour seul substrat la diamine notée S. Le mécanisme catalytique de type MichaelisMenten est le suivant : k1 k 2 E+S- - - - ES -- E + P k-1 La loi de vitesse de MichaelisMenten donne la vitesse initiale de formation du produit P en fonction de deux paramètres vmax et KM et de la concentration initiale en substrat [S]0 : v0 = vmax [S]0 KM + [S]0 Elle est obtenue à l'aide des hypothèses suivantes : · Le substrat est en excès par rapport à l'enzyme. · On peut appliquer l'approximation de l'état quasi-stationnaire (AEQS) au complexe enzyme-substrat ES. Q. 39. En appliquant l'AEQS à ES et en utilisant la conservation de matière de l'enzyme, exprimer [ES] en fonction de [E]0 , [S] et des constantes de vitesse des actes élémentaires (k-1 , k1 et k2 ). Q. 40. Retrouver la formule de MichaelisMenten en donnant l'expression de vmax et de KM en fonction des constantes de vitesse des actes élémentaires (k-1 , k1 et k2 ) et de [E]0 . Lorsque le substrat est en large excès, il peut arriver que deux molécules de substrat se lient à la protéine, formant une espèce ESS, inhibant alors l'activité catalytique de l'enzyme (on parle d'inhibition par le substrat). On note Ki la constante de dissociation du complexe ESS formé à partir de ES et S et on suppose que cet équilibre est établi instantanément. Q. 41. Écrire l'équilibre de dissociation de ESS et définir Ki . Par souci de simplification, on ne fera pas apparaître la concentration standard C 0 dans l'expression de Ki . Q. 42. Déterminer la vitesse initiale de formation du produit dans ce cas d'inhibition par le substrat en fonction de vmax , KM , [S]0 et Ki . On donne dans la Figure 7 le résultat de la série d'expériences en utilisant comme substrat soit la putrescine, soit la cadavérine. Q. 43. En utilisant un raisonnement qualitatif de comportement aux limites des expressions de v0 dans le cas d'un mécanisme avec ou sans inhibition par le substrat, indiquer pour lequel des deux substrats on a une inhibition par le substrat. 9 Figure 7: Vitesse initiale de formation de la réaction d'hydroxylation du substrat par FbSI en fonction de la concentration en substrat pour la putrescine (points noirs) et pour la cadavérine (carrés bleus). Étude des étapes de réoxydation de la flavine dans une FMO On s'intéresse maintenant spécifiquement aux étapes de réoxydation de la flavine H- par le dioxygène. Pour cela, on peut réaliser des expériences en l'absence de substrat. Dans ce cas, le produit d'addition de O2 sur (HOOH) se dégrade pour donner du peroxyde d'hydrogène et redonner la flavine oxydée . On souhaite plus précisément suivre les 2 étapes suivantes : · Étape A. Formation de HOOH : O2 + H- + H+ HOOH · Étape B. Dégradation de HOOH : HOOH + H2 O2 On réalise pour cela des mesures de cinétique dites « stopped-flow » qui permettent de suivre des cinétiques de réaction rapides. L'instant t = 0 correspond au mélange très rapide d'une quantité égale de solution de FMO avec la flavine préalablement réduite H- de concentration 40 10-6 mol.L-1 et d'une solution contenant une concentration en dioxygène comprise entre 130 10-6 et 1030 10-6 mol.L-1 . La méthode de détection suivie est l'absorption UV-visible. On donne dans la Figure 8a les spectres d'absorption typiques de H- (ligne pointillée), HOOH (cercles noirs) et (ligne continue) dans une flavoprotéine et dans la Figure 8b le suivi de l'absorbance à 370 et 450 nm. Figure 8: (a) Spectres d'absorption des espèces H- (ligne pointillée), HOOH (cercles noirs) et (ligne continue) dans une flavoprotéine. (b) Évolution de l'absorbance pour 4 concentrations en dioxygène différentes. Les courbes avec une absorbance initiale aux alentours de 0,07 (axe des ordonnées de gauche) correspondent à l'absorbance à 370 nm et les courbes démarrant autour de 0,05 (axe des ordonnées de gauche) correspondent à l'absorbance à 450 nm. 10 Q. 44. Justifier le choix des longueurs d'onde utilisées pour suivre la réaction. Q. 45. Commenter l'évolution de l'absorption à 370 nm et à 450 nm en fonction du temps, en vous servant des spectres présentés sur la Figure 8a. Au vu des données expérimentales, on peut considérer que les étapes A et B sont bien dissociées dans le temps : toute la flavine H- est consommée pour donner HOOH avant que celui-ci ne se dégrade. On s'intéresse ici uniquement à l'étape A de formation de HOOH à partir de H- . Celle-ci se décompose en réalité en 3 actes élémentaires (voir partie précédente). En considérant que l'étape de protonation finale est quasi-instantanée, la loi cinétique régissant la disparition de H- peut-être modélisée par une loi cinétique de pseudo-ordre 1 par rapport à la concentration en flavine réduite [H- ], de constante de vitesse kobs . Q. 46. Dans cette hypothèse, quelle est la loi attendue suivie par l'absorbance A de la solution à 370 nm, en supposant que seules les espèces H- et HOOH absorbent à cette longueur d'onde. On notera A0 l'absorbance initiale et A l'absorbance finale (à la fin de l'étape A et avant le début de l'étape B). On souhaite modéliser les données expérimentales par l'équation : A = D + E × 1 - e-kobs t où D, E, et kobs sont des paramètres inconnus à optimiser pour reproduire au mieux les données expérimentales. L'optimisation de ces paramètres se fait à l'aide d'un code python en utilisant la fonction curve_fit de la librairie scipy.optimize. On donne dans la Figure 9a ci-dessous le code utilisé avec une partie à compléter, de façon à obtenir la Figure 9b. (a) (b) Figure 9: Script python (a) permettant de modéliser les résultats expérimentaux par l'équation -k t obs A=D+E× 1-e pour tracer la figure (b). 11 Q. 47. Compléter le code ci-dessus en écrivant une série d'instructions permettant de tracer les données expérimentales avec des symboles ainsi que la courbe modèle avec une ligne continue, pour un temps t variant de 0 à 1000 s, de façon à obtenir la Figure 9b. On donne en annexe un exemple d'utilisation de la librairie matplotlib pour tracer une fonction. On donne ci-dessous les valeurs obtenues pour kobs pour 4 concentrations différentes en dioxygène : [O2 ] (mmol.L-1 ) kobs (s-1 ) 0,15 2,00 0,30 3,99 0,60 8,02 0,90 11,98 Q. 48. En déduire la valeur approchée de la constante de vitesse bimoléculaire de la réaction de formation de HOOH. Dans certains cas, on peut obtenir des courbes qui présentent un caractère biexponentiel. Ceci peut provenir de la coexistence de 2 conformations différentes de la protéine qui impactent la cinétique de la réoxydation. On cherche alors à modéliser les courbes d'absorbance par l'équation : A = a0 + a1 1 - e-kobs,1 t + a2 1 - e-kobs,2 t où A est l'absorbance, a1 et a2 les amplitudes de variation de l'absorbance dans les deux phases, kobs,1 et kobs,2 les constantes de vitesse observées de ces deux phases et a0 la valeur initiale de l'absorbance. Q. 49. Modifier la fonction funtofit du programme précédent pour correspondre à une fonction biexponentielle. Q. 50. Comment peut-on modifier les lignes 18 et 19 du code de la Figure 9a pour récupérer et afficher les valeurs des deux constantes de vitesse kobs,1 et kobs,2 ? 12 2 Deuxième partie : Synthèse de l'alliacol A Cette partie représente environ 35% du total des points. Le (+)-alliacol A (1), un sesquiterpène polycyclique, a été isolé en 1977 à partir du champignon Marasmius Alliaceus. Ce composé présente des propriétés cytotoxiques à faible concentration. En raison du faible rendement obtenu par extraction et de sa structure originale, cette molécule a suscité un intérêt particulier en synthèse totale et diverses approches synthétiques ont été développées. Nous nous pencherons sur une voie de synthèse assez originale, impliquant une étape clé de cyclisation électrochimique du composé (2). Figure 10: Structure du (+)-alliacol A et approche rétrosynthétique. 2.1 La structure de l'Alliacol A Q. 51. Identifier tous les centres stéréogènes de cette molécule et indiquer le nombre maximal de stéréoisomères possibles. Q. 52. Donner le descripteur stéréochimique du ou des centre(s) stéréogène(s) quaternaire(s) en nommant la règle utilisée. 2.2 Synthèse du dérivé furanique (2) Figure 11: Schéma de la synthèse du dérivé furanique (2). Q. 53. En utilisant la nomenclature IUPAC, donner le nom chimique du composé (3). Q. 54. Sachant que c'est la forme énol du composé (3) qui réagit avec le dibrome, proposer un mécanisme pour la première étape (3) (4). Q. 55. Quel autre produit est formé au cours de cette réaction ? Q. 56. Discuter de l'importance de contrôler la température du milieu réactionnel. 13 Q. 57. Dans la réaction (4) (5), l'imidazole permet à la fois d'activer le chlorosilane de départ (TBSCl) et de servir de base pour déprotoner l'alcool. Justifier le site préférentiel de protonation de l'imidazole et proposer un mode d'activation du TBSCl par l'imidazole. Q. 58. Donner la structure de Lewis de la triéthylphosphite, P(OEt)3 , et en déduire le caractère électrophile ou nucléophile de cette espèce. La réaction (5) (8) met en jeu un mécanisme comprenant deux étapes élémentaires. À l'issue de la première étape un intermédiaire réactionnel transitoire (6) est généré et, lors de la seconde étape, la formation du -céto-phosphonate (8) s'accompagne de la génération d'un deuxième produit (7) qui est un composé chimique volatil de formule brute C2 H5 Br. Q. 59. Proposer une structure du composé (6) sachant qu'il s'agit d'une espèce ionique dans laquelle le degré d'oxydation de l'atome de phosphore est égal à (+V). Q. 60. Proposer un mécanisme pour la transformation (5) (8). Pourquoi la volatilité du produit (7) s'avère-t-elle bénéfique à cette réaction ? Q. 61. Soit la description suivante du spectre RMN 1 H du composé (10). Identifier les groupes de protons magnétiquement équivalents sur cette molécule et attribuer chacun des signaux observés. 1 H NMR (250 MHz, Chloroform-d) : = 7,35 7,27 (m, 1H) ; 7,25 7,17 (m, 1H) ; 6,74 (dt, J = 14,7, 5,3 Hz, 1H) ; 6,30 6,21 (m, 1H) ; 6,14 (d, J = 14, 7 Hz, 1H) ; 3,79 (s, 2H) ; 2,65 (t, J = 7, 4 Hz, 2H) ; 2,56 2,40 (m, 2H) ; 1,18 (s, 6H) ; 0,90 (s, 9H) ; 0,12 (s, 6H) Q. 62. Comment expliquer la différence entre le déplacement chimique des groupements méthyles à coté du motif cétone et celui des groupements méthyles portés par le silicium ? Q. 63. L'addition du diméthylcuprate Me2 Cu(CN)Li sur l'énone (10) s'effectue régiosélectivement pour conduire au composé (2). Cette réaction d'addition s'effectue-t-elle sous contrôle orbitalaire ou sous contrôle de charge ? Justifier votre réponse. 2.3 Cyclisation électrochimique L'étape clé de cette synthèse implique l'électrolyse du composé (2) dans une cellule indivisée avec une anode en carbone vitreux réticulé (RVC) et une cathode en carbone graphite (Cg) dans les conditions réactionnelles décrites ci-dessous : Figure 12: Conditions réactionnelles de l'électrolyse du composé (2). Q. 64. En recopiant le schéma simplifié de la cellule indivisée ci-dessus, identifier l'anode et la cathode et le sens du courant. Quel est le rôle du perchlorate de lithium dans cette réaction ? 14 Dans cette réaction électrochimique, le composé (2) cède deux de ses électrons à l'une des deux électrodes pour conduire au composé bicyclique (11). Q. 65. À quelle électrode (RVC ou Cg) s'effectue la réaction désirée ? Donner la demi-équation électronique de cette réaction rédox. Q. 66. La formation de bulles de gaz est constatée à l'électrode opposée. Quelle réaction redox pourrait se produire à cet endroit ? Q. 67. Estimer le rendement faradique de cette cyclisation électrochimique en précisant le mode de calcul. 2.4 Fin de la synthèse Figure 13: Schéma de la fin de la synthèse de (1). Q. 68. En vous inspirant du mécanisme d'hydrolyse d'un acétal, proposer un mécanisme permettant d'expliquer la formation de (12) à partir de (11). 15 Q. 69. Proposer des conditions réactionnelles pour promouvoir la transformation (12) (13). Q. 70. Lorsque de la triphénylphosphine (PPh3 ) est mise en présence d'iode, cela conduit à la formation de [IPPh3 ]+ I- (iodure d'iodotriphénylphosphonium). À partir de cet intermédiaire, proposer un mécanisme permettant la transformation de l'alcool (13) en le dérivé iodé (14) sachant que l'imidazole sert de base et que de l'oxyde de triphenylphosphine (O=PPh3 ) est également généré au cours de cette réaction. Q. 71. Lors de la transformation (14) (15), un précipité blanc photosensible de faible constante de solubilité est formé. Identifier ce précipité et en déduire le rôle du nitrate d'argent dans cette réaction Q. 72. En raisonnant à partir de la structure du composé (17), proposer une structure pour le composé (16). Q. 73. Proposer un mécanisme pour la transformation (17) (18). Q. 74. En s'inspirant du mécanisme d'estérification entre un alcool et un chlorure d'acyle, proposer un mécanisme pour la réaction (18) (19). Q. 75. Expliquer le contrôle total de régiosélectivité dans cette réaction. Q. 76. Proposer un ou plusieurs réactif(s) pour promouvoir la transformation (19) (20). Q. 77. Proposer un ou plusieurs réactif(s) pour promouvoir la transformation (20) (21). Soit le cycle catalytique suivant pour la transformation (21) (22) : Figure 14: Cycle catalytique pour la transformation (21) (22). Q. 78. De quel type de réaction s'agit-il ? Identifier le pré-catalyseur et le catalyseur. Q. 79. Donner le degré d'oxydation du métal dans RuCl3 , les espèces « A », « C » et « D ». Q. 80. À quoi correspond « B » ? Q. 81. Proposer des flèches de mécanisme pour expliquer le passage de « C » à « D ». Q. 82. Donner l'équation bilan de la réaction « D » « A ». Q. 83. Proposer une structure pour le composé (23) et le mécanisme associé à sa formation. 16 Q. 84. Pour cette étape, combien d'équivalent de LiTMP est-il nécessaire d'utiliser ? Q. 85. Pour la transformation (23) (1), quel produit est intermédiairement formé après réaction de (23) avec l'iodure de méthyle. Pourquoi cette étape est-elle essentielle pour obtenir le composé (1) ? 17 Annexes Constantes fondamentales et données chimiques : · Constante d'Avogadro : NA = 6,02 × 1023 mol-1 · Constante de Boltzmann : kB = 1,38 × 10-23 m2 · kg · s-2 · K-1 · Constante des gaz parfaits : R = 8,314 J · mol-1 · K-1 · Charge élémentaire : e = 1,6 × 10-19 C · Constante de Planck : h = 6, 63 × 10-34 J · s · Célérité de la lumière dans le vide : c = 3, 00 × 108 m · s-1 · Constante de Faraday : F = 96 485 C · mol-1 Réacothèque : Réaction de HornerWadsworthEmmons : Réaction de protection / déprotection d'alcools : Données thermodynamiques relatives aux couples rédox et acidobasiques de la flavine mononucléotide (FMN) : Valeurs de pKa : Potentiels rédox standard E 0 (en mV) : pKa (H2 / H- ) = 6,6 E10 = E 0 (H/H- ) = -172 pKa (H- / 2- ) > 14 E20 = E 0 (/- ) = -333 pKa (H+ 2 / H) = 2,3 pKa (H / - ) = 8,6 + pKa (H2+ 2 / H ) < 0 pKa (H+ / ) = 2,8 On prendra : RT ln(10) = 0, 06 V à 298 K. F 18 Diagramme d'orbitales moléculaires de O2 : Dans le nom des OM, le caractère liant ou antiliant de l'OM est indiqué en exposant (« l » pour liant et « al » pour antiliant) Eléments de documentation sur la programmation python : Représentation de la courbe y(x) = sin(x) avec la librairie matplotlib 19 Table de valeurs de déplacements chimiques en RMN 1 H : Échelle de Pauling représentant l'électronégativité de quelques éléments du tableau périodique 20 Fin du sujet 21 7 6 5 4 3 2 1 87 55 37 19 11 3 1 masse 223 88 56 38 20 12 4 Symbole Z Fr Cs 132.91 Rb 85.468 K 39.098 Na 22.990 Li 6.941 H 1.0079 1 IA Ra Ba 226 137.33 Sr 87.62 Ca 40.078 Mg 24.305 Be 9.0122 2 IIA 44.956 57-71 Y 88.906 Sc Ac-Lr 89-103 La-Lu 39 21 3 IIIA 89 57 104 72 40 22 261 Ac La 227 138.91 Rf Hf 178.49 Zr 91.224 Ti 47.867 4 IVB 90 58 105 73 41 23 262 Th 232.04 Ce 140.12 Db Ta 180.95 Nb 92.906 V 50.942 5 VB 91 59 106 74 42 24 266 Pa 231.04 Pr 140.91 Sg W 183.84 Mo 95.94 Cr 51.996 6 VIB 92 60 264 U 238.03 Nd 144.24 Bh Re 186.21 Tc 96 54.938 Mn 107 75 43 25 7 VIIB 93 61 55.845 Hs Os Np 237 145 277 190.23 Ru 101.07 Fe Pm 108 76 44 26 8 VIIIB 94 62 109 77 45 27 268 Pu Sm 244 150.36 Mt Ir 192.22 Rh 102.91 Co 58.933 9 VIIIB 95 63 58.693 281 Eu 243 151.96 Ds Pt 195.08 Pd 106.42 Ni Am 110 78 46 28 10 VIIIB 96 64 280 Cm Gd 247 157.25 Rg Au 196.97 Ag 107.87 Cu 63.546 11 IB 111 79 47 29 Classification periodique des elements 97 65 112 80 48 30 285 Bk Tb 247 158.93 Cn Hg 200.59 Cd 112.41 Zn 65.39 12 IIB 98 66 113 81 49 31 13 5 284 Cf Dy 251 162.50 Nh Tl 204.38 In 114.82 Ga 69.723 Al 26.982 B 10.811 13 IIIA 99 67 114 82 50 32 14 6 289 Es Ho 252 164.93 Fl Pb 207.2 Sn 118.71 Ge 72.64 Si 28.086 C 12.011 14 IVA 100 68 115 83 51 33 15 7 288 Fm Er 257 167.26 Mc Bi 208.98 Sb 121.76 As 74.922 P 30.974 N 14.007 15 VA 15.999 78.96 293 209 Md 258 168.93 Lv Po Te 127.6 Se S 32.065 O Tm 101 69 116 84 52 34 16 8 16 VIA 102 70 117 85 53 35 17 9 292 No Yb 259 173.04 Ts 210 126.9 At I Br 79.904 Cl 35.453 F 18.998 17 VIIA 103 71 118 86 54 36 18 10 2 83.8 294 222 Lr Lu 262 174.97 Og Rn Xe 131.29 Kr Ar 39.948 Ne 20.180 He 4.0025 18 VIIIA
