CCINP Chimie PC 2025
| Thème de l'épreuve | L'acétaldéhyde. Autour du phosphore. |
| Principaux outils utilisés | cristallographie, solutions aqueuses, cinétique chimique, oxydoréduction, courbes courant-potentiel, thermodynamique, chimie organique, procédés industriels continus |
| Mots clefs | paraldéhyde, pentaérythritol, cannizzaro, crotonaldéhyde, acide phosphorique, phosphates |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - -
Énoncé complet
(télécharger le PDF)














Rapport du jury
(télécharger le PDF)





Énoncé obtenu par reconnaissance optique des caractères
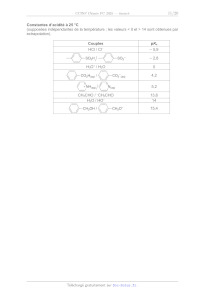
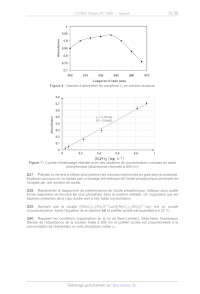
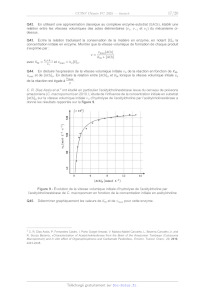
SESSION 2025 PC3C ÉPREUVE SPÉCIFIQUE - FILIÈRE PC ____________________ CHIMIE Durée : 4 heures ____________________ N.B. : le candidat attachera la plus grande importance à la clarté, à la précision et à la concision de la rédaction. Si un candidat est amené à repérer ce qui peut lui sembler être une erreur d'énoncé, il le signalera sur sa copie et devra poursuivre sa composition en expliquant les raisons des initiatives qu'il a été amené à prendre. RAPPEL DES CONSIGNES · · · Utiliser uniquement un stylo noir ou bleu foncé non effaçable pour la rédaction de votre composition ; d'autres couleurs, excepté le vert, bleu clair ou turquoise, peuvent être utilisées, mais exclusivement pour les schémas et la mise en évidence des résultats. Ne pas utiliser de correcteur. Écrire le mot FIN à la fin de votre composition. ______________________________________________________________________________ Les calculatrices sont interdites. Le sujet est composé de deux problèmes indépendants. Chaque problème est constitué de parties indépendantes. Des données sont disponibles à la fin de chaque problème. Des aides de calcul au problème 2 sont disponibles à la fin de ce problème. Toute réponse devra être clairement justifiée. 1/20 PROBLÈME 1 L'acétaldéhyde L'acétaldéhyde est un liquide incolore et volatil qui se trouve à faibles doses dans les fleurs et feuilles de nombreuses plantes et dans les fruits mûrs. Il est entre autres utilisé comme intermédiaire en synthèse organique dans la fabrication de colorants, de caoutchoucs, de parfums, de cosmétiques ainsi que dans l'industrie alimentaire. Ce problème s'intéresse à l'acétaldéhyde et à quelques-uns de ses dérivés synthétiques (figure 1) : Figure 1 - L'acétaldéhyde et quelques-uns de ses dérivés Les parties de ce problème sont indépendantes et le candidat est libre de les traiter dans l'ordre qu'il souhaite. Pour l'écriture des mécanismes, chaque fois qu'il le juge nécessaire, le candidat pourra utiliser des notations simplifiées des molécules lui permettant de se concentrer uniquement sur les groupes caractéristiques concernés. Partie I - L'acétaldéhyde De nos jours, l'acétaldéhyde produit annuellement dans le monde provient pour plus de 20 % du procédé Hoechst-Wacker (figure 2), à savoir la synthèse de l'aldehyde à partir de l'éthylène : Figure 2 - Description simplifiée du cycle catalytique du procédé Hoechst-Wacker Q1. Donner le nom de l'acétaldéhyde en nomenclature officielle. Identifier l'espèce catalytique du procédé Hoechst-Wacker. Identifier l'étape d'élimination réductrice et préciser le rôle du dichlorure de cuivre (CuCl2). Donner le bilan de la formation de l'acétaldéhyde par ce procédé. 2/20 À 25 °C, la constante thermodynamique de l'équilibre tautomérique entre l'acétaldéhyde et sa forme énol, l'éthénol, est égale à 3,9·108. La formation de l'éthénol à partir de l'acétaldéhyde selon un processus unimoléculaire, via une migration-1,3 d'hydrogène, présente une barrière d'activation trop élevée pour se produire à 25 °C. Des études cinétiques ont cependant montré que des traces d'acides catalysent efficacement la transformation en éthénol (schéma 1). Schéma 1 - Équilibre tautomérique céto-énolique de l'acétaldéhyde Q2. Calculer la valeur de l'enthalpie standard rH° de cet équilibre à l'aide des données des enthalpies standard de dissociation de liaison. Proposer un mécanisme pour la formation de l'éthénol à partir de l'acétaldéhyde en présence d'une quantité catalytique de chlorure d'hydrogène (HCl). Une autre voie d'obtention de l'acétaldehyde est l'utilisation du polytéréphtalate d'éthylène (PET) qui est un polymère de la famille des polyesters. C'est le polymère le plus utilisé pour la fabrication de bouteilles en plastique destinées à contenir des eaux gazeuses. Sa photo-oxydation conduit à la formation de l'ester vinylique 1 qui s'hydrolyse en acétaldéhyde au contact d'une eau acide (schéma 2) : Schéma 2 - Séquence réactionnelle de la dégradation du polytéréphtalate d'éthylène en acétaldéhyde Q3. Proposer un mécanisme rendant compte de la formation de l'acétaldéhyde par hydrolyse de l'ester vinylique 1 au contact d'une eau gazeuse de pH 5,5. Représenter l'autre composé formé. En fait, en solution aqueuse acide, les aldéhydes s'hydratent en diols géminés. L'étude cinétique des équilibres d'hydratation de l'acétaldéhyde et du formaldéhyde à 25 °C dans une solution tamponnée de pH 4,5 ont permis de déterminer les constantes de vitesse données au schéma 3 (Source : A. R. Rendina, J. D. Hermes , W. W. Cleland, Biochemistry, 1984, 23, 5148) : Schéma 3 - Équilibres d'hydratation de l'acétaldéhyde et du formaldéhyde 3/20 Q4. Proposer un mécanisme rendant compte de la formation de l'éthane-1,1-diol à partir de l'acétaldéhyde en milieu acide aqueux. Proposer une explication au fait d'avoir une constante de vitesse k2 plus grande que la constante de vitesse k1. Partie II - Le paraldéhyde Le paraldéhyde est un somnifère et sédatif efficace. Utilisé autrefois pour endormir les patients en hôpital psychiatrique et en gériatrie, il reste de nos jours employé dans le traitement de l'épilepsie. Le paraldéhyde est obtenu par condensation de l'acétaldéhyde en présence d'une quantité catalytique d'acide sulfurique (H2SO4) à 25 °C via l'intermédiaire 2 (schéma 4) : Schéma 4 - Séquence réactionnelle de la synthèse du paraldéhyde à partir de l'acétaldéhyde Q5. Indiquer le nombre de molécules d'acétaldéhyde qui sont incorporées dans une molécule de paraldéhyde. Proposer un mécanisme rendant compte de la formation du paraldéhyde à partir de l'acétaldéhyde en présence d'acide. Q6. Représenter tous les stéréoisomères de configuration du paraldéhyde. Indiquer si ces stéréoisomères sont chiraux et préciser la (les) relation(s) de stéréoisomérie qui les lie(nt). Partie III - Le pentaérythritol et ses dérivés Le pentaérythritol est un intermédiaire dans la synthèse d'explosifs, de plastiques, de peintures et de cosmétiques. Il peut être obtenu par réaction de l'acétaldéhyde avec le formaldéhyde en milieu alcalin aqueux (Source : H. B. J. Schurink, Organic Syntheses, 1925, 4, 53). La réaction procède via la formation successive des intermédiaires 3 et 4 et du pentaérythrose (schéma 5) : Schéma 5 - Synthèse du pentaérythritol à partir de l'acétaldéhyde 4/20 Q7. Représenter les deux formes limites de résonance de l'espèce chimique obtenue par réaction de l'acétaldéhyde avec l'ion hydroxyde (HO) et identifier la forme la plus contributive à la réalité. Proposer un mécanisme rendant compte de la formation de l'intermédiaire 3 en milieu basique aqueux. Nommer cette réaction. La dernière étape de la formation du pentaérythritol à partir de l'acétaldéhyde correspond à une réaction de Cannizzaro croisée entre le pentaérythrose et le formaldéhyde (schéma 6) : Schéma 6 - Réaction de Cannizzaro croisée entre le pentaérythrose et le formaldéhyde La réaction de Cannizzaro a été initialement décrite avec le benzaldéhyde. Des expériences menées avec DO ont mis en évidence un mécanisme comportant trois étapes élémentaires (schéma 7) : Schéma 7 - Réaction de Cannizzaro avec le benzaldéhyde (Ph = phényle = C6H5) Q8. Écrire l'équation de la réaction de Cannizzaro avec le benzaldéhyde. Expliquer pourquoi cette réaction est décrite comme une dismutation du benzaldéhyde. Q9. À l'aide du formalisme des flèches courbes, représenter les transferts électroniques mis en jeu dans la deuxième étape du mécanisme. Justifier par le calcul que la troisième étape élémentaire est quantitative. Q10. Identifier le composé 5 qui accompagne la formation du pentaérythritol lors de la réaction de Cannizzaro croisée entre le pentaérythrose et le formaldéhyde (schéma 6). Q11. Justifier pourquoi la formation du méthanol (CH3OH) est également observée au cours de la réaction. 5/20 Les dérivés du pentaérythritol ont de nombreuses applications dans l'industrie. Le tétraacrylate de pentaérythritol (PETA) est par exemple utilisé pour la production de polymères et de résines époxy, et le tétranitrate de pentaérythritol (PETN) est l'un des explosifs les plus puissants connus à l'heure actuelle (schéma 8) : Schéma 8 - Séquence réactionnelle de la synthèse du tétraacrylate de pentaérythritol et du tétranitrate de pentaérythritol Q12. Proposer un réactif 6 et des conditions opératoires permettant d'obtenir le tétraacrylate de pentaérythritol (PETA) avec un bon rendement à partir du pentaérythritol. La première étape de la synthèse du tétranitrate de pentaérythritol (PETN) conduit à la formation du composé 8 via l'intermédiaire [7] (schéma 9) : Schéma 9 - Séquence réactionnelle de la première étape de la synthèse du tétranitrate de pentaérythritol Q13. Écrire le schéma de Lewis de l'acide nitrique (HNO3). Proposer un mécanisme rendant compte de la formation du composé 8 à partir du pentaérythritol en présence d'acide nitrique (HNO3) pur. Le pentaérythritol est également utilisé pour la synthèse d'un relaxant musculaire, le loprodiol (2,2-bis(chlorométhyl)propane-1,3-diol). La synthèse de ce composé à partir du pentaérythritol nécessite quatre étapes qui sont décrites dans le schéma 10 (Source : H. Rapoport, Journal of the American Chemical Society, 1946, 68, 341) : Schéma 10 - Séquence réactionnelle de la synthèse du loprodiol à partir du pentaérythritol 6/20 Q14. Proposer un réactif 9 et des conditions pour la transformation du pentaérythritol en espèce chimique 10. Donner le nom du groupe fonctionnel créé. La réaction du composé 10 avec deux équivalents de chlorure de tosyle (TsCl) au reflux de la pyridine donne un intermédiaire [11] qui est instable dans les conditions opératoires et conduit spontanément au dérivé dichloré 12. Q15. Représenter l'intermédiaire [11] et expliquer l'utilité de sa formation. Proposer un mécanisme rendant compte de la transformation [11] 12. Proposer des conditions opératoires pour la transformation 12 loprodiol. Partie IV - Le crotonaldéhyde Le crotonaldéhyde est un intermédiaire très important en synthèse organique. Il est naturellement présent dans certains produits alimentaires tels que l'huile de soja. Il est produit industriellement en deux étapes (Source : R. P. Schulz, J. Blumenstein, C. Kohlpaintner, Crotonaldehyde and Crotonic Acid in Ullman's Encyclopedia of Industrial Chemistry, Weinheim : Wiley-VCH, 2011) : une étape d'aldolisation de l'acétaldéhyde sur lui-même en milieu basique, suivie d'une étape de crotonisation en milieu acide du 3-hydroxybutanal formé. La deuxième étape de la réaction a lieu sous contrôle thermodynamique et donne le crotonaldéhyde sous la forme d'un isomère très majoritaire (schéma 11) : Schéma 11 - Séquence réactionnelle de la synthèse industrielle du crotonaldéhyde à partir de l'acétaldéhyde Q16. Indiquer le nombre de stéréoisomères de configuration possibles du 3-hydroxybutanal. Préciser la (les) relations de stéréoisomérie qui les lie(nt). Représenter le (3R)-hydroxybutanal. Q17. Attribuer le descripteur stéréochimique E ou Z à la double liaison carbonecarbone de l'isomère majoritaire du crotonaldéhyde obtenu. Justifier pourquoi cet isomère est formé majoritairement sous contrôle thermodynamique. Le spectre de résonance magnétique nucléaire du proton (RMN 1H) du crotonaldéhyde pur réalisé à 60 MHz présente les signaux rapportés dans le tableau 1 (Source : D. E. MacGreer, B. D. Page, Canadian Journal of Chemistry, 1969, 47, 866) : Déplacements chimiques (ppm) 9,40 6,85 5,99 1,93 Intégrations Multiplicités 1H d 1H qd 1H qdd 3H dd d = doublet, q = quadruplet Constantes de couplage J (Hz) 3 J = 7,6 3 J = 15,4 et 6,7 3 J = 15,4 et 7,6 ; 4J = 1,5 3 J = 6,7 ; 4J = 1,5 Tableau 1 Données RMN 1H du crotonaldéhyde 7/20 Q18. Attribuer chacun des signaux à un ou des atome(s) d'hydrogène caractéristique(s). On utilisera la notation de la figure 3. Montrer que les constantes de couplage permettent de confirmer le descripteur stéréochimique E ou Z de l'isomère majoritaire du crotonaldéhyde. Figure 3 - Affectation des atomes d'hydrogène du crotonaldéhyde Le spectre infrarouge (IR) du crotonaldéhyde présente, entre autres, les bandes d'absorption rapportées dans le tableau 2 (Source : https://www.chemicalbook.com/SpectrumEN_4170-303_IR2.htm) : Nombres d'onde (cm1) 2 808 2 727 1 699 1 629 Intensités moyenne moyenne forte moyenne Tableau 2 Données IR du crotonaldéhyde Q19. Proposer une attribution pour ces bandes. Q20. Proposer un mécanisme réactionnel rendant compte de la formation du crotonaldéhyde à partir du 3-hydroxybutanal en présence d'une quantité catalytique d'acide éthanoïque. Identifier la force motrice de cette réaction. La crotonisation du 3-hydroxybutanal peut également être réalisée en milieu basique à chaud pour donner le même isomère majoritaire du crotonaldéhyde. Cette réaction est réalisée au laboratoire. Q21. Proposer un mécanisme réactionnel rendant compte de la formation du crotonaldéhyde à partir du 3-hydroxybutanal avec une solution aqueuse à 5 % de soude (NaOH). Le crotonaldéhyde est utilisé, entre autres, dans la synthèse du 3-méthoxybutanol, liquide à faible viscosité, utilisé comme solvant dans les revêtements et les peintures. La synthèse industrielle de ce composé comprend deux étapes décrites au schéma 12 (Source : R. P. Schulz, J. Blumenstein, C. Kohlpaintner, Crotonaldehyde and crotonic acid in Ullman's Encyclopedia of Industrial Chemistry, Weinheim : Wiley-VCH, 2011) : Schéma 12 - Séquence réactionnelle de la synthèse industrielle du 3-méthoxybutanol à partir du crotonaldéhyde Le crotonaldéhyde a une réactivité similaire à l'acroléine (CH2=CHCHO). Une représentation des orbitales moléculaires frontalières (OF1 à OF4) et une partie de la répartition des charges partielles de l'acroléine et de l'ion méthanolate (MeO) sont données à la figure 4 (Source : P. Chaquin et F. Fuster, OrbiMol, Sorbonne Université, CNRS, Laboratoire de Chimie Théorique, LCT, F-75005 Paris, France). 8/20 Q22. Identifier le(s) site(s) électrophile(s) de l'acroléine. Représenter le produit qui serait obtenu si la réaction avec le crotonaldéhyde était sous contrôle de charges. Q23. Identifier les deux orbitales frontalières (OF) de l'acroléine et de l'ion méthanolate (CH3O). Interpréter la formation du 3-méthoxybutanal à partir du crotonaldéhyde sous contrôle frontalier ou orbitalaire. Proposer un mécanisme rendant compte de la formation du 3-méthoxybutanal à partir du crotonaldéhyde et d'une solution de méthanolate de sodium (MeONa) dans le méthanol (MeOH). Donner le nom de la réaction mise en jeu. Figure 4 - Surface d'iso-densité des orbitales frontalières et charges partielles de l'acroléine et de l'ion méthanolate Q24. Proposer d'autres conditions opératoires qui permettraient d'obtenir le 3-méthoxybutanol à partir du 3-méthoxybutanal au laboratoire. Le crotonaldéhyde est également utilisé dans la synthèse de la pent-3-èn-2-one qui est un agent aromatisant (schéma 13) : Schéma 13 - Séquence réactionnelle de la synthèse de la pent-3-èn-2-one à partir du crotonaldéhyde Q25. Représenter l'intermédiaire 14 qui conduit à la pent-3-èn-2-one par oxydation. Proposer un réactif 13 et des conditions opératoires pour obtenir l'intermédiaire 14 à partir du crotonaldéhyde. 9/20 Données relatives au problème 1 Numéros atomiques Éléments Z H 1 C 6 N 7 CH 395 CO 460 O 8 Enthalpies standard de dissociation de liaison Liaisons Énergie (kJ·mol1) CC 360 OH 355 C=C 630 C=O 735 Sources : a) https://labs.chem.ucsb.edu/zakarian/armen/11---bonddissociationenergy.pdf. b) G. da Silva, C.-H. Kim, J. W. Bozzelli, Journal of Physical Chemistry A, 2006, 110, 7925. c) G. da Silva, J. W. Bozzelli, Journal of Physical Chemistry A, 2006, 110, 13058. Données RMN 1H Gamme de déplacements chimiques de quelques atomes d'hydrogène caractéristiques et valeurs typiques des constantes de couplage 3J des atomes d'hydrogène éthyléniques et 4J celles des atomes d'hydrogène allyliques. Atomes d'hydrogène C=CCH CHO C=CH CHO (aldéhyde) (ppm) 1,6 2,3 3,5 4,8 4,6 7,0 9,1 10,3 Structures J (Hz) 3 J = 12 18 3 J = 5 12 4 J=13 Source : E. Pretsch, W. Simon, J. Seibl, T. Clerc, W. Fresenius, J. F. K Hubert, E. Pungor, G. A. Rechnitz, W. Simon, Tables of Spectral Data for Structure Determination of Organic Compounds, 2nd Edition, 1989. Données infrarouge Gamme de nombre d'ondes de quelques liaisons caractéristiques. Liaisons O=CH C=O (aldéhyde) C=O (aldéhyde conjugué) C=C (alcène) C=C (alcène conjugué) (cm1) 2 695 2 830 1 720 1 740 1 660 1 705 1 645 1 675 1 620 1 650 Intensités moyenne (deux bandes) forte forte moyenne moyenne Source : E. Pretsch, W. Simon, J. Seibl, T. Clerc, W. Fresenius, J. F. K Hubert, E. Pungor, G. A. Rechnitz, W. Simon, Tables of Spectral Data for Structure Determination of Organic Compounds, 2nd Edition, 1989. 10/20 Constantes d'acidité à 25 °C (supposées indépendantes de la température ; les valeurs < 0 et > 14 sont obtenues par extrapolation). Couples pKa HCl / Cl 5,9 2,8 H3O+ / H2O 0 4,2 5,2 CH3CHO / CH2CHO H2O / HO 13,6 14 15,4 11/20 PROBLÈME 2 Autour du phosphore Le phosphore est un élément essentiel à la vie, principalement présent dans les organismes sous forme de phosphates (RO) PO . Les phosphates forment l'ossature de l'ADN et l'ARN, et interviennent dans l'adénosine triphosphate (ATP), molécule permettant la gestion de l'énergie au sein des cellules. Le phosphore est également un composant clé des membranes cellulaires ainsi que de l'émail dentaire. Cet élément est également présent dans la croûte terrestre sous la forme d'apatite, un minerai dont environ 220 millions de tonnes sont extraites chaque année, principalement pour la production d'engrais. Le phosphore fait ainsi partie des éléments sous tension, dont les ressources sont limitées et très exploitées. Le problème 2 propose d'étudier les propriétés du phosphore, une synthèse de l'acide phosphorique, ainsi que deux méthodes de détection des composés phosphorés dans les effluents. Partie I - Propriétés du phosphore élémentaire Le phosphore existe sous différentes variétés allotropiques. La réduction des ions phosphate contenus dans l'apatite produit du phosphore blanc solide, dont la formule brute est P et qui cristallise dans une structure cubique centrée. Cette forme constitue l'état standard de référence du phosphore à 300 K. Q26. Énoncer les deux règles de construction des configurations électroniques. Donner la configuration électronique du phosphore à l'état fondamental et identifier ses électrons de valence. Q27. Proposer une structure de Lewis pour l'ion phosphate PO . Quelle est la géométrie autour de l'atome de phosphore ? Q28. Représenter une maille de phosphore blanc, en assimilant le motif à une sphère. Déterminer la compacité de ce cristal et donner une valeur numérique de cette compacité. Une autre variété allotropique est le phosphore rouge solide, de formule brute P. Q29. Déterminer l'enthalpie standard et l'entropie standard de la réaction de changement d'état du phosphore blanc en phosphore rouge, supposées indépendantes de la température. Q30. Montrer que la variété allotropique du phosphore la plus stable à 300 K et à pression standard est le phosphore rouge. Commenter le fait que la réduction de l'apatite forme du phosphore blanc dans les conditions normales de pression et température. Le phosphore rouge est notamment utilisé sur le côté des boîtes d'allumettes. Par friction, la température s'élève et il se forme du phosphore blanc qui s'enflamme spontanément au contact de l'air. Cela initie la flamme, qui est ensuite maintenue pendant plusieurs secondes par combustion du bois de l'allumette et de la paraffine dont il est imbibé. Cela fonctionne si la flamme initiale est assez chaude pour déclencher la combustion de la paraffine, en sublimant les 10 mg (2,8 10 mol) de paraffine présents sur la tête de l'allumette. Q31. Déterminer l'énergie thermique nécessaire pour sublimer totalement 10 mg de paraffine initialement à 300 K et à pression atmosphérique. 12/20 Partie II - Synthèse de l'acide phosphorique H3PO4 L'un des procédés les plus utilisés pour former de l'acide phosphorique à partir du phosphore blanc est le procédé thermique. L'acide phosphorique ainsi obtenu présente une haute pureté et peut être utilisé dans les engrais ou pour des applications pharmaceutiques ou alimentaires. Il se décompose en trois étapes : i. combustion du phosphore blanc à l'état gazeux au contact de l'air pour former du pentaoxyde de diphosphore (P O ) gazeux selon la réaction (1) qui sera étudiée à la question Q32. Cette étape est réalisée dans un réacteur ouvert parfaitement agité continu isochore (RPAC), qui fonctionne en régime permanent stationnaire à une pression de 2 bar et à une température de 1 700 K ; ii. hydratation du pentaoxyde de diphosphore à l'aide de vapeur d'eau pour former l'acide phosphorique selon la réaction (2) : P O () + 3 H O() = 2 H PO () (2) iii. refroidissement de l'acide phosphorique obtenu et retraitement des vapeurs issues du réacteur pour en extraire l'acide phosphorique avant de les rejeter vers l'extérieur. On s'intéressera dans cette partie uniquement à la première étape. Le schéma global du procédé thermique est présenté à la figure 5. Figure 5 - Schéma du procédé thermique pour la production d'acide phosphorique La constante thermodynamique d'équilibre de la réaction (1), écrite pour une mole de phosphore blanc, vaut = 10 , et l'enthalpie standard de la réaction est = -3 10 kJ mol. Q32. Écrire l'équation de la réaction (1). Indiquer l'influence d'une augmentation de pression à température constante sur cet équilibre à l'aide d'un raisonnement sur l'expression du quotient réactionnel. Indiquer ensuite l'influence d'une augmentation de température à pression constante sur cet équilibre. Q33. Commenter les conditions réactionnelles retenues par les industriels. Les débits en quantité de matière pour le phosphore blanc dans le réacteur (1) sont notés P () = 1,1 mol s en entrée et P () en sortie. Le débit en volume total en sortie de réacteur est , = 140 L s . Le taux de conversion au sein de ce réacteur est = 99,9 %. La loi de vitesse de la réaction (1) peut s'écrire sous la forme : [P ], avec une constante de vitesse . 13/20 Q34. Effectuer un bilan de matière sur le phosphore blanc au sein du réacteur (1). En déduire une relation entre la vitesse de réaction , le volume du réacteur et les débits en quantité de matière de phosphore blanc en entrée (P ) et sortie (P ). Q35. Déterminer la valeur du volume du réacteur (1) pour un fonctionnement avec le taux de conversion souhaité. Q36. Le taux de conversion obtenu en remplaçant le réacteur (1) par un réacteur RPAC de volume = 6 m , le débit sortant étant inchangé, est = 99,95 %. Commenter. Partie III - Dosage des phosphates dans une eau de rivière Les phosphates d'ammonium et de potassium sont les composants principaux des engrais agricoles. L'utilisation excessive d'engrais peut entraîner une pollution de l'environnement par des ions phosphate (PO ). Ces ions sont sans danger pour la santé humaine, mais un excès de phosphates dans les plans d'eau ou rivières entraîne une eutrophisation, c'est-à-dire une surpopulation d'algues qui amène à un appauvrissement de l'eau en dioxygène et à la disparition des espèces aquatiques. Les quantités d'engrais utilisées sont ainsi réglementées pour assurer une teneur en ions phosphate inférieure à 0,5 mg L dans les eaux, contrôlable par dosage spectrophotométrique selon une méthode décrite par Pradhan et al.1 et présentée ci-dessous. L'acide phosphorique réagit en milieu acide en présence de molybdate d'ammonium ((NH ) MoO ) pour former un complexe phosphomolybdate de couleur jaune [(MoO3 )12 (PO4 )]3- (), noté , selon une transformation modélisée par la réaction (3), quantitative : H PO () + 12 (NH ) MoO () + 21 H () = [(MoO ) (PO )] () + 24 NH () + 12 H O() (3) Le complexe phosphomolybdate réagit ensuite avec de l'acide ascorbique (noté AscH) pour former un complexe de couleur bleue [(MoO ) (PO )] (), noté , par la réaction (4) qui sera étudiée à la question Q39. La couleur bleue provient de la modification du nombre d'électrons du complexe. Une courbe d'étalonnage est réalisée à partir de solutions d'acide phosphorique de concentrations connues, selon le même protocole qui est ensuite utilisé pour la solution à tester : Dans une fiole jaugée de 25 mL sont introduits un prélèvement de 2 mL de l'eau à tester, 1 mL d'acide sulfurique à 10 mol·L-1, 2 mL d'une solution de molybdate d'ammonium à 0,13 mol·L-1, et 1 mL d'acide ascorbique à 0,5 mol·L-1. De l'eau distillée est ajoutée jusqu'au trait de jauge. Après 35 min, l'absorbance de la solution est mesurée à 835 nm. La figure 6 présente le spectre d'absorption d'une solution aqueuse du complexe et la figure 7 la courbe d'étalonnage obtenue à 835 nm en appliquant le protocole précédent à des solutions étalon d'acide phosphorique. Le complexe n'absorbe pas à cette longueur d'onde. 1 S. Pradhan and M. R. Pokhrel, «Spectrophotometric Determination of Phosphate in Sugarcane Juice, Fertilizer, Detergent and Water Samples by Molybdenum Blue Method», Scientific World, Vol 11 (11), 2013, 58-62. 14/20 Figure 6 - Spectre d'absorption du complexe en solution aqueuse Figure 7 - Courbe d'étalonnage réalisée avec des solutions de concentrations connues en acide phosphorique (absorbance mesurée à 835 nm) Q37. Préciser la verrerie à utiliser pour prélever les volumes mentionnés en gras dans le protocole. Expliquer pourquoi on ne réalise pas un dosage pH-métrique de l'acide phosphorique provenant de l'engrais par une solution de soude. Q38. Représenter le diagramme de prédominance de l'acide phosphorique. Indiquer sous quelle forme majoritaire se trouvent les ions phosphate dans la solution réalisée. On supposera que les espèces présentes dans l'eau dosée sont à très faible concentration. Q39. Sachant que le couple [(MoO ) (PO )] ()/[(MoO ) (PO )] () est un couple d'oxydoréduction, écrire l'équation de la réaction (4) et justifier qu'elle est quantitative à 25 °C. Q40. Rappeler les conditions d'application de la loi de Beer-Lambert. Déterminer l'expression littérale de l'absorbance de la solution finale à 835 nm et justifier qu'elle est proportionnelle à la concentration de l'échantillon en ions phosphate, notée . 15/20 L'eau d'une rivière est dosée selon ce protocole. L'absorbance de la solution finale à 835 nm s'élève à 0,25. Le spectrophotomètre utilisé a une précision de mesure de 0,05 en absorbance. Q41. Cette eau respecte-t-elle la réglementation ? On négligera les incertitudes dues aux mesures de volume devant l'incertitude due à la mesure par le spectrophotomètre. Partie IV - Composés organophosphorés Une autre utilisation du phosphore est l'obtention de composés organophosphorées. Dans le langage courant, on désigne par organophosphoré tout composé organique comportant au moins un atome de phosphore. Certains de ces composés sont très toxiques et sont utilisés en tant qu'herbicides, pesticides ou armes de guerre. Le chlorpyriphos, dont la structure est présentée en figure 8, est un exemple d'insecticide commercialisé par la société Dow Chemical depuis 1966, et dont l'utilisation est interdite en Europe depuis 2020. Cl S Cl Cl N O P O O Figure 8 - Structure du chlorpyriphos L'importation de produits issus de cultures traitées est soumise à une réglementation qui varie selon les pays. En Europe, la quantité de chlorpyriphos résiduelle est limitée à 10 mol kg de produit récolté. La présence de ces composés dans l'environnement ou l'alimentation est particulièrement dangereuse car ils sont neurotoxiques. Des techniques fines de détection ont été développées afin d'assurer le respect de la législation. L'une de ces méthodes est l'utilisation d'un biocapteur ampérométrique sélectif pour la détection de composés organophosphorés. À la surface du biocapteur sont greffées deux enzymes, l'acétylcholinestérase, dont le chlorpyriphos est un inhibiteur, et la choline oxydase. IV.1 - Action de l'acétylcholinestérase L'acétylcholinestérase intervient dans la transcription chimique des impulsions nerveuses au niveau des synapses. Le passage des signaux nerveux est rapide, l'enzyme est très efficace et les complexes enzyme-substrat (EACh) ont une très courte durée de vie. L'acétylcholinestérase (notée E) catalyse l'hydrolyse de l'acétylcholine (ACh) en acétate (A) et choline (Ch) selon la réaction (5) suivante : O O + N + O H2O O acétylcholine - + acétate HO + N + + H (5) choline L'eau intervient au cours du mécanisme uniquement dans des étapes qui n'influencent pas la vitesse globale de la transformation. Le mécanisme global peut être assimilé à un mécanisme simplifié de type Michaelis-Menten : E + ACh EACh (i) EACh E + Ch + A (ii) 16/20 Q42. En utilisant une approximation classique au complexe enzyme-substrat (EACh), établir une relation entre les vitesses volumiques des actes élémentaires ( , et ) du mécanisme cidessus. Q43. Écrire la relation traduisant la conservation de la matière en enzyme, en notant [E] la concentration initiale en enzyme. Montrer que la vitesse volumique de formation de chaque produit s'exprime par : [ACh] = + [ACh] avec = et = [E] . Q44. En déduire l'expression de la vitesse volumique initiale de la réaction en fonction de , et de [ACh] . En déduire la relation entre [ACh] et lorsque la vitesse volumique intiale de la réaction est égale à . C. R. Dias Assis et al.2 ont étudié en particulier l'acétylcholinestérase issue du cerveau de poissons amazoniens (C. macropomum) en 2010. L'étude de l'influence de la concentration initiale en substrat [ACh] sur la vitesse volumique initiale d'hydrolyse de l'acétylcholine par l'acétylcholinestérase a donné les résultats rapportés sur la figure 9. Figure 9 - Évolution de la vitesse volumique initiale d'hydrolyse de l'acétylcholine par l'acétylcholinestérase de C. macropomum en fonction de la concentration initiale en acétylcholine Q45. Déterminer graphiquement les valeurs de et de pour cette enzyme. 2 C. R. Dias Assis, P. Fernandes Castro, I. Porto Gurgel Amaral, V. Matoso Matiel Carvalho, L. Bezerra Carvalho Jr. and R. Souza Bezerra, «Characterization of Acetylcholinesterase from the Brain of the Amazonian Tambaqui (Colossoma Macropomum) and in vitro effect of Organophosphorus and Carbamate Pesticides», Environ. Toxicol. Chem., 29, 2010, 2243-2248. 17/20 IV.2 - Inhibition par les composés organophosphorés Le chlorpyriphos, comme de nombreux composés organophosphorés, est un inhibiteur de l'acétylcholinestérase. Lorsque l'acétylcholine n'est plus hydrolysée au niveau des synapses, les signaux nerveux sont plus intenses, ce qui peut provoquer une paralysie, des spasmes et jusqu'au décès. Il existe différentes classes d'inhibiteurs enzymatiques I, caractérisés par une constante de dissociation qui modélise l'affinité de l'inhibiteur pour l'enzyme : - Inhibiteur compétitif : peut se lier à l'enzyme E pour former un complexe enzymeinhibiteur EI non réactif. La vitesse volumique initiale de la réaction est : = - [ACh] [ACh] + 1 + [I] Inhibiteur incompétitif : l'inhibiteur peut se lier au complexe enzyme-substrat pour former un complexe EAChI inactif. La vitesse volumique initiale de réaction est : [ACh] [I] 1 + = [ACh] + [I] 1 + Par analogie avec la situation sans inhibiteur, une vitesse maximale apparente et une constante de Michaelis apparente sont définies de manière à ce que la vitesse volumique initiale en présence d'inhibiteur s'exprime sous la forme : max [ACh]0 = M + [ACh]0 Q46. Préciser pour chaque classe d'inhibiteur comment sont modifiées la vitesse maximale apparente et la constante de Michaelis apparente par rapport au cas sans inhibiteur. La même équipe de chercheurs a étudié l'influence de la présence de chlorpyriphos sur l'activité catalytique de l'acétylcholinestérase de poissons C. macropomum. Les résultats de l'étude sont présentés à la figure 10. Figure 10 - Évolution de l'inverse de la vitesse volumique initiale d'hydrolyse par l'acétylcholinestérase de C. macropomum en présence d'inhibiteur en fonction de l'inverse de la concentration initiale en acétylcholine pour une concentration en chlorpyriphos constante 18/20 Q47. À l'aide de la courbe représentée à la figure 10, déterminer la vitesse maximale apparente et la constante de Michaelis apparente pour l'inhibiteur étudié. Q48. En déduire la classe d'inhibiteurs à laquelle appartient le chlorpyriphos. Justifier. IV.3 - Action de la choline oxydase et détection Deux enzymes sont présentes sur le biocapteur, ainsi que de l'acétylcholine. Lorsque le biocapteur est plongé dans l'échantillon, la présence d'un composé organophosphoré inhibe l'activité de l'acétylcholinestérase et la quantité de choline formée diminue. La seconde enzyme, la choline oxydase, catalyse la réaction (6), qui est supposée rapide et totale : HO + N choline + O O2 + N + H2O 2 (6) aldéhyde de bétaine L'apport en dioxygène est supposé constant, à une pression de 1 bar. Le dispositif permet de réaliser une mesure ampérométrique à partir de trois électrodes, une au chlorure d'argent et deux de platine. Le potentiel de l'électrode de travail en platine est fixé à 0,7 V et le biocapteur mesure l'intensité anodique dans ces conditions. L'échantillon est une eau d'effluent, dont le pH est proche de 7. Dans les conditions de mesure, le potentiel d'équilibre des couples H /H et O /H O valent respectivement = -0,4 V et = 0,8 V. Le biocapteur est sensible jusqu'à des concentrations de l'ordre de 10 mol L en peroxyde d'hydrogène. Q49. Déterminer le potentiel d'équilibre du couple O /H O à la limite de détection du capteur et représenter l'allure des courbes intensité-potentiel associées aux couples en présence dans la solution. Les dérivés de la choline et les enzymes sont supposés redox-inertes. Q50. Justifier que la mesure de l'intensité à 0,7 V est proportionnelle à la quantité de peroxyde d'hydrogène en solution. 19/20 Données relatives au problème 2 à 298 K Numéro atomique du phosphore : (P) = 15. Enthalpie standard de formation et entropies molaires standard (supposées indépendantes de la température) P(, ) = -17 kJ mol P(, ) = 23 J K mol ; P (, ) = 41 J K mol Données relatives à la paraffine (supposées indépendantes de la température) - température de sublimation : = 370 °C = 643 K ; capacité thermique molaire pour la paraffine solide : = 880 J K mol ; enthalpie standard de sublimation : = 500 kJ mol . Constantes d'acidité (supposées indépendantes de la température) L'acide phosphorique est assimilé à un diacide fort. Couple ()/ () ()/ () ()/ () 2,1 p 7,2 12,3 Potentiels standard à pH = 0 Couple (V) ()/ () 0,1 [( ) ( )] ()/[( ) ( )] () 0,5 ()/ () 0,7 (V) (V) 0 1,1 0,7 0,4 Aides de calcul pour le problème 2 3,1 , 0,04 , 0,999 1 27 , 68 + 15,3 = 83,3 880 × 343 = 301 840 , , 7 log(0,8) - 0,1 , 0,07 300 × 92 = 27 600 0,2 4 × 17 = 68 2,8 × 801 840 2 250 000 ln(10) 0,06 V à 298 K FIN 20/20 4,6 4 × 23 = 92 300 × 51 = 15 300 I M P R I M E R I E N A T I O N A L E 25 1053 D'après documents fournis Surtensions à vide sur électrode de platine (les autres couples sont supposés rapides) Couple ()/ () ()/ ()
