X Physique MP 2010
| Thème de l'épreuve | Caractérisation de particules et de pores à l'échelle nanométrique |
| Principaux outils utilisés | rayonnement dipolaire, potentiel chimique |
| Mots clefs | électron élastiquement lié, diffusion des rayons X, adsorption, loi de Guinier, loi de Porod, surface spécifique, loi de Laplace, tension superficielle, condensation capillaire |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - -
Énoncé complet
(télécharger le PDF)






Rapport du jury
(télécharger le PDF)


Énoncé obtenu par reconnaissance optique des caractères
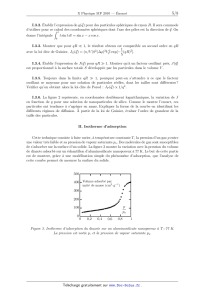
ÉCOLE POLYTECHNIQUE FILIÈRE MP CONCOURS D'ADMISSION 2010 COMPOSITION DE PHYSIQUE (Durée : 4 heures) L'utilisation des calculatrices est interdite pour cette épreuve. Pour les applications numériques, on se contentera d'un seul chiffre significatif. Caractérisation de particules et de pores à l'échelle nanométrique On s'intéresse dans ce problème à la caractérisation de particules et de pores de taille nanométrique (1 nm = 10-9 m) par deux techniques différentes : la diffusion des rayons X aux petits angles et l'adsorption gazeuse. Les trois parties sont indépendantes. Données numériques Vitesse de la lumière dans le vide : Permittivité du vide : Perméabilité du vide : Charge élémentaire : Constante de Rydberg : Masse de l'électron : Nombre d'Avogadro : Masse molaire du diazote N2 : Masse volumique de l'azote liquide : Aire équivalente de la molécule de N2 : Tension superficielle de N2 à 77 K : Constante des gaz parfaits : Volume molaire d'un gaz parfait dans les conditions standard de température et de pression (T = 298 K et p = 1 bar) : Formulaire : X n=0 n xn = c = 0 = µ0 = e = R = me = NA = M = = sm = = RGP = 3, 0 × 108 m · s-1 8, 9 × 10-12 F · m-1 1, 3 × 10-6 H · m-1 1, 6 × 10-19 C 1, 1 × 107 m-1 9, 1 × 10-31 kg 6, 0 × 1023 mol-1 28, 0 g 0, 81 g · cm-3 0, 16 nm2 8, 9 × 10-3 N · m-1 8, 3 J · K-1 · mol-1 VM = 25 L x pour |x| < 1 (1 - x)2 cos x = 1 - x2 x4 + + o(x5 ) 2 24 sin x = x - 1 x3 x5 + + o(x6 ) . 6 120 I. Diffusion des rayons X aux petits angles I.1. Interaction d'une onde électromagnétique avec un électron libre On considère un électron libre qui, en l'absence de toute force, est situé à l'origine du repère orthonormé de vecteurs unitaires (~ex , ~ey , ~ez ) d'un référentiel d'étude, supposé galiléen. Cet électron, de charge -e, est soumis à une onde électromagnétique monochromatique plane de pulsation et de vecteur d'onde ~k = k~ey ; en représentation complexe, le champ électrique de ~ = E0 exp i(t - ~k ·~r) ~ez , l'origine des temps étant choisie de telle manière que cette onde s'écrit E E0 soit réel et positif. On néglige l'effet du champ magnétique sur le mouvement de cet électron et on considère que la propagation se fait dans le vide. I.1.1. On note ~(t) le vecteur position de l'électron à l'instant t. On fait l'approximation que, pour tout t, le champ électrique de l'onde est le même qu'à l'origine. Montrer que l'équation du mouvement de l'électron admet une solution de la forme ~(t) = 0 exp(it)~ez , en représentation complexe, avec 0 = eE0 /me 2 . 1 0 cE02 . 2 L'onde est un faisceau de rayons X de longueur d'onde = 0, 1 nm = 10-10 m, et d'intensité I0 = 200 W · mm-2 . Calculer numériquement 0 puis 0 /, et vérifier la validité de l'approximation faite à la question I.1.1. I.1.2. On rappelle que l'intensité énergétique de l'onde est donnée par I0 = I.1.3. La pulsation caractéristique du mouvement de l'électron autour d'un noyau atomique est 0 = 2cR , où R est la constante de Rydberg. Comparer les valeurs numériques de et 0 et justifier que l'on peut considérer, pour l'interaction d'un électron atomique avec l'onde électromagnétique de la question I.1.2, que l'électron est libre. M z O ~e ~er x y ~e Figure 1. Coordonnées sphériques I.1.4. L'électron accéléré rayonne un champ électromagnétique équivalent à celui d'un dipôle ~ 1 (M ) et B ~ 1 (M ) les électrique de moment dipolaire p(t)~ez = p0 exp(it)~ez = -e~(t). On note E champs électrique et magnétique rayonnés au point M par le dipôle situé à l'origine. Dans le système de coordonnées sphériques de repère orthonormé (~er , ~e , ~e ), leurs expressions au point M (r, , ) (voir figure 1) sont ~ 1 (M ) = E 1 p(t - r/c) sin ~e 40 c2 r et 2 ~ 1 (M ) = µ0 p(t - r/c) sin ~e , B 4c r où p désigne la dérivée seconde de p par rapport au temps. Rappeler le domaine de validité de ces expressions et expliquer la dépendance en t - r/c du champ électromagnétique. ~ 1 (M ) peut se mettre sous la forme I.1.5. Montrer que E ~ 1 (M ) = b E0 exp[i(t - r/c)] sin ~e , E r où b est une constante (appelée longueur de diffusion Thomson) dont on donnera l'expression et dont on calculera la valeur. I.1.6. On place un atome dans le champ de l'onde incidente. Montrer que le champ rayonné par le noyau est négligeable devant celui rayonné par un électron. I.2. Diffusion par un ensemble d'électrons On considère à présent un ensemble de N électrons dont les positions moyennes sont repérées par les vecteurs ~rj , l'origine O étant choisie à l'intérieur de cet ensemble. Ces électrons sont soumis à l'onde électromagnétique de la partie I.1. Il résulte de la question I.1.1 que si la position moyenne de l'électron est ~rj , l'expression complexe de sa position instantanée est ~rj + ~(t) avec ~(t) = (eE0 /m 2 ) exp(it - i~k · ~rj )~ez . I.2.1. On suppose que la distance du point d'observation M à l'origine est très grande devant la taille de l'ensemble d'électrons. Montrer à l'aide d'un schéma que le champ électrique rayonné en M par l'ensemble des électrons est alors donné par ~ ~ 1 (M ) E(M )=E N X exp(i~ q · ~rj ) , j=1 ~ 1 (M ) est le champ obtenu à la question I.1.5 et ~ où E q = k~er - ~k est nommé vecteur de diffusion. I.2.2. Exprimer q = k~ q k en fonction de la longueur d'onde et de l'angle entre ~er et ~k. I.2.3. On dispose au point M un détecteur de rayonnement d'aire SM perpendiculaire à ~er . Soient P la puissance reçue par le détecteur et l'angle solide, supposé petit, sous lequel le détecteur est vu depuis l'origine (SM = r 2 ). Montrer que la section efficace différentielle de diffusion, définie par (~ q ) = (1/I0 )(P/), peut se mettre sous la forme 2 (~ q ) = (b sin ) N X 2 exp(i~ q · ~rj ) . j=1 I.2.4. Exprimer (~ q ) en fonction des vecteurs ~rjk = ~rj - ~rk . On suppose les électrons aléatoirement répartis et N 1. Quelle est la forme asymptotique de (~ q ) lorsque les distances entre les électrons sont toutes très grandes devant q -1 ? Qu'en est-il au contraire lorsque toutes les distances sont petites devant q -1 ? Commenter ces résultats, en termes de l'intensité diffusée par l'ensemble des électrons. I.2.5. À l'aide des résultats de la question précédente, évaluer l'ordre de grandeur en degrés des angles utiles pour obtenir des informations sur la structure de particules d'une dizaine 3 de nanomètres en utilisant la diffusion des rayons X de la question I.1.2. À quelle difficulté technique peut-on s'attendre ? I.3. Diffusion par une suspension diluée de nanoparticules Cette partie concerne un ensemble de n particules solides en suspension dans un volume V . Le milieu est globalement neutre. Les particules sont considérées comme des distributions continues de charge, le volume de chacune d'elles étant noté VP . On note respectivement 1 la densité volumique d'électrons, supposée uniforme, dans la solution, et 2 = 1 + la densité volumique d'électrons à l'intérieur des particules, supposée uniforme elle aussi. On s'intéresse à des rayons X diffusés par ce milieu dans une direction faisant un petit angle avec l'axe d'incidence Oy. (0 < 1). La géométrie est donc la même que précédemment, avec sin 1. Les charges électroniques sont les seules à diffuser. La formule donnée à la question I.2.3 s'adapte en (~ q) = b 2 ZZZ 2 (~r) exp(i~ q · ~r)d3 r , V avec (~r) = 1 dans la solution et (~r) = 2 à l'intérieur des particules. On suppose que V est suffisamment grand pour que ZZZ exp(i~ q · ~r)d3 r soit négligeable, et que la suspension est V suffisamment diluée pour que les particules diffusent indépendamment les unes des autres. I.3.1. On s'intéresse à la grandeur J(~ q ) = (~ q )/V , pour ~ q 6= ~0, qui est une mesure de l'intensité diffusée hors deZZZ la direction d'incidence. On suppose les particules sphériques et identiques, exp(i~ q · ~r)d3 r pour une particule centrée à l'origine. Considérant suc- et l'on note g(~ q) = VP cessivement l'intensité diffusée par une particule centrée à l'origine, puis l'intensité diffusée par ~ montrer que J(~ une particule centrée en un point R, q ) = (n/V )b2 ()2 |g(~ q )|2 . 108 J (cm)-1 106 104 102 100 Données Ajustement global k~ q k (nm)-1 10-2 0,001 0,01 0,1 1,0 Figure 2. Diffusion des rayons X aux petits angles par des nanoparticules de silice [d'après H.K. Kammler et al, 2000 ]. 4 I.3.2. Établir l'expression de g(~ q ) pour des particules sphériques de rayon R. Il sera commode d'utiliser pour ce Zcalcul des coordonnées sphériques dont l'axe des pôles est la direction de ~q. On x donne l'intégrale t sin t dt = sin x - x cos x. 0 I.3.3. Montrer que pour qR 1, le résultat obtenu est compatible au second ordre en qR 1 avec la loi dite de Guinier, JG (~ q ) = (n/V )b2 ()2 VP2 exp[- (qR)2 ]. 5 I.3.4. Établir l'expression de J(~ q ) pour qR 1. Montrer qu'à un facteur oscillant près, J(~ q) est proportionnel à la surface totale S développée par les particules dans le volume V . I.3.5. Toujours dans la limite qR 1, pourquoi peut-on s'attendre à ce que le facteur oscillant se moyenne pour une solution de particules réelles, dont les tailles sont différentes ? Vérifier qu'on obtient alors la loi dite de Porod : JP (~ q ) 1/q 4 . I.3.6. La figure 2 représente, en coordonnées doublement logarithmiques, la variation de J en fonction de q pour une solution de nanoparticules de silice. Comme le montre l'encart, ces particules ont tendance à s'agréger en amas. Expliquer la forme de la courbe en identifiant les différents régimes de diffusion. À partir de la loi de Guinier, évaluer l'ordre de grandeur de la taille des particules. II. Isotherme d'adsorption Cette technique consiste à faire varier, à température constante T , la pression d'un gaz p entre une valeur très faible et sa pression de vapeur saturante ps . Des molécules de gaz sont susceptibles de s'adsorber sur la surface d'un solide. La figure 3 montre la variation avec la pression du volume de diazote adsorbé sur un échantillon d'aluminosilicate nanoporeux à 77 K. Le but de cette partie est de montrer, grâce à une modélisation simple du phénomène d'adsorption, que l'analyse de cette courbe permet de mesurer la surface du solide. 500 400 Volume adsorbé par unité de masse (cm3 ·g-1 ) 300 200 p ps 100 0 0 0,2 0,4 0,6 0,8 1 Figure 3. Isotherme d'adsorption du diazote sur un aluminosilicate nanoporeux à T=77 K. La pression est notée p, et la pression de vapeur saturante ps . 5 II.1. Modèle de Langmuir de l'adsorption monocouche Le modèle de Langmuir repose sur les hypothèses suivantes : tous les sites d'adsorption sont équivalents ; les molécules adsorbées n'interagissent pas entre elles et le mécanisme d'adsorption est le même pour toutes les molécules. Notant S l'aire du solide en contact avec le gaz, supposé parfait, et sm l'aire d'une molécule, on considère qu'il y a NS = S/sm sites d'adsorption. On modélise l'adsorption par la réaction réversible s0 + mG = smA , où s0 est un site de surface non occupé, mG une molécule à l'état gazeux et smA un site de surface occupé par une molécule adsorbée. On considère la couche adsorbée comme un fluide binaire bidimensionnel, assimilé à un mélange condensé idéal et composé de sites vides et de sites occupés. On note NAd le nombre de molécules adsorbées et = NAd /NS le taux de couverture. Dans cette partie, 0 6 6 1. II.1.1. Soit K(T ) la constante d'équilibre de cette réaction et p0 la pression standard de référence (p0 = 1 bar). Montrer que K(T ) = . (1 - )p/p0 II.1.2. Le processus d'adsorption est exothermique. Quel est le signe de l'enthalpie standard de réaction r H 0 (T ) ? On fait l'approximation que r H 0 (T ) ne dépend pas de la température. Comment K(T ) dépend-il de T ? II.1.3. Notant a = K(T )/p0 , exprimer et tracer la variation de en fonction de p. Le résultat permet-il d'interpréter la courbe de la figure 3 ? II.2. Théorie BET (Brunauer, Emmett et Teller) de l'adsorption multicouche En réalité, lorsque la pression augmente, il se produit une adsorption multicouche non uniforme (figure 4). On note 0 , 1 , · · · , n , · · · la proportion de sites de surface ayant 0, 1, · · · , n, · · · molécules de gaz adsorbées. Figure 4. Modèle d'adsorption multicouche. II.2.1. On généralise le modèle de la partie II.1 en exprimant l'équilibre entre les couches n - 1, n, et le gaz sous la forme 1 = ap0 , 2 = bp1 , · · · n = bpn-1 , · · · Justifier le fait qu'à part celle qui concerne la première couche, toutes les constantes d'équilibre sont égales et que bp < 1. On note C = a/b et l'on suppose C > 1. II.2.2. Exprimer n (n > 0) en fonction de C, du produit bp et de 0 . II.2.3. Calculer 0 en fonction de C et de bp. 6 II.2.4. Montrer que le taux de couverture total = NAd /NS , où NAd est le nombre total de molécules adsorbées, est Cbp = . (1 - bp)[1 + (C - 1)bp] Lorsque p ps , le gaz se liquéfie. Justifier l'égalité bps = 1. II.2.5. La relation établie à la question II.2.4 est maintenant mise à profit pour déterminer la surface spécifique (surface par unité de masse) de poudres ou de matériaux poreux. Elle est généralement utilisée sous une forme équivalente, dite de BET (Brunauer, Emmett et Teller) ; notant vA le volume total de gaz adsorbé par unité de masse du solide et vS le volume maximal adsorbable dans la première couche par unité de masse de solide ( = NAd /NS = vA /vS ), l'équation BET est Å ã p p/ps 1 1 + (C - 1) . = vA (1 - p/ps ) vS C ps Les données du début de l'isotherme de la figure 3 ont été reportées sur la figure 5 conformément à l'équation BET. La valeur du volume de gaz adsorbé est donnée dans les conditions standard de température et de pression. Déterminer l'ordre de grandeur de C et la valeur de vS , et en déduire la surface spécifique de l'aluminosilicate. 0,006 p/ps [g·cm-3 ] vA (1 - p/ps ) 0,005 0,004 0,003 0,002 p ps 0,001 0 0 0,05 0,1 0,15 0,2 0,25 0,3 Figure 5. Détermination d'une surface spécifique par la méthode BET. III. Condensation capillaire En plus de l'adsorption de surface étudiée dans la partie II, il peut se produire une condensation du gaz en dessous de la pression de vapeur saturante dans les pores de taille nanométrique. Cet effet est dû à la surpression qui règne dans le gaz par suite des forces de tension superficielle dans le cas d'une interface liquide-gaz présentant un ménisque. III.1. Soit une bulle de gaz sphérique de rayon r dans un liquide. Le gaz et le liquide sont deux phases d'un même corps pur. On admet que la pression du gaz pG est reliée à la pression dans le liquide pL par la relation pG = pL + 2/r, où est nommée constante de tension superficielle. Montrer que a la dimension d'une force par unité de longueur. 7 III.2. On traite le gaz comme un gaz parfait. Soit µG (T, p0 ) son potentiel chimique à la température T et à la pression de référence p0 . Rappeler l'expression du potentiel chimique µG (T, pG ) pour une pression pG quelconque. III.3. Notant vL le volume molaire du liquide et admettant que le potentiel chimique de ce dernier est de la forme µL (T, pL ) = µL (T, p0 ) + vL (pL - p0 ), établir la condition d'équilibre entre le liquide et le gaz pour une bulle sphérique de rayon r. III.4. Dans la limite où r est infini (interface plane), expliquer pourquoi la valeur de pG à l'équilibre est la pression de vapeur saturante ps . III.5. On note pG (r) la valeur de pG à l'équilibre pour une bulle de rayon r. Établir la relation entre pG (r) et ps . III.6. Sous une approximation que l'on justifiera, montrer que pG (r) = ps exp(-r0 /r), et donner l'expression de r0 en fonction de , vL , T , et de la constante des gaz parfaits RGP . III.7. Calculer r0 pour du diazote à 77 K et en déduire le rapport pG /ps pour la condensation capillaire dans des pores de 5 nm, 10 nm et 100 nm (figure 6). gaz 2r couche adsorbée liquide Figure 6. Condensation dans un pore cylindrique. III.8. L'isotherme d'adsorption de la figure 3 montre que la condensation capillaire s'ajoute à l'adsorption de surface étudiée précédemment. Déduire de cette courbe le diamètre moyen des pores en tenant compte de l'épaisseur de la couche adsorbée avant condensation eA = 2, 1 nm. 8
