Centrale Physique et Chimie 2 MP 2021
| Thème de l'épreuve | Purification de l'eau du circuit primaire dans une centrale nucléaire |
| Principaux outils utilisés | optique ondulatoire, électromagnétisme, cristallographie, thermodynamique, solutions aqueuses |
| Mots clefs | spectrométrie, réseau, trous d'Young, résolution, torche, plasma, théorème d'Ampère, effet de peau, milieu ohmique, plutonium, résines échangeuses |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)







Rapport du jury
(télécharger le PDF)

Énoncé obtenu par reconnaissance optique des caractères
Physique-chimie 2
MP
4 heures Calculatrice autorisée
2021
A propos de la purification de l'eau du
circuit primaire dans une centrale nucléaire
Un réacteur nucléaire à eau sous pression est constitué de trois principaux
circuits d'eau qui permettent l'éva-
cuation de la chaleur (figure 1). Le circuit primaire permet le transfert de
l'énergie depuis le coeur du réacteur
(où se situe le combustible et s'opère la fission nucléaire) vers le générateur
de vapeur.
La contamination de l'eau du circuit primaire provient principalement de la
corrosion des parois métalliques
(cuve de réacteur, tuyaux, pompes, etc.). La conséquence est qu'une fraction
des éléments constitutifs des aciers
va se solubiliser et ainsi progressivement charger en ions métalliques le
fluide primaire en s'y accumulant, car il
circule en circuit fermé. Le contrôle et la purification de l'eau sont
nécessaires, ce qui est réalisable via la mise
en dérivation d'une certaine quantité de fluide.
Ce sujet s'intéresse tout d'abord à l'élément plutonium et à son oxyde présent
dans la composition du combustible
nucléaire MOX (partie I). Il présente ensuite les résines échangeuses d'ions
qui sont utilisées pour purifier l'eau
(partie Il). Enfin, il aborde la technique de spectrométrie ICP-AES qui permet
notamment l'étude de l'abondance
des éléments métalliques présents dans le fluide primaire (partie IT).
Certaines données numériques et un formulaire sont fournis en fin d'énoncé. Il
importe d'en prendre connaissance
avant de traiter le sujet.
Certaines questions, peu ou pas guidées, demandent une prise d'initiative de la
part du candidat. Elles sont
signalées par une barre dans la marge gauche. Il est alors demandé d'expliciter
clairement la démarche de
résolution, les hypothèses effectuées et d'illustrer le raisonnement, le cas
échéant, par des schémas. Le barème
valorise la prise d'initiative et tient compte du temps nécessaire à la
résolution de ces questions. Les résultats
établis dans ces questions ne sont toutefois pas indispensables pour le
traitement des autres questions du
problème.
De façon plus générale, le candidat est invité à expliciter toutes les
hypothèses et initiatives qu'il est amené à
prendre, y compris en dehors de ces questions.
Réacteur nucléaire
(enceinte de sécurité)
Générateur de vapeur
(échangeur de chaleur)
Figure 1 Schéma des trois circuits principaux d'une centrale nucléaire à eau
sous pression!
1 Frédéric Gressier. Étude de la rétention des radionucléides dans les résines
échangeuses d'ions des circuits d'une centrale nucléaire
à eau sous pression. Chemical Sciences. Ecole Nationale Supérieure des Mines de
Paris, 2008.
P021/2021-03-05 08:22:32 Page 1/9 (cc AUREZ
I Le plutonium dans le combustible nucléaire MOX
Le combustible nucléaire MOX est utilisé dans certains réacteurs nucléaires. Il
s'agit d'un mélange d'oxydes
d'uranium et de plutonium dans lequel ce dernier élément intervient à environ 8
%.
IA --- Présentation du plutonium
Le plutonium est un élément chimique qui est des plus rares dans la nature et
presque exclusivement produit
par l'homme dans le coeur des réacteurs nucléaires de 1940 à nos jours.
Q 1. Le numéro atomique du plutonium est 94 et sa configuration électronique
dans son état fondamental
est [Rn]5f°7s?. Indiquer sa place dans la classification périodique (bloc,
période). Préciser les électrons de coeur
et ceux de valence.
Q 2. Le plutonium possède-t-il des électrons célibataires à l'état fondamental
? Si oui, proposer un quadru-
plet de nombres quantiques, que l'on nommera, pouvant caractériser l'un des
électrons célibataires.
I.B --- Oxyde de plutonium
L'oxyde de plutonium Pu,;O,,, qui entre dans la composition du combustible MOX,
est un solide ionique constitué
d'ions Pu*+ et O2. Il cristallise dans l'une des structures représentées figure
2.
o--
Structure À Structure B
Figure 2
Q 3. Déterminer, pour chaque structure et pour chaque entité, le nombre
d'entités en propre dans la maille
concernée. Montrer qu'une seule des deux structures est possible pour Pu,O,,.
Donner alors la formule de cet
oxyde et le nombre de motifs par maille.
Q 4. Déterminer la coordinence de chacun des ions dans la structure choisie à
la question précédente.
Q 5. On donne respectivement le rayon ionique de l'ion oxyde O7 et la masse
volumique de l'oxyde de
plutonium : R(O*) -- 140 pm et Pru,O, -- 11.5 x 10° kg-m *. En admettant la
tangence anion-cation, calculer
le rayon ionique du plutonium Put. Commenter le résultat obtenu sachant que la
valeur trouvée dans la
littérature est de 86 pm.
Q 6. Calculer la compacité de cette structure. Commenter la valeur obtenue.
II Les résines échangeuses d'ions et la purification de l'eau
L'eau du circuit primaire d'une centrale nucléaire est traitée à l'aide de
filtres et de résines échangeuses d'ions
(notées RET dans la suite du sujet). Ce traitement à base de REI permet de
décontaminer le fluide tout en
conservant ses propriétés physicochimiques.
Les REI possèdent la faculté d'échanger des ions contenus en leur sein avec les
ions contenus dans la solution
aqueuse qui est mise en contact avec elles. Elles sont constituées de chaînes
polymères réticulées entre elles par
des agents spécifiques. Les résines échangeuses de cations portent des charges
négatives sur leur squelette qui
sont compensées par des ions NaT ou HT appelés « contre-ions ». La figure 3
montre un exemple d'échange de
ces ions.
IT. A -- Synthèse des REIT
Les billes de polymères constituant les REI correspondent à un polystyrène
réticulé porteur de groupes fonction-
nels. Pour les synthétiser, un des précurseurs utilisés est le vinylbenzène,
aussi appelé styrène. Nous étudierons
dans cette partie une méthode de synthèse industrielle du styrène.
P021/2021-03-05 08:22:32 Page 2/9 (cc) BY-NC-SA
Figure 3
La production de styrène (noté S) est très largement assurée par la
déshydrogénation de l'éthylbenzène (noté
E), selon une réaction d'équation :
NN
À -- À + EH, (IL.1)
Pour simplifier, nous noterons aussi l'équation de cette réaction : E = S' + H..
Les gaz seront considérés comme parfaits. La réaction s'effectue en phase
gazeuse.
Q 7. À l'aide de la figure 4, calculer l'entropie standard de réaction À,.S" et
l'enthalpie standard de réaction
À,.H°, en considérant qu'elles sont indépendantes de la température dans le
domaine de température étudié.
La réaction est-elle endothermique ou exothermique ? Auraït-on pu prévoir sans
calcul le signe de l'entropie
standard de réaction À,.5° ?
10° é
1071 (2
10 2 e
10
1074 e
K°
©
10° :
106 e
107 e
10--È
10° e
10710
0,0010 O,0015 0,0020 0,0025
1/T(K°)
Figure 4
Q 8. Prévoir, justification à l'appui, dans quel sens l'équilibre est déplacé
lors d'une augmentation de
pression à température et composition constantes.
Q 9. Prévoir, justification à l'appui, dans quel sens l'équilibre est déplacé
lors d'une élévation de température
à pression et composition constantes.
Q 10. La synthèse industrielle du styrène par déshydrogénation de
l'éthylbenzène s'opère généralement
dans un réacteur de volume constant où l'on mélange de la vapeur d'eau à
l'éthylbenzène (dans un rapport de
plusieurs moles d'eau par mole d'éthylbenzène), à une température d'environ 650
°C et à une pression totale
voisine de la pression atmosphérique, en présence d'un catalyseur à base
d'oxydes de fer. Commenter le choix
de ces conditions opératoires.
P021/2021-03-05 08:22:32 Page 3/9 (cc) BY-NC-SA
ITI.B --- Détermination de la capacité d'échange d'une résine
Une résine échangeuse d'ions peut être vue comme un réservoir de contre-ions
prêts à être échangés. La capacité
d'échange maximale (notée CE) de ce réservoir, c'est-à-dire la quantité de
matière de contre-ions qui peuvent
être échangés par unité de masse de résine humide, est une donnée essentielle à
connaître pour les manipulateurs.
Il est précisé que les ions présents sur la résine ne peuvent être impliqués
que dans des réactions d'échange,
comme celles que l'on peut écrire avec le formalisme de Vanselow. Dans ce
formalisme, on part de l'hypothèse
fondamentale que l'échange d'ions peut se traduire par une réaction chimique
classique. Pour exemple, si la
réaction étudiée se fait entre une résine contenant initialement un ion A*4 et
une solution contenant le contre-
ion B7E, on écrira pour l'échange
ZA Z2B Z A ZB
2BA(és) + ZA Bag © 2BA (ag) + ZAB (rés)
La détermination expérimentale de la valeur de CE d'une résine échangeuse
d'ions HT peut s'obtenir par un
protocole de titrage en retour. L'étude se fera sur la résine IRN 97H.
Une masse m connue de 0,50 g de résine humide est introduite dans un bécher
contenant V = 100,0 mL d'une
solution de soude en excès (NaY + HO") à la concentration C = 0,025 mol-L !.
Après 2 h d'agitation, un volume
V, = 50,0 mL de solution est prélevé et la soude en excès est dosée par une
solution d'acide chlorhydrique de
concentration C, = 0,10 mol-L !. Le suivi du titrage se fait par pH-métrie et
la courbe obtenue est donnée
figure 5. On mesure un volume équivalent noté VW...
13
X x
XXE XX XX XX XX X XX XX X M x
X x
X_X
11 X x,
9 %
MRRX KT":
x
XX
: X X X
XXXXXXXXX À
0 1 2 3 4 9 6 :7 8 9 10
V (mL) 6,7 mL
Figure 5 Suivi pH-métrique du titrage de la soude en excès par la solution
d'acide
chlorhydrique de concentration ©, = 0,10 mol-L'!
orilice de remplissage
solution saturée de KCI
Bl de platine
gaine isolante
mercure
calomel
jonction
cristaux de KCI
verre fritté
|
Capteur 1 Capteur 2 Capteur 3 Capteur 4
Figure 6 Différents capteurs
Q 11. En utilisant le formalisme d'échange ionique de Vanselow, écrire
l'équation bilan traduisant l'échange
des ions HT sur la résine.
P021/2021-03-05 08:22:32 Page 4/9 cc BY-NC-SA
Q 12. Écrire l'équation de la réaction support du titrage.
Q 13. Proposer un montage expérimental pour réaliser le dosage : choix de la
verrerie et choix des capteurs.
Vous donnerez le nom de chaque capteur représenté figure 6 et indiquerez celui
(ceux) à utiliser pour l'expérience
ainsi que leur rôle.
Q 14. Exprimer, avec les données littérales fournies, la quantité d'ions
hydroxyde HO restant, notée no.
dans le volume V'initial. Faire l'application numérique.
Q 15. Lors d'une séance de travaux pratiques, quand on réalise un seul titrage,
à quel type d'évaluation de
l'incertitude peut-on procéder ? Expliquer. Le volume V, a été mesuré avec une
pipette jaugée double trait de
tolérance 0,1 mL. Identifier au moins une source possible d'incertitude.
Q 16. On estime l'incertitude-type sur nyo-, à 1 X 10° mol. De quelle manière
devez-vous présenter le
résultat sur nyo-, ? On fournira une incertitude élargie pour un niveau de
confiance de 95 %.
Q 17. Écrire l'expression littérale de la capacité d'échange CE puis faire
l'application numérique.
III La spectrométrie ICP-AES
Cette partie s'intéresse à quelques aspects de la spectrométrie ICP-AES,
acronyme de Inductively Coupled
Plasma - Atomic Emission Spectrometry (plasma à couplage inductif -
spectrométrie d'émission atomique). Il
s'agit d'une technique d'analyse de grande précision permettant la mesure de la
nature et de la concentration
des éléments qui se trouvent dans les matières solides, les liquides ou les
gaz. On peut notamment déterminer
grâce à celle-ci l'abondance des métaux lourds dans l'eau du circuit primaire
d'une centrale nucléaire ou encore
contrôler l'efficacité des résines échangeuses d'ions.
Un spectromètre ICP-AES utilise une torche à plasma (figure 7). À la base de la
torche sont introduits de
l'argon, ainsi que l'échantillon à analyser à l'état d'aérosol
(microgouttelettes d'un diamètre maximum de l'ordre
de 100 pm). Le plasma est initié par l'envoi d'une décharge électrique et doit
ensuite être entretenu à l'aide d'un
bobinage qui crée un champ magnétique variable à haute fréquence.
analyse spectrale
plasma 17 de la lumière par
monochromateur
2
à réseau
bobinage /
d'induction HF
4
argon échantillon
en aérosol Photographies du plasma d'une torche
, | Vue latérale à gauche et vue axiale à droite
Schéma d'une torche à plasma
Figure 7
Dans le plasma, à plusieurs milliers de kelvins, l'échantillon est vaporisé,
désolvaté, atomisé voire ionisé. Les
atomes sont ionisés si leur énergie d'ionisation est inférieure à celle de
l'argon, ce qui est le cas de la plupart des
éléments chimiques.
Chaque atome ou ion excité émet plusieurs photons (rayonnement lumineux) à des
longueurs d'onde qui lui sont
propres lors de son retour à l'état fondamental. La lumière est envoyée vers un
monochromateur à réseau dont
la résolution spectrale en longueur d'onde est très élevée, voisine de 20 pm.
Les signaux lumineux sont mesurés
par un capteur qui permet l'analyse de longueurs d'onde allant de 166 à 847 nm,
l'intensité des pics émis étant
fonction de la concentration de l'échantillon initial.
Nous allons dans un premier temps étudier un modèle simple de la partie optique
du dispositif. Ensuite, nous
nous intéresserons aux effets du champ magnétique variable sur le plasma.
TITI. À -- Spectroscopie et résolution
III. A.1) Interférences à deux ondes
On considère le dispositif de la figure 8. Une pupille dans le plan
perpendiculaire à l'axe (O2) est percée de deux
trous d'Young identiques espacés de la distance a. Une onde plane progressive
monochromatique de longueur
d'onde À (dans l'air, assimilé au vide) éclaire cette pupille en incidence
normale. On observe la figure obtenue
dans le plan focal image d'une lentille de centre optique O et d'axe optique
(Oz). On repère un point M de
l'écran recevant les ondes issues des deux trous par ses cordonnées
cartésiennes (x, y, f").
P021/2021-03-05 08:22:32 Page 5/9 (cc) BY-NC-SA
> 5 | MK(x, y, f")
Y
ù
À
\
Figure 8
Q 18. Établir l'expression de la différence de marche 6(M) en fonction de a, x
et f', en faisant les approxi-
mations jugées utiles.
Q 19. Établir l'expression de l'intensité lumineuse Z(M). Décrire la figure que
l'on observe sur l'écran.
Q 20. Calculer numériquement l'interfrange pour a = 100 pm, f" = 20 em et À =
499,3 nm (longueur d'onde
associée à une raie du nickel présent dans un échantillon).
Q 21. La résolution d'un spectromètre est le plus petit écart entre deux
longueurs d'onde que l'on peut
séparer. Expliquer pourquoi le dispositif précédent à deux trous d'Young ne
peut permettre d'atteindre la
résolution voisine de 20 pm d'un spectromètre ICP-AES.
III. A.2) Interférences à N ondes
On considère à présent un réseau constitué de N ouvertures identiques (N > 2),
distantes de a suivant l'axe
parallèle à (Ox). Ces N ouvertures sont éclairées par une onde plane
progressive monochromatique en incidence
normale de longueur d'onde À. Sur la figure 9, l'angle 0, orienté selon le sens
trigonométrique, indique une
direction des interférences à l'infini à N ondes.
Y
Y
\
Figure 9
Q 22. Expliciter le déphasage & entre deux ondes issues de trous successifs en
fonction de À, a et 6.
Q 23. Justifier qu'on observe un maximum d'intensité si on à & = 2pr avec p un
entier relatif accessible.
Comment appelle-t-on l'entier p ? Exprimer l'angle 0, correspondant au pic p =
I.
Q 24. Le réseau utilisé dans certains spectromètres ICP-AES comporte 1800
ouvertures par millimètre. Calcu-
ler numériquement 0, pour À = 499,3nm. Pourquoi n'est-il plus envisageable
d'utiliser le dispositif de projection
(lentille et écran) décrit en III.A.1 ?
Q 25. Établir que la demi-largeur d'un pic d'intensité lumineuse est donnée par
Ag = 2r/N et en déduire
la demi-largeur angulaire AO du pic observé dans la direction 0.. Évaluer
numériquement A0, sachant que les
N ouvertures éclairées du réseau occupent une largeur £ = 5 cm.
Q 26. On considère que la source émet une deuxième longueur d'onde À" très
proche de À. On note 0: l'angle
d'observation du premier pic (p = 1) correspondant à la longueur d'onde \". On
admet que l'on peut séparer
les deux pics seulement si [0 -- 0,} > A0. Obtenir l'expression de la
résolution du dispositif en fonction des
grandeurs utiles parmi À, NV et a.
Q 27. Évaluer numériquement la résolution du réseau utilisé. Proposer des
raisons visant à expliquer la
différence entre cette valeur et celle, voisine de 20 pm, d'un spectromètre
ICP-AES.
ITI.B --- Interaction champs -- plasma dans la torche
L'étude analytique du plasma de la torche de la figure 7 est complexe en raison
notamment de la géométrie
cylindrique du dispositif, de la forme du bobinage d'induction haute fréquence,
de l'écoulement du gaz, des effets
thermiques... On va néanmoins chercher à dégager quelques aspects physiques à
l'aide d'une approche simplifiée
en géométrie unidimensionnelle cartésienne.
P021/2021-03-05 08:22:32 Page 6/9 (cc) BY-NC-SA
On repère un point de l'espace par ses coordonnées cartésiennes (x,y,z) dans
une base orthonormée directe
(é,. y: é,). Le plasma est un gaz composé d'ions supposés fixes et d'électrons
mobiles. Il est localement neutre
dans tout le domaine --a < x < a qu'il occupe et où sa densité électronique n est uniforme et constante. Le domaine du plasma est délimité par deux lames planes identiques (épaisseur b) qui modélisent le bobinage inducteur haute fréquence. La lame de droite est parcourue par un vecteur densité de courant électrique uniforme J(t)é, et celle de gauche par le vecteur opposé --J(t)é, (figure 10). On néglige les effets de bords selon les directions y et z. On admet dans toute la suite que les fréquences de travail sont suffisamment faibles pour se placer dans l'approxi- mation des régimes quasi-stationnaires magnétique. Cette hypothèse permet d'écrire les équations de Maxwell sous la forme approchée suivante : _ _,= 0B _ 7, divE =" rot E = ----, div B = 0, rot B = up]. EUR) Ot Q 28. Donner, sans démonstration, l'expression, sous forme intégrale, des quatre équations de Maxwell écrites ci-dessus dans une formulation locale. 417 --J(t}e, J(4E, © © x OTY _ b D 2a D b _ lame de courant plasma lame de courant Figure 10 III.B.1) Champ magnétique produit par les lames Q 29. Déterminer, en explicitant soigneusement l'argumentation, le champ magnétique produit dans tout l'espace uniquement par la lame de gauche (on ne tiendra donc pas compte de l'autre lame et du plasma). Q 30. En déduire le champ magnétique produit dans tout l'espace par l'ensemble des deux lames, sans tenir compte du plasma. Représenter en fonction de x, pour une valeur donnée de J(t) non nulle, le profil de ce champ magnétique. III.B.2) Propriétés dans le plasma Q 31. Expliquer qualitativement pourquoi il peut exister dans le plasma un champ électrique dû aux courants dans les lames. Montrer qu'il s'écrit sous la forme ÆE(x,t) -- E(x,t)e, et justifier que E(x,t) est une fonction impaire de la variable x. Q 32. Le champ magnétique qui règne dans le plasma ne correspond pas à celui produit par les lames calculé précédemment. Expliquer qualitativement pourquoi. Montrer qu'il s'écrit sous la forme B(x,t) -- B(x,t)e, et justifier que B(x,t) est une fonction paire de la variable x. Q 33. Le vecteur densité de courant électrique dans le plasma s'écrit J(x,t) = j(x,t)e,. Expliciter, d'une part, l'équation aux dérivées partielles reliant E(x,t) et B(x,t) et, d'autre part, celle reliant B(x,t) et j(x,t). À ce stade, il manque une loi de réponse du plasma (c'est-à-dire une relation liant 7(x,t) et E(x,t)) afin d'accéder aux profils des divers champs en son sein. On souhaite répondre à ce manque en utilisant tour à tour deux modèles très différents. Il s'agit de voir lequel des deux est le plus acceptable pour comprendre ce qu'il se passe dans une torche à plasma dans notre approche simplifiée. III.B.3) Modèle non collisionnel Dans ce premier modèle, on néglige les collisions dans le plasma ainsi que la force magnétique. Les électrons, de densité volumique n uniforme et constante, de masse m et de charge --e, sont non relativistes et la seule force qui agit sur eux est d'origine électrique. Le vecteur densité de courant électrique 7(x,t) et le champ électrique E (x,t) sont alors liés par la relation différentielle suivante : 7 2 Oj(x, t) _ (xt). Ot m P021/2021-03-05 08:22:32 Page 7/9 (cc) BY-NC-SA O2E(x.t 1 0 E{æ,t) -- -- E(x,t) = 0 où À est une grandeur à déterminer en Ox? X2 fonction des données. Vérifier que l'expression de À lui confère une dimension cohérente avec celle attendue au regard de l'équation différentielle précédente. Q 34. Montrer que E(x,t) est solution de cosh(x/À) Q 35. Obtenir la forme générale de E(x,t). En déduire que B(x,t) = ------ cosh(a/À) B,(t) en posant B,(t) -- B(a,t). On ne tiendra pas compte de tout champ magnétique statique. Q 36. Déterminer E{x,t) et j(x,t) en fonction de x, a, Ho, À, Bit) et dB,(t)/dt. Q 37. Rappeler l'expression de la puissance volumique cédée par le champ électromagnétique aux électrons et l'exprimer en fonction des données du problème. Que vaut-elle en moyenne sachant que l'excitation par le bobinage d'induction haute fréquence est périodique ? Pourquoi ce modèle n'est-il pas acceptable pour décrire l'entretien du plasma de la torche du spectromètre ICP-AES ? III.B.4) Modèle collisionnel Dans ce second modèle, on considère que la densité du plasma est telle qu'il n'est plus possible de négliger les collisions en son sein. On admet qu'il se comporte alors comme un milieu ohmique, c'est-à-dire que 7 = oE où o est la conductivité électrique du plasma est une grandeur réelle, supposée uniforme et constante. Q 38. Établir l'équation aux dérivées partielles vérifiée par B(x,t). On se place en régime sinusoïdal forcé de pulsation w. Le champ magnétique dans le plasma est associé au champ complexe B(x,t) = f(x) exp(iwt)é,. Le champ électrique est associé au champ complexe E(x,t) = g(x) exp(iwt)e,,. Les fonctions f(x) et g(x) sont à priori à valeurs complexes. On pose la constante réelle f, = f{a) = f(--a). 2 Q 39. On note Ô -- . Quelle est la dimension de Ô ? Justifier. | Ho0w Q 40. Déterminer le champ magnétique complexe B(x. t) en fonction de x, t, a, w, 8 et f, en faisant intervenir la fonction cosinus hyperbolique à variable complexe. Une fois le champ magnétique déterminé, il est possible d'en déduire l'expression du champ électrique complexe -->
E(x,t) dans le plasma, puis la puissance volumique moyenne cédée au plasma.
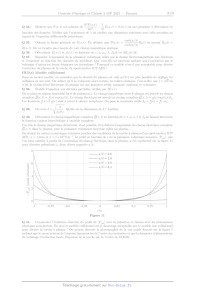
On choisit les valeurs numériques suivantes proches des conditions de la torche
à plasma d'un spectromètre ICP-
AFS : a = 1,0cm et o = 1 x 10° S-m !. Le profil en fonction de x de la
puissance volumique moyenne (P,.,), que
l'on peut calculer à partir de l'expression du champ électrique dans le plasma,
a été représenté sur la figure 11
pour diverses pulsations w, donc divers rapports a/à.
a/ù = 2,8
| |
\ 1 /,
_] 0,75 0.5 0,25 0 0,25 0,5 0,75 1
x/a
ë |
a/à = 0,6
a/ô = 2,0
©
HS
7
\
(Pa) (unité arbitraire)
Figure 11
Q 41. Commenter l'évolution observée du profil de {P,.,,) avec la pulsation en
liaison avec les phénomènes
physiques sous-jacents. En quoi ce modèle collisionnel est-il davantage
acceptable que le modèle non collisionnel
pour décrire la torche à plasma ? On pourra discuter la photographie de la vue
axiale fournie sur la figure 7
sachant que le rayon externe de l'anneau lumineux est de l'ordre du centimètre
et que la fréquence d'alimentation
du bobinage d'induction haute fréquence de la torche est de l'ordre de 10 MHz.
P021/2021-03-05 08:22:32 Page 8/9 (cc) BY-NC-SA
Données
Perméabilité magnétique du vide Lo = 1,26 x 10 © H-m !
Permittivité diélectrique du vide En = 8,85 x 10 2 Fm !
Charge élémentaire e = 1,60 x 10 1 C
Masse de l'électron m = 9,11 x 10 °1 kg
Constante d'Avogadro N 1 = 6,02 x 10° mol !
Constante de Boltzmann kp = 1,38 x 10 # JK |
Constante des gaz parfaits R = 8,31J-K !-mol {
Constante de Planck h = 6,63 x 10 * Je
Vitesse de la lumière dans le vide c = 3,00 x 10° ms !
Extrait du tableau périodique (masses molaires en g-mol!)
Numéro atomique 1 8 11 94
Symbole H Ô Na Pu
Masse molaire 1,01 16,0 23,0 244
Formulaire
-- On note i l'unité imaginaire telle que i? = --1.
-- Pour deux grandeurs a(M,t) et b(M,t) variant sinusoïdalement en fonction du
temps avec une pulsation
commune w, on pose
a(M,t) = Rela(M,#)] = Refa,(M)e] et b(M,t) = Refb(M, #)] = Relb,(M)eï']
La moyenne temporelle du produit de a(M,t) et b(M,t) est
I
(ab) -- ; Rela b"] où b" désigne le complexe conjugué de b.
-- Les fonctions cosinus hyperbolique et sinus hyperbolique à variable z
complexe sont définies par
exp(z) + exp(--2)
2
sinh(z) = exp(z) exp(Ca)
h --
cosh(z) 5
et
ee eFINeee
P021/2021-03-05 08:22:32 Page 9/9 (cc) BY-NC-SA
