Centrale Physique et Chimie 1 MP 2021
| Thème de l'épreuve | La ruée vers l'or |
| Principaux outils utilisés | thermochimie, physique statistique, diffusion thermique, électromagnétisme, physique des ondes |
| Mots clefs | nanoparticules, système à deux niveaux, indice optique, dispersion, résonance, plasmon, onde électromagnétique |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)








Rapport du jury
(télécharger le PDF)



Énoncé obtenu par reconnaissance optique des caractères
Physique-chimie 1
MP
4 heures Calculatrice autorisée
2021
La ruée vers l'or
---- Introduction!
Les nanoparticules sont des objets dont les trois dimensions sont inférieures à
100 nm. Ces nano-objets se
situent donc au confluent des échelles macroscopique (matériaux massifs) et
moléculaire (ou atomistique). D'un
point de vue fondamental, l'étude des nanoparticules apparaît essentielle afin
d'élargir notre compréhension
de la matière. Toutefois, l'intérêt de la communauté scientifique pour les
nanoparticules ne s'arrête pas là. En
effet, ces nanomatériaux présentent des propriétés particulières et originales
attribuables à des effets de taille.
Ainsi, certaines nanoparticules semi-conductrices (quantum dots) présentent un
élargissement de l'écart entre les
bandes de valence et de conduction lorsque leur taille décroît, leur conférant
des propriétés optiques originales.
Les nanoparticules de métaux nobles (Au, Ag, Pt) montrent une forte bande
d'extinction dans le domaine visible
(bande plasmon).
En outre, ces objets nanométriques sont assimilables à des briques de base vers
la construction de dispositifs fonc-
tionnels de tailles micrométriques. On note leur utilisation dans des domaines
aussi divers que la santé (crèmes
solaires, cosmétiques..), la biologie, le photovoltaïque, le stockage de
l'information, l'imagerie, l'électronique ou
encore la catalyse.
Les nanoparticules d'or
Les suspensions de nanoparticules d'or (« or colloïdal ») sont connues depuis
l'Antiquité pour leur couleur rouge
intense. Elles ont été notamment utilisées pour la coloration d'objets en verre
[...]. La coloration rouge rubis
des vitraux de la cathédrale de Chartres est due à la présence de
nanoparticules d'or. L'étude scientifique
de ces nanoparticules a débuté avec les travaux de Michaël Faraday au milieu du
xIx° siècle et elles sont
à l'heure actuelle l'objet d'un intérêt scientifique intense et présentent
plusieurs applications prometteuses.
Parmi ces applications, on peut citer la dépollution, notamment la catalyse par
les nanoparticules d'or de la
transformation du monoxyde de carbone CO en dioxyde de carbone CO ainsi que des
applications en biologie
(agents de contraste pour localiser des cellules cancéreuses et thérapie par
hyperthermie). Les propriétés optiques
des nanoparticules d'or dépendent fortement de leur taille, de leur forme, de
leur état d'agrégation et de leur
environnement local.
Ce sujet propose l'étude de quelques propriétés physico-chimiques des
nanoparticules d'or. La première partie
illustre le rôle que peuvent jouer les nanoparticules d'or dans le domaine de
la catalyse pour la dépollution
des gaz. Dans la seconde partie, on propose une étude de l'imagerie des
nanoparticules d'or en lien avec leurs
propriétés thermiques. Les deux dernières parties abordent la modélisation de
la réponse d'une nanoparticule
d'or à une excitation électromagnétique.
Un ensemble de valeurs numériques et un formulaire sont disponibles en fin
d'énoncé et doivent impérativement
être lus avant de commencer à traiter le sujet.
À toute grandeur sinusoïdale réelle de pulsation w, fonction du temps #, de la
forme a(t) = à cos(wt -- +), où
à et sont deux constantes, on fait correspondre une grandeur complexe a(w) =
àäexp(i(wt -- $)), appelée
représentation complexe de la grandeur a(t).
Certaines questions, peu ou pas guidées, demandent une prise d'initiative de la
part du candidat. Elles sont
signalées par une barre dans la marge gauche. Il est alors demandé d'expliciter
clairement la démarche de
résolution, les hypothèses effectuées et d'illustrer le raisonnement, le cas
échéant, par des schémas. Le barème
valorise la prise d'initiative et tient compte du temps nécessaire à la
résolution de ces questions. Les résultats
établis dans ces questions ne sont toutefois pas indispensables pour le
traitement des autres questions du
problème.
De façon plus générale, le candidat est amené à expliciter toutes les
hypothèses et initiatives qu'il est amené à
prendre, y compris en dehors de ces questions.
P039/2021-02-10 06:41:54 Page 1/10 CHELLES
I Utilisation des nanoparticules d'or en catalyse hétérogène
La combustion du carburant dans un moteur thermique automobile conduit à la
formation de monoxyde de
carbone, gaz toxique inodore et incolore. Le pot catalytique vise à réduire la
nocivité des gaz d'échappement.
Le monoxyde de carbone y est oxydé en dioxyde de carbone au contact d'éléments
catalyseurs qui contiennent
des métaux nobles comme le platine, le palladium ou le rhodium.
Jusqu'à la fin des années 1980, l'or était considéré comme un métal inactif en
catalyse, contrairement aux autres
métaux nobles précédemment cités. C'est en 1987 qu'une équipe de recherche
japonaise a mis en évidence non
seulement les propriétés de catalyse remarquables de nanoparticules d'or de
taille inférieure à 5 nm dans la
réaction d'oxydation du monoxyde de carbone, mais aussi que l'or était le seul
métal capable de catalyser cette
réaction à température ambiante, voire à plus basse température.
IA -- Influences de la température, de la pression et de la composition du
mélange gazeux sur
l'oxydation du monoxyde de carbone
On étudie l'équilibre chimique résultant de l'oxydation du monoxyde de carbone
par le dioxygène. Toutes les
espèces chimiques considérées sont en phase gazeuse à la température T'et à la
pression totale P fixées et sont
assimilées à des gaz parfaits.
Q 1. Ecrire l'équation de la réaction qui modélise l'oxydation en phase gazeuse
du monoxyde de carbone
en dioxyde de carbone en se ramenant à une mole de dioxygène.
Q 2. Calculer la valeur de la constante thermodynamique K°(T') de cet équilibre
chimique dans le cas
particulier où T° = 298 K.
Q 3. L'état initial est constitué d'un mélange idéal de monoxyde de carbone et
de dioxygène gazeux seule-
ment. On définit la proportion initiale de dixoygène par le paramètre ©, égal
au rapport de la quantité initiale de
dioxygène sur la quantité initiale de monoxyde de carbone. On définit aussi le
taux de conversion du monoxyde
de carbone comme étant la quantité de monoxyde de carbone qui a réagi,
rapportée à la quantité initiale de
monoxyde de carbone. On le note a.
Établir la relation qui lie le taux de conversion du monoxyde de carbone à
l'équilibre a. à la constante ther-
modynamique d'équilibre K°(T) à la température T, à la pression totale P du
mélange gazeux, à la pression
standard P° et à la proportion initiale de dioxygène o.
Q 4. Indiquer quelles sont les conditions de température et de pression qui
favorisent l'oxydation du mo-
noxyde de carbone. Dans ces conditions, discuter de l'intérêt d'utiliser un
catalyseur.
a?(1 + ao -- a/2)
A a)? TD) en fonction de «
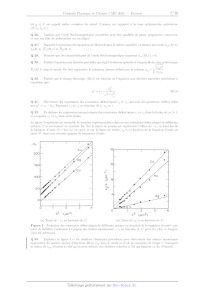
Le graphe de la figure 1 représente les variations de la fonction F: ah
pour différentes valeurs de ©, dans une échelle semilogarithmique.
101 = 7
= li
_-- / !
-- /
3 / gd O -- 0,2
10 = , 4
= Pt o = 0,5
1 / "
-- D LL | O -- 1,0
' /
10? -- ou -- -- = 5 Û
= °T
= = A | og = 10,0
cu + D A
1 Le DA
10 = 27 AT
= TT AT
1 T7 AT
_ | | _eT 277
0 et 27 TT
10 = . et et TT
= | et eT TT
E ee 077 TT
| | D PTT
10 | | | |
0,0 0,2 0,4 0,6 0,8 1,0
Taux de conversion a
Figure 1
Q 5. Indiquer comment il convient de choisir la proportion initiale de
dioxygène © pour favoriser l'oxydation
du monoxyde de carbone.
P039/2021-02-10 06:41:54 Page 2/10 (C2) 8Y-Nc-sA |
I.B --- Modèle de Langmuir de l'adsorption
La catalyse de l'oxydation du monoxyde de carbone par des nanoparticules d'or
fait intervenir une étape
d'adsorption (plus précisément de chimisorption) au cours de laquelle les
molécules de monoxyde de carbone
viennent se lier, par liaison chimique, à certains sites d'adsorption sur la
surface d'une nanoparticule. Un site
d'adsoprtion lié à une molécule de monoxyde de carbone est qualifié d'occupé,
par opposition à un site vacant.
On propose de déterminer à l'aide d'un modèle de cinétique chimique dans un
premier temps, puis grâce à des
arguments de thermodynamique statistique dans un second temps, la fraction des
sites d'adsorption occupés à
l'équilibre thermodynamique à la température T'en fonction de la pression p en
monoxyde de carbone. Cette
fraction, également appelée taux d'occupation, est notée 0. Elle est égale au
nombre de sites occupés divisé par
le nombre total de sites.
L.B.1) Modèle cinétique
L'adsorption d'une molécule de monoxyde de carbone sur une surface est
modélisée par le processus
ka
CO(g) + S vacant CO --5 ; (L.1)
ka
où un site d'adsorption vacant est noté Sacant EURt un site occupé par une
molécule de monoxyde de carbone
adsorbée est noté CO -- $S. La constante de vitesse de la réaction d'adsorption
est notée k, alors que la constante
de vitesse du processus réciproque, appelé désorption, est notée k,.
On suppose que la vitesse de la réaction d'adsorption est d'ordre 1 par rapport
à la pression partielle en
monoxyde de carbone, notée p, et d'ordre 1 par rapport au taux de sites
vacants. De même, on suppose que la
vitesse de la réaction de désorption est d'ordre 1 par rapport au taux de sites
occupés.
À dé
Q 6. Etablir l'expression de la vitesse d'apparition des sites occupés. d en
fonction de k,, k;, 0 et p.
Q 7. Exprimer 4, lorsque l'équilibre est établi, en fonction du rapport K = k,
/k, des constantes de vitesse
et de la pression p. L'expression obtenue a été établie pour la première fois
par Irving Langmuir, physicien
et chimiste américain, récipiendaire du prix Nobel de chimie en 1932 pour ses
travaux en physico-chimie des
surfaces.
I.B.2) Modèle statistique
On propose de retrouver l'expression du taux d'occupation, établi à la question
7 précédente, à l'aide d'arguments
de thermodynamique statistique. Pour cela, on considère l'ensemble des N sites
d'adsorption et des molécules
de monoxyde de carbone, à la pression p et à la température 7, supposées
maintenues constantes. L'énergie
d'un site vacant est choisie arbitrairement nulle, alors que l'énergie d'un
site occupé est notée --£EUR avec EUR > 0.
La probabilité d'occupation d'un site est donnée par le facteur de Boltzmann.
Tous les sites sont indiscernables.
Une configuration microscopique du système étudié est définie par le nombre n
(0 < n < N) de sites occupés. On pose 5 = 1/(k21') où kk est la constante de Boltzmann. Q 8. Donner l'expression de l'énergie E(n) associée à une configuration microscopique où n sites, parmi les N, sont occupés. On note g, le nombre de réalisations de cette configuration microscopique. Exprimer g,, en fonction de n et N. On définit la fonction de partition Z comme étant la quantité : N 2 = Y 9, exp(-BE(n)). (2 n=Û0 Q 9. Donner l'expression de la probabilité P(n) que le système soit dans une configuration où n sites sont occupés, en faisant intervenir Z, g, et le facteur de Boltzmann. Q 10. On note {n) le nombre moyen de sites occupés à l'équilibre thermodynamique. Montrer qu'on peut le 10nZ calculer ainsi : (n) = -- n Q 11. Établir l'expression du taux d'occupation 0 à l'équilibre thermodynamique en fonction de la pression p du monoxyde de carbone sachant qu'une étude plus approfondie permet d'établir que le facteur exp(fe) est proportionnel à la pression p. Par comparaison avec le résultat établi à la question 7, proposer une expression du coefficient de proportionnalité. P039/2021-02-10 06:41:54 Page 3/10 (C2) BY-Nc-SA | I.B.3) Confrontation de mesures expérimentales au modèle de Langmuir La figure 2 représente des mesures d'adsorption du monoxyde de carbone sur des nanoparticules d'or : le taux d'occupation Ô est représenté en fonction de la pression p en monoxyde de carbone à température ambiante fixée. On cherche à modéliser ces données par le modèle de Langmuir qui fournit l'expression de 0 en fonction de p obtenue aux questions 7 et 11. 1 U p(Pal 6 Îp(Pal 6 5,6 | 0,06 || 91,7 | 0,35 0,6 ° 11,1 | 0,09 || 130,5 | 0,43 | + 16,7 | 0,15 || 266,6 | 0,50 0,4 ? 25,0 | 0,17 || 533,3 | 0,59 9 38,9 | 0,23 || 799,9 | 0,64 0.2 À 50,0 | 0,28 |11066,6| 0,71 | 63,9 | 0,26 |[1336,0| 0,79 0 0 200 400 600 p (Pa) Figure 2 'Taux d'occupation 0 de la surface du catalyseur (nanoparticule d'or) en fonction de la pression p en monoxyde de carbone, à température ambiante' Q 12. On choisit de modéliser les données expérimentales données dans la figure 2 à l'aide du modèle de Langmuir. Estimer une valeur approchée du rapport K des constantes de vitesse compatible avec les mesures dans la limite des faibles pressions. Expliquer de façon argumentée (en s'appuyant par exemple sur une représentation graphique) si cette valeur permet d'accorder le modèle de Langmuir avec les mesures réalisées aux plus hautes pressions. IT Imagerie des nanoparticules d'or Les nanoparticules sont trop petites pour être visualisées avec un microscope. Des techniques d'imagerie indirecte sont donc développées pour les détecter. Une équipe de l'université Bordeaux 1 à mis au point il y a une quinzaine d'années une technique de microscopie photothermique qui permet de détecter et de localiser, dans un échantillon, des particules d'or dont le rayon n'excède pas quelques nanomètres. Une étape de ce protocole consiste à chauffer la particule par un faisceau laser et fait l'objet de cette partie. On considère une sphère d'or, de rayon a = 10 nm, immobilisée dans un gel constitué très majoritairement d'eau, et chauffée par un faisceau laser. Le milieu (le gel) entourant la sphère est considéré comme homogène, infini et initialement à la température 71,. On note k la conductivité thermique du milieu et EUR, sa capacité thermique volumique. On supposera que, dans le domaine de températures exploré, ces grandeurs sont indépendantes de la température. On note P,..(t) la puissance totale absorbée par la sphère et C'\,, la capacité thermique volumique de l'or. Compte tenu de la taille de la nanosphère, on admet que sa température est partout égale à sa température de surface, que l'on note 7°.(t). On suppose que le contact thermique entre le gel et la nanoparticule est parfait donc que T(a*,t) =T,(t). II.A --- Équation de la diffusion thermique en géométrie sphérique Q 13. Montrer, à l'aide d'un argument simple, que la température T'en un point du milieu ne dépend spatialement que de r, distance séparant le centre de la nanosphère du point considéré. Q 14. Effectuer un bilan énergétique entre t et t + dt pour un système bien choisi et établir l'équation aux dérivées partielles vérifiée par la température T(r,t) dans le milieu : OT K Ô OT Co --(r,t) = ---- =) t). IL.1 De 357 ( or) (0 A) Page 4/10 CEE P039/2021-02-10 06:41:54 Cette équation se met sous la forme (le calcul n'est pas demandé) : OT K O°(rT) C--(r,t) = -- r,t). g 5e ) Tr. Or? (7,8) IT.B --- Température dans le milieu en régime stationnaire On se place en régime stationnaire, c'est-à-dire que les températures de la sphère et du milieu ne dépendent pas du temps. Q 15. Établir l'expression de la température T (r) dans le milieu en fonction de a, r, T, et T°. Q 16. En déduire l'expression de la puissance fournie par la nanosphère au milieu extérieur, P fonction de a, k et 07, = T, -- 7, sous la forme : ph-- milieu? en P sph-- milieu -- ATakÔT,.. ITI.C --- Température de surface de la nanosphère On suppose maintenant que l'intensité du faisceau laser chauffant la nanosphère d'or est modulée sinusoïdale- ment, la puissance absorbée par la sphère étant donnée par : Payet) = P(1 + cos(Qt)) à où P, est une constante positive. On admet que l'expression de P. établie à la question 16 est valable même en régime variable. ph-- milieu Q 17. En effectuant un bilan énergétique pour la nanosphère entre t et & + dt, établir l'équation différentielle vérifiée par 01.(t) et la mettre sous la forme : OT". (É -- (+7 dt ATrKka où 7 est une constante dont on donnera l'expression en fonction des données du problème et dont on vérifiera qu'elle est bien homogène à un temps. Q On donne F, = 0,375 nW et 2x -- 700 kHz. T Q 18. Justifier que la température 7°.(t) se met sous la forme approchée : P Ti(t) = To + Ta (1 + cos(Qt)) . Q 19. Donner l'expression de l'élévation moyenne ÔT.. de la température de la surface de la sphère et calculer sa valeur. IT.D --- Température du gel autour de la sphère On admet que la solution de l'équation de la diffusion thermique dans le gel s'écrit : T(r,t) =T, + © (: + EXP (---) COS (ar - --)) , r th th 2K QC. q où «à est une constante réelle et r,} = Q 20. Interpréter physiquement la constante 7? et citer un autre domaine de la physique où l'on rencontre th une situation similaire. Q 21. Établir l'expression de la constante a en fonction de Fy et K. Q 22. En considérant que a & r,, déterminer l'expression de l'élévation moyenne ÔT = (T(r,t) -- 15) de la température du milieu contenu dans une sphère de rayon r,, autour de la nanoparticule, la moyenne étant effectuée sur le temps puis sur le volume de la sphère de rayon r,,. L'exprimer en fonction de a, r,, et de Ô7, (voir question 19). Évaluer numériquement ÔT! Q 23. Proposer une technique permettant de révéler les variations faibles de l'indice optique du gel induites par cette variation de température. P039/2021-02-10 06:41:54 Page 5/10 (C2) BY-Nc-SA | III Propriétés optiques du métal or On souhaite modéliser les propriétés optiques de l'or à l'état métallique à l'aide du modèle de Drude. Pour ce faire, on considère que le métal est composé d'un ensemble d'ions supposés fixes, qui constituent le réseau cristallin, et d'un gaz d'électrons libres de se déplacer sur des distances très largement supérieures aux distances interatomiques. Chaque électron porte la charge --e et possède une masse notée m,.. En l'absence d'excitation électromagnétique extérieure, l'état du métal est stationnaire et qualifié d'état de repos. Il est désigné par les grandeurs physiques suivantes, indicées par 0, indépendantes du temps. Les champs électrique et magnétique au repos, en un point M, sont identiquement nuls : E(M ) = O et B,(M ) = Ü. Les électrons sont animés d'un mouvement d'agitation thermique, mais la vitesse moyenne des électrons qui se situent au voisinage d'un point M est nulle : ü(M) -- Ü. Au repos, le métal est électriquement neutre à l'échelle locale : le nombre moyen d'électrons par unité de volume est égal au nombre moyen d'ions par unité de volume. On note n,, le nombre moyen d'électrons par unité de volume dans l'état de repos du métal, supposé uniforme. La propagation d'une onde électromagnétique vient perturber localement l'état de repos du métal. On suppose que cette perturbation est d'amplitude suffisamment faible pour que les différentes grandeurs physiques puissent s'écrire comme la somme de la valeur de cette grandeur au repos, indicée par 0 et d'une valeur perturbée, indicée par le chiffre 1. Aïnsi, le champ électrique, le champ magnétique, le champ de vitesse des électrons et le nombre moyen d'électrons libres par unité de volume s'écrivent respectivement comme suit : E(M,t) = E(M)+E,(M,t) =0+E (M,t), B(M.,t) = B(M) + B,(M,t) =0+B,(M,t), ü(M,t) = do(M) +, (M,t) =0+%,(M,t), NM t) = neo + Ne1( Mit). Les grandeurs E,(M,t), B.(M,t), ü,(M,t) et n.,(M,t) sont associées à la propagation de l'onde électromagné- tique dans le milieu. Leurs amplitudes respectives sont supposées suffisamment faibles pour qu'on se limite à un traitement linéaire : tous les calculs se limiteront à des termes qui s'expriment au premier ordre vis-à-vis des amplitudes indicées par le chiffre 1. Ci-dessous est présenté un exemple de linéarisation au premier ordre du produit de deux grandeurs a(M,t)b(M,t) où le terme du second ordre est finalement négligé : a(M,t)b(M,t) = (ao + a(M,t))(b +b,(M,t)) -- apbo + ob (Mt) + ba, (Mt) +a,(M,t)b,(M,t) ordre 0 ordre 1 ordre 2 négligeable = 4606 + aob1(M;t) + bou (Mt). III. A --- Mouvement des électrons libres On s'intéresse dans un premier temps au mouvement des électrons libres. Le gaz d'électrons libres est assimilé à un fluide. On note respectivement m, et --e la masse et la charge électrique d'un électron. On suppose qu'en plus de la force d'interaction avec le champ électromagnétique de l'onde, les électrons sont soumis à une force EUR dissipative qui modélise leurs interactions avec le réseau cristallin : ----%,(M,t). Le mouvement des électrons est supposé non relativiste (|ü,| < EUR, où c est la célérité de la lumière dans le vide). Dans l'approximation linéaire, l'équation du mouvement des électrons se met sous la forme approchée OÙ, me LE) = --eEi (M6) -- Teÿ (Mt). (IIL.1) T Q 24. Expliquer pourquoi, compte tenu des hypothèses retenues, la composante magnétique de la force exercée par l'onde électromagnétique sur les électrons n'apparaît pas dans l'équation du mouvement (IIL.1). Q 25. Exprimer, dans l'approximation linéaire, la densité volumique de courant électrique 7,(M,t) dans le métal en fonction, entre autres, de la vitesse moyenne des électrons ü, (M ,t), puis établir l'équation différentielle liant 7,(M,t) et E,(M,t). ITI.B --- Relation de dispersion On suppose que le métal est soumis à une onde électromagnétique, harmonique de pulsation w, dont le champ électrique s'écrit ainsi en notation complexe : _, _ | w \ E (Mt) = E; exp (it -- n=x)) ê U 1 (IIL.2) P039/2021-02-10 06:41:54 Page 6/10 (C2) BY-Nc-SA | où n EUR C est appelé indice complexe du métal. L'espace est rapporté à la base orthonormée cartésienne (O;é,,EUR,,EUR,). Q 26. Justifier que l'onde électromagnétique considérée peut être qualifiée de plane, progressive, transverse et que son état de polarisation est rectiligne. Q 27. Rappeler l'expression des équations de Maxwell dans le milieu considéré, en faisant intervenir n,.(M,,t), ni (M, t), E,(M. t) et B;(M, t). Q 28. Montrer que les caractéristiques de l'onde électromagnétique imposent n,,(M,t) = 0. Q 29. Établir l'équation aux dérivées partielles qui régit l'évolution spatiale et temporelle du champ électrique _ nee E,(M,t) dans le métal. On fera apparaître la pulsation plasma définie par la relation w, -- 0. MmeEo Q 30. Établir que le champ électrique (IIL.2) est solution de l'équation aux dérivées partielles précédente à condition que : n° =1---E.-., (IIL.3) rie Q 31. Déterminer les expressions des constantes diélectriques EUR, et £, (qui sont des grandeurs réelles) telles 2 que n° -- EUR, --ie,. Exprimer EUR; et & en fonction de w, w, et 7. Q 32. En déduire les expressions asymptotiques des constantes diélectriques EUR, et £ dans la limite où wr > 1,
et comparer EUR, et #, dans cette limite.
La figure 3 représente un ensemble de données expérimentales relatives aux
constantes diélectriques de différents
métaux. L'or correspond au symbole Au. Sur la figure de gauche est représentée
l'allure de --£, en fonction de
la longueur d'onde (À = 2rc/w) au carré, et sur la figure de droîte, EUR,/À en
fonction de la longueur d'onde au
carré }?, dans une certaine gamme de longueurs d'onde.
16
200
- a
cu °
150 12 T --
ii a
100 E Au
z 8f ® s
< = L. È 50 SN / " a}- da à 0 L. ° 4 | | | O 1 2 3 4 ie l D O 1 2 3 4 À (um?) A? (um?) (a) Tracé de --EUR, en fonction de X° (b) Tracé de &,/X en fonction de X. Figure 3 Évolution des constantes diélectriques de différents métaux en fonction de la longueur d'onde* ; par souci de lisibilité, l'ordonnée à l'origine des droites représentant --EUR, en fonction de À? pour l'or (Au) et l'argent (Ag) est arbitraire Q 33. Exploiter la figure 3 et les résultats théoriques précédents pour déterminer des valeurs numériques approchées du nombre moyen d'électrons libres n.,9 dans le métal or et de la constante de temps 7. Comparer la valeur de n,, obtenue à celle qu'on peut déduire des données relatives à l'or qui figurent en fin d'énoncé. P039/2021-02-10 06:41:54 Page 7/10 (cc) BY-NC-SA IV Résonance plasmon des nanoparticules d'or IV.A - Pulsation propre d'une nanoparticule d'or ---- Les nanoparticules d'or! Lorsqu'une particule métallique est soumise à un champ électromagnétique dont la longueur d'onde À est beaucoup plus grande que la taille des particules, tous les électrons libres subissent le même champ et oscillent collectivement et en phase. En effet, lorsque le nuage d'électrons est déplacé par rapport aux noyaux métalliques par interaction avec le champ électrique, il se crée une force de rappel due à l'attraction coulombienne entre noyaux et électrons (figure 4). Lorsque la fréquence de l'onde incidente correspond à la fréquence propre de ces oscillations, il se produit un phénomène de résonance, appelé résonance de plasmon de surface. Ei Réseau cris- tallin Nuage élec- tronique Figure 4 Représentation schématique des oscillations de plasmon pour une nanoparticule sphérique, montrant le déplacement des élec- trons libres par rapport au réseau cristallin des noyaux métalliques La fréquence de résonance plasmon dépend de la nature du métal. Elle a lieu dans le domaine du visible, seulement pour l'or, le cuivre et l'argent, d'où la coloration particulière de ces nanoparticules. Si la particule est sphérique et beaucoup plus petite que la longueur d'onde (rayon < quelques dizaines de nanomètres) alors la position de la résonance plasmon est indépendante de la taille de la particule |...]. Elle dépend alors des propriétés du métal et du milieu environnant. Ainsi, des nanoparticules d'or de 20 nm ont une bande de résonance plasmon vers 520-530 nm (absorption dans le vert) et sont rouges. L'or sous forme de nanoparticules perd donc sa couleur dorée si caractéristique. Pour interpréter le rappel du nuage des électrons libres et en déduire une expression de la pulsation propre { de son mouvement d'oscillation, il faut s'intéresser à la séparation des charges électriques qui résulte du déplacement de ce nuage électronique. La figure 4 suggère qu'on peut modéliser cette distribution de charges électriques par la superposition de deux boules, de même rayon À, qu'on peut considérer uniformément chargées en volume, l'une correspondant au nuage des électrons libres, l'autre au réseau cristallin des noyaux métalliques, et dont le décalage est donné par le vecteur r(t). Ce déplacement reste bien inférieur au rayon À de la nanoparticule. Q 34. Déterminer une expression du champ électrostatique à l'intérieur de la nanoparticule, qui résulte du déplacement du nuage électronique par rapport au réseau cristallin. Commenter le résultat obtenu. IV.B - Modélisation de la réponse d'une nanoparticule à une excitation électromagnétique On considère une nanoparticule d'or sphérique, de rayon À, placée dans le vide. En première approche, on . | . | | A | assimile son nuage électronique à un oscillateur harmonique, de masse égale à TA n.om., et de pulsation propre ( = wp/V3 excité par le champ électrique d'une onde électromagnétique incidente. On note E,(O, t) le champ électrique de cette onde au centre © de la nanoparticule, à l'instant t. On admet que ce centre se confond avec le centre du réseau cristallin, considéré comme fixe dans le référentiel d'étude. On suppose également que le champ électrique est uniforme à l'échelle de la nanoparticule. Q 35. Justifier que l'équation différentielle vérifiée par le vecteur déplacement r(t) du nuage électronique par rapport au centre © de la nanoparticule s'écrit sous la forme d'r(t) . e -- de. + Q2r(#) -- -- Æ1(0.#) . EUR -- On se place désormais en régime sinusoïdal forcé où E,(O,t) = Ë, cos(wt -- p)é, où ÿ est une constante. Q 36. Déterminer l'expression de la représentation complexe du déplacement 7 en régime sinusoïdal forcé en fonction, entre autres, de £., représentation complexe du champ électrique de l'onde incidente. P039/2021-02-10 06:41:54 Page 8/10 (C2) BY-Nc-SA | Q 37. En déduire l'expression du moment dipolaire électrique » de la nanoparticule en fonction de E sous la forme -- D -- Eoa(w)E, . Q 38. Expliciter la polarisabilité complexe a(w) en fonction de w, Q, w, et R. Préciser la dimension du module |a(w)| de la polarisabilité complexe. La polarisabilité complexe de la nanoparticule traduit sa réponse à une excitation électromagnétique sinusoïdale extérieure. Q 39. Étudier et interpréter qualitativement le comportement de |[a(w)| en fonction de la pulsation w. Indi- quer quelle modification principale entraîne la prise en compte d'effets dissipatifs dans le mouvement du nuage électronique. Un modèle plus précis, tenant à la fois compte du caractère dissipatif du mouvement du nuage électronique et de l'indice optique nr, du milieu transparent dans lequel se trouve la nanoparticule d'or, conduit à l'expression suivante de la polarisabilité complexe : 2 _ y? T où n° est l'indice complexe de l'or au carré, donné par la relation (IIL.3). On montre aussi que la puissance électromagnétique absorbée par une nanoparticule d'or est proportionnelle à la valeur absolue de la partie imaginaire de sa polarisabilité complexe a(w). Q 40. Vérifier que la relation (1V.1) est compatible avec l'expression, déterminée à la question 37, de la polarisabilité complexe d'une nanoparticule placée dans le vide lorsqu'on néglige les phénomènes dissipatifs (wr > 1).
Q 41. Calculer la valeur de la longueur d'onde principalement absorbée par des
nanoparticules d'or présentes
dans le verre d'un vitrail (no = 1,5). Conclure quant à la couleur par
transmission des vitraux de la cathédrale
de Chartres mentionnés dans l'introduction du sujet.
Données et formulaire
Constantes physiques
Masse de l'électron m, = 9,11 x 10 kg
Charge élémentaire e = 1,60 x 10 C
Permittivité diélectrique du vide En = 8,85 x 10 À Fm !
Célérité de la lumière dans le vide c = 3,00 x 10° mes !
Constante des gaz parfaits R =8,31J-K !'mol !
Données thermodynamiques à 298 K
O:(8) CO(g) CO:(8)
Enthalpie standard de formation À H° (kJ:mol") --110,6 --393,5
Entropie molaire standard S° (J-K-!-:mol 1) 204,8 197,6 213,7
P039/2021-02-10 06:41:54 Page 9/10 (C2) BY-Nc-SA |
Données relatives à l'or
Symbole de l'élément chimique or Au
Type de réseau cristallin cubique à faces centrées
Rayon atomique 135 pm
Configuration électronique à l'état fondamental Xe] 6s! 4ff# 5410
Capacité thermique volumique Cu = 2,5 x 106 J-K°l:m *
Données relatives au gel (partie II)
Conductivité thermique du gel Kk = 0,6 W-m !K !
capacité thermique volumique C, = 42 X 106 J-K-!l:m
Formulaire
rot(rot À) = grad(div A) -- AA
Tv
oe+y)" =) Sy
n
TL
k=0 k
ee erINesee
1 D'après l'article Synthèse et détermination de la taille de nanoparticules
d'or, par J. Piard et al. Bulletin de l'Union des
Physiciens, vol. 107, mars 2013.
2 Données extraites de : H. Hartshorn, C.J. Pursell, B.D. Chandler (2009).
Adsorption of CO on supported gold nanoparticule
catalysts: a comparative study. Journal of Physical Chemistry ©, 113 (24),
10718-10725.
3 D'après P.B. Johnson et R.W. Christy, Optical constants of the noble metals,
Phys. Rev. B 6, 4370 (1972).
P039/2021-02-10 06:41:54 Page 10/10 CHETES
