Centrale Physique et Chimie 1 MP 2019
| Thème de l'épreuve | Vie et mort d'un photon |
| Principaux outils utilisés | mécanique, physique quantique, ondes, électronique |
| Mots clefs | photon, cavité, atomes de Rydberg, faisceau gaussien, circuits couplés |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
Énoncé complet
(télécharger le PDF)








Rapport du jury
(télécharger le PDF)



Énoncé obtenu par reconnaissance optique des caractères
Physique-chimie 1
MP
4 heures Calculatrice autorisée
2019
Vie et mort d'un photon
Dans la plupart des expériences, la mesure de la présence d'un photon se fait
par absorption, c'est-à-dire par
destruction du photon: un oeil ou une caméra CCD détruisent les photons
incidents en les absorbant. De
nombreux travaux ont toutefois permis de réaliser des mesures quantiques non
destructives (QND, quantum
non-demolition measurement). Ainsi, à la fin du xx° siècle, la présence d'un
photon a pu être détectée sans que
celui-ci ne soit détruit, ouvrant la porte à des mesures successives de l'état
du même photon.
L'équipe de Serge Haroche de l'École Normale Supérieure de Paris a en
particulier utilisé ses connaissances en
électrodynamique quantique en cavité (CQED, cavity quantum electrodynamics)
pour mesurer sans le détruire
l'état d'un seul photon piégé. Pour la première fois, l'apparition et la
disparition du même photon ont pu être
observées en direct.
Figure 1 Principe de l'expérience d'électrodynamique quantique en cavité
(Exploring the Quantum - Atoms, cavities and photons - Serge Haroche et Jean-
Michel Raimond - Oxford University Press (2006))
Dans cette expérience, le photon est piégé dans une cavité C constituée de deux
miroirs en vis-à-vis (figure 1). Le
photon effectue des allers-retours entre les deux miroirs jusqu'à sa
disparition (absorption par l'un des miroirs
ou fuite hors de la cavité).
Pour sonder la présence du photon, on utilise un atome de Rubidium sortant du
four © dont la vitesse est
sélectionnée grâce aux lasers L; et L'. L'atome est ensuite excité dans un état
dit de Rydberg circulaire au niveau
de B. L'atome subit ensuite une impulsion micro-onde au niveau de R;, ce qui le
place dans une superposition
de deux états. En traversant la cavité C, les deux états acquièrent un
déphasage relatif &,, dépendant de la
présence ou non d'un photon. L'atome subit une deuxième impulsion micro-onde au
niveau de À, et son état
final est mesuré par le détecteur D. Cet état final dépend du déphasage relatif
®,, et donc de la présence ou non
du photon. Celui-ci n'a pas été absorbé par l'atome, mais à seulement induit un
déphasage dans la structure
électronique de l'atome.
L'équipe de Serge Haroche a par la suite généralisé la mesure non destructive à
un nombre de photons supérieur
à un et à utilisé cette technique pour réaliser une expérience de chat de
Schrôdinger, ce qui a entre autres
valu à Serge Haroche l'obtention du prix Nobel de physique en 2012. Dans le
cadre de ce sujet, nous ne nous
intéresserons toutefois qu'à certains aspects de l'expérience décrite sur la
figure 1.
La partie I étudie quelques propriétés des atomes de Rubidium excités dans
l'état de Rydberg (on parle alors
d'atomes de Rydberg) ainsi que leur détection. La partie IT s'intéresse aux
propriétés de la cavité permettant de
piéger un photon pendant une durée suffisante. La partie IIT étudie le couplage
entre un atome de Rydberg et
un photon de la cavité. Les trois parties sont indépendantes, même si le
contexte reste celui de l'expérience de
la figure 1.
Des données numériques, un formulaire et une annexe sont présents en fin de
sujet.
2019-05-10 12:11:14 Page 1/11 CHELLES
Certaines questions peu ou pas guidées, demandent de l'initiative de la part du
candidat. Leur énoncé est repéré
par une barre en marge. Il est alors demandé d'expliciter clairement la
démarche, les choix et de les illustrer,
le cas échéant, par un schéma. Le barème valorise la prise d'initiative et
tient compte du temps nécessaire à la
résolution de ces questions.
I Étude des atomes de Rydberg circulaires
Les atomes utilisés dans l'expérience sont des atomes de Rubidium dont
l'électron situé sur la couche électronique
la plus énergétique est excité dans un état de nombre quantique principal n
très élevé. Des atomes ainsi excités
sont appelés atomes de Rydberg. Si de plus le nombre quantique secondaire £ de
l'électron excité est maximum,
alors on parle d'atomes de Rydberg circulaires.
I.A --- Préliminaires
Q 1. Donner la structure électronique du Rubidium (Z = 37) dans son état
fondamental. Entourer le ou
les électron(s) de valence. À quelle famille cet élément appartient-il ?
Considérons un atome polyélectronique contenant Z électrons. Le noyau sera
considéré comme ponctuel et fixe
en ©. On s'intéresse à l'électron de la couche électronique la plus énergétique
que l'on repère en coordonnées
sphériques. L'énergie potentielle électrostatique de cet électron est de la
forme
Z(r)q
Ur) = =
2
e
où l'on a posé q -- n avec EUR, la permittivité diélectrique du vide. La
fonction Z{(r) est positive et vérifie
TE)
Z(r -- 0) =Zet Z(r -- +oo) = 1.
Q 2. Justifier le signe de U(r.).
Q 3. Interpréter physiquement les valeurs limites de la fonction Z{(r) en r --
0 et r -- +oo.
Q 4. On cherche un ordre de grandeur de la taille typique a, de l'atome. On
estime que a, est de la forme
Gp = h° q°mn? où m, est la masse de l'électron. Établir soigneusement que a =
2, 8 = --1et y = --1. La grandeur
a, est appelée rayon de l'atome de Bohr, calculer sa valeur numérique.
I.B --- Atomes de Rydberg
L'électron le plus énergétique de l'atome précédent est excité dans un niveau
de nombre quantique n > 1
(typiquement n = 50), le reste de l'atome étant inchangé. On étudie par la
suite le comportement de cet
électron dont la masse est toujours notée m,. L'atome est isolé de son
environnement extérieur.
I.B.1) Étude classique
Q 5. Justifier que l'énergie potentielle de l'électron est alors : U(r) = 1
Tr
Q 6. Démontrer que le moment cinétique £ de cet électron est constant et en
déduire que le mouvement
de l'électron est plan. On introduit le repère sphérique (r,0,%) tel que £ =
Le, avec £ > 0. Le noyau est
toujours à l'origine du repère. Montrer que le mouvement de l'électron est
alors situé dans le plan Oxy et
donner l'expression de la constante Z en fonction de m,, r et ç.
Q 7. Que peut-on dire de l'énergie mécanique EUR,, de l'électron ? Montrer que
l'on peut mettre cette énergie
mécanique sous la forme
1
Em = Mi + Cpetr(r)
7 2
où l'on exprimera &,,.g(r) en fonction de q, r, m, et £.
Q 8. Justifier que, pour une trajectoire circulaire, Eper(r) est minimale. En
déduire la valeur du rayon re
de l'électron lorsqu'il est sur une trajectoire circulaire. On exprimera r,; en
fonction de £, m, et q, puis on
£L?
vérifiera que ro = 72 0:
I.B.2) Étude quantique
En physique quantique, l'état de l'électron excité dans le niveau n est décrit
par la fonction d'onde Y(M,t).
Celle-ci vérifie l'équation de Schrôdinger
2
RU = ay Ty
Ot 2m T
EUR
où À est l'opérateur laplacien.
On cherche V(M,t) sous la forme d'un état stationnaire : YW(M,t) = (M)x(t).
2019-05-10 12:11:14 Page 2/11 (C)EATETSS
Et
Q 9. Justifier que x(t) est de la forme Y{t) = A exp (©) avec À et EUR deux
constantes.
Q 10. Justifier sans calcul le signe de EUR pour l'électron étudié.
I
On met P(M) sous la forme P(M) = -u(r)Y (4,4) et on admet que u(r) vérifie
l'équation
T
(- + PU +1) _ 1) u(r) = Eur) (I.1)
2m,7T r
où £ est le nombre quantique secondaire.
Q 11. Rappeler les valeurs permises pour le nombre quantique £.
Q 12. En utilisant notamment la question 7 et en procédant par identification,
justifier qu'en physique
quantique les valeurs possibles de £? sont £(£ + 1)h°. Quelle est en
particulier la valeur maximale que £? peut
prendre pour l'électron étudié ?
Q 13. Que vaut alors le rayon r, de la trajectoire circulaire obtenue en
question 8 ? On donnera le résultat
en fonction de a, et de n pour un atome de Rydberg.
Q 14. On cherche à adimensionner l'équation (1.1). Montrer que cette équation
peut se mettre sous la forme
d' (+1) 2 |
x p° p
en posant p = r/ap et EUR = --E/E,, avec EUR, une constante que l'on exprimera
en fonction de a, et de q. Quelle
est la valeur numérique de EUR, en électron-volts ?
IC --- Atomes de Rydberg circulaires
L'électron le plus énergétique est maintenant placé dans un état de nombre
quantique principal n > 1 et de
nombre quantique secondaire EUR maximum. Sa fonction d'onde spatiale est
D(r,0,w) = A(n) (2 sin 0 ee) exp (=) (L.3)
ap na
avec A(n) une constante réelle positive de normalisation.
Q 15. Exprimer la probabilité dP de trouver l'électron entre r et r + dr,
quels que soient 0 et &. On ne
cherchera pas à calculer les éventuelles intégrales.
dP
Q 16. Montrer que la densité de probabilité dr est maximale pour le rayon r,,,
= n'a. Commenter ce
T
résultat.
Q 17. Faire l'application numérique pour n = 50. Pourquoi qualifie-t-on les
atomes de Rydberg circulaires
d'atomes géants ?
L'expression de la fonction d'onde (non demandée) permettrait en outre de
montrer que la probabilité de
présence est maximale dans la direction 0 = 7x/2. On admet également que la
dispersion relative de r et la
A 1
dispersion de 0 sont de l'ordre de Du AÛ = ----
T
V2n
Q 18. Pourquoi peut-on dire que le comportement de l'électron excité de l'atome
de Rydberg circulaire est
« classique » ?
Q 19. Donner, à partir de la forme de la fonction d'onde (1.3), l'expression de
u(p) pour l'électron le plus
énergétique dans un atome de Rydberg circulaire, à un facteur multiplicatif
constant près. En déduire l'expression
de EUR puis de EUR pour l'électron dans un tel état. Commenter ce résultat.
Q 20. Calculer la fréquence z,, du photon correspondant à la transition entre
les états EUR, _50 et EUR, _51. Dans
quel domaine des ondes électromagnétiques se situe-t-il ?
I.D --- Détection des atomes de Rydberg circulaires
On se reportera aux différents documents de l'annexe pour traiter cette
sous-partie qui est indépendante des
résultats précédents.
Q 21. Considérons tout d'abord un atome d'hydrogène dans son état fondamental.
L''électron est à une
distance moyenne du noyau de l'ordre de 107! m. Donner l'ordre de grandeur de
la norme du champ électrique
créé par le proton au niveau de l'électron. Justifier pourquoi on peut, en
ordre de grandeur, assimiler la valeur
de ce champ électrique à celle du champ d'ionisation de l'atome d'hydrogène.
Q 22. On assimile l'état de Rydberg circulaire n à un atome d'hydrogène dont
l'électron est excité dans le
niveau n > 1. On s'intéresse aux trois états de Rydberg circulaires n = 50, n =
51 et n = 52. Une approche
théorique non détaillée ici permet de calculer les champs d'ionisation des
trois états précédents. Ces champs sont
dans le désordre, en unités du système international, 1,48 X 10°, 1,36 x 10° et
1,60 x 10°. Attribuer à chaque n
son champ d'ionisation en justifiant succinctement.
2019-05-10 12:11:14 Page 3/11 (C)EATETSS
Q 23. Classer les potentiels V,, V,, V., V3, V et V; des différentes électrodes
de la figure 11 dans l'ordre
croissant en justifiant.
Q 24. Estimer la vitesse des atomes de Rydberg dans la zone d'ionisation à
l'aide du protocole I.
Q 25. Dans le protocole 2, la variation de V,(t) suit une loi affine : V,(t) =
V, + K(t--t,) avec V, = 32 V
le potentiel de l'électrode b, t, l'instant initial de déclenchement de la
variation de V,(t) et K° une constante.
Déterminer l'instant de déclenchement t, de la rampe et sa pente X° permettant
d'observer les deux signaux
d'ionisations sélectives de la figure 13 de l'annexe.
Q 26. Quel problème pourrait-on rencontrer si l'on choisissait une variation de
V,(t) plus rapide ? Et plus
lente ?
Q 27. Quelle valeur faut-il prendre pour t,, défini dans le paragraphe «
Principe de la détection » à la fin de
l'annexe ? Quelle(s) cause(s) expérimentale(s) pourraient fausser l'attribution
de l'électron détecté au bon état
de Rydberg ?
II Étude de la cavité micro-ondes
La cavité micro-ondes est constituée de deux miroirs métalliques en vis-à-vis
entre lesquels un photon de longueur
d'onde À, est piégé. Dans un premier temps (sous-partie IL.A) nous allons nous
intéresser aux propriétés d'une
cavité composée de miroirs métalliques plans avant d'aborder le cas des miroirs
sphériques (sous-partie IL.B).
IT. À --- Miroirs plans
Considérons une cavité constituée de deux miroirs plans métalliques (figure 2)
séparés par le vide d'une distance
d -- 26,6 mm. Le coefficient de réflexion r,, en amplitude pour le champ
électrique est identique pour les deux
miroirs. r,, est un réel négatif à la longueur d'onde À, considérée : --1 < rx < 0 et 1--{ryl & 1. 7 Sy RLTOSTTRÈQOT--+ A 24 ' L TT 23 7 S9 TT RÈRQoT TT y 7 -- LRO 8] y S 29 TRÈS TT + 7 - 7 Z O d L 7 Vide L miroir de gauche miroir de droite Figure 2 Cavité plane On se place dans l'approximation scalaire. L'intensité est définie comme 1 = 5 s* où s est l'amplitude complexe de la vibration. Une onde 5, (2: t) = Syexp(ilwt -- kz)) se propage dans la cavité (S, est un réel positif). Elle subit des réflexions multiples dans la cavité. On note s (&:t) l'onde réfléchie sur le miroir de droite, 8, (2:t) l'onde réfléchie sur le miroir de gauche et de manière générale s (2; t) l'onde ayant subi n réflexions. Q 28. Onse place en un point d'abscisse z à l'intérieur de la cavité. Exprimer s .( t) en fonction de s (2: t). Q 29. Exprimer 5, (2; t) en fonction de 5 (2: t) ainsi que 5, (2: t) en fonction de 8 (2; t). On fera intervenir la grandeur ® = 4rd/). Q 30. Simplifier alors l'expression de la somme cohérente des amplitudes complexes des ondes se propa- +00 geant dans le sens des z croissants : s, (2, t) = > 8, (2 t). De même pour la
somme cohérente des amplitudes
p=0
+00
complexes des ondes se propageant dans le sens des z décroissants : s (2,1) = >
Sn Ce: t).
p=0
On admet que l'intensité maximale L,,. de l'onde totale 8, (2: t)+s (z,t) au
niveau d'un de ses ventres dépend
de ® selon l'expression
Î
Luax = _ (IL.1)
1 + M sin°(®/2)
4R
AR)
avec Î,, une constante et M -- où À -- Sr. La dépendance en ® de Z,,, est
tracée en figure 3.
2019-05-10 12:11:14 Page 4/11 (C)EATETSS
Lax
DER
0 --A4r --37r --27 1 T° 27x 37 47
Phase
Figure 3 Tracé de /,.. en fonction de ®
Q 31. Pour quelles fréquences 7... cette intensité est-elle maximale ?
Q 32. On s'intéresse à la largeur à mi-hauteur 06® des pics de Z,,, définie par
1,,,(0®/2) = 1,,/2. Dans
l'hypothèse où 1 -- À EUR 1, donner l'expression de 0® en fonction de M. En
déduire la largeur en fréquence 07
des pics de résonance de la cavité.
Q 33. Associer à cette largeur de fréquence une durée typique 7 de l'onde dans
la cavité en fonction de EUR, d
et À, toujours dans l'hypothèse où 1 -- R 1.
Nous cherchons maintenant à retrouver l'ordre de grandeur de cette durée 7 en
adoptant un point de vue
corpusculaire. À chaque réflexion, la probabilité que le photon franchisse le
miroir et sorte de la cavité est
T=1---Rk.
Q 34. Déterminer la durée de vie moyenne du photon dans la cavité en fonction
de EUR, d et À.
Q 35. Que doit valoir 1 -- À pour avoir une durée de vie du photon de 100 ms ?
Commenter.
Q 36. On recouvre en pratique les miroirs d'un supraconducteur de résistance
électrique nulle. Pourquoi ?
ITI.B --- Miroirs sphériques
Les miroirs ont en réalité une dimension finie. Considérons la situation où
l'on aurait des disques plans de rayon
a -- 25 mm. Comme indiqué en figure 4, l'onde électromagnétique parvenant sur
un miroir (ici le miroir de
droite) est ainsi diffractée. Une partie de l'onde diffractée n'est pas captée
par le miroir en vis-à-vis (ici le miroir
de gauche).
} O
miroir de gauche ES V miroir de droite
Figure 4 Diffraction sur l'un des
deux miroirs (ici le miroir de droite)
Q 37. Estimer la durée 7x au bout de laquelle l'intensité restant dans la
cavité est divisée d'un facteur
1000 par rapport à l'intensité initiale pour un photon de fréquence 51,1 GHz.
Commenter ce résultat.
y
Figure 5 Photographie des miroirs sphériques, Schéma d'un miroir sphérique,
Schéma de la cavité
2019-05-10 12:11:14 Page 5/11 CHELLES
Afin de palier le problème lié à la diffraction, on prend des miroirs en forme
de portion de sphère de rayon
de courbure R, -- 40 mm. Le rayon des miroirs est toujours a -- 25 mm, mais la
distance entre les deux est
désormais d' = 27,6 mm. La cavité est présentée en figure 5. On se place
dorénavant en coordonnées cylindriques
avec l'origine du repère au centre de la cavité ct l'axe (Oz) selon son axe de
révolution. L'intérieur de la cavité est
dans le vide. On admet que la diffraction est ainsi limitée et on s'intéresse à
l'étude de l'onde électromagnétique
dans cette cavité.
Pour une longueur d'onde À,, l'onde stationnaire pouvant exister dans la cavité
est de la forme
2 2
U r 2T2 À0Z AT
-- 8, --0 _ LE 207 --__ IL.2
s(M,t) 02 EXP | 7) COS | x, arctan ne) + KR) + s) exp(iwt) (IL.2)
d(r, 2)
D
À0Z
Où W(z) = Wp4/1 + (2) est le rayon typique du faisceau au niveau de l'abscisse
z dans le plan perpendicu-
2
AW,
laire à (Oz), w, est une constante appelée col du faisceau (waist en anglais),
R,(2) est le rayon de courbure des sur-
2 / /
) 1 TW À d d
faces d'onde : R,(2) = z+- su et & est une phase constante. On admet que wy =
1| -- TS Ry -- 5 J:
Z 0 T
Q 38. Calculer w, pour une fréquence de 51,1 GHz.
Q 39. Au niveau de l'axe (Oz) (r = 0), on souhaite que la structure d'onde
stationnaire présente un noeud
au niveau de chaque miroir et p ventres avec en particulier un ventre au niveau
de ©. En déduire, en fonction
de p, la variation en valeur absolue de P(r = 0,2) entre z = 0 et z = d'/2. Que
vaut p pour une fréquence de
l'onde de 51,1 GHZ ?
Q 40. En faisant l'analogie avec la corde de Melde, estimer l'ordre de grandeur
de la taille d'un fuseau.
Faire l'application numérique et commenter sachant que le jet atomique traverse
la cavité en son centre et a un
diamètre de 0,7 mm.
III Couplage entre un atome de Rydberg et la cavité
Les deux parties précédentes ont permis de mettre en évidence qu'un atome de
Rydberg et une cavité sont deux
systèmes dans lesquels il est possible de stocker de l'énergie : une énergie
hv,, = Aw,, pour l'atome (entre les deux
niveaux d'énergie n = 50 et n = 51 que l'on supposera isolés des niveaux
inférieurs) et une énergie hr, = Au,
pour un photon piégé dans la cavité. Nous allons maintenant voir comment ces
deux systèmes peuvent interagir,
échanger éventuellement de l'énergie et comment on peut utiliser cette
interaction pour détecter la présence
d'un photon dans la cavité sans le détruire.
Le traitement de ces interactions est quantique, mais il est possible de faire
des analogies avec des systèmes
classiques usuels.
IIT. A --- Représentation électrocinétique du couplage atome-photon
On admet que le couplage entre l'atome et un photon de la cavité peut être
assimilé à la présence d'une
inductance mutuelle M entre deux circuits LC (figure 6). Le circuit de gauche
représente la cavité tandis que le
circuit de droite est analogue à l'atome. On note w,.., et w.. les pulsations
propres de chacun des deux circuits
en l'absence de couplage.
C C
Cav at
Figure 6 Circuit équivalent au sys-
tème {photon + atome}
Q 41. Déterminer les expressions de w,, et w,,, en fonction de Z, C', et Ca.
Q 42. Les deux circuits sont considérés sans résistance. Quels phénomènes
physiques sont ainsi négligés au
niveau de l'atome et au niveau de la cavité ?
On pose 0 = w,4 --w.., le désaccord entre les deux pulsations. On considèrera
dans toute la suite que [| &
Weav + Wat
(151 & w,+). Par ailleurs, on note : w, -- 5
2019-05-10 12:11:14 Page 6/11 (C)EATETSS
Q 43. Montrer que les deux intensités 2, et ?,. vérifient le système
d'équations couplées suivant :
décay Q d'in 2 .
ae ag de + (6 ie = 0
(IIL.1)
d'i Q d°i
at Cav 2 -
------ + (wi +eE)ji,; = 0
dt? «w, dt? KG + Er
où l'on exprimera Q et EUR en fonction de w, à, M et L.
On cherche la possibilité pour que l'ensemble du circuit oscille à la même
pulsation w (on parle de mode propre).
On cherche ainsi ,, et 4, sous la forme complexe à, (t) =, expliwt) et à (4) =
I, exp(iut).
Q 44. Déterminer l'équation vérifiée par w, équation que l'on écrira sous la
forme d'un polynôme en w qui
s'annule, mais que l'on ne cherchera pas à résoudre.
On admet que w peut prendre deux valeurs dans le cas où à > (7, situation dans
laquelle on se place désormais :
ÿ ®
We = wp + Ë + 5) | (IIL.2)
ITI.B --- Couplage atome-photon de la cavité
Revenons à l'expérience d'électrodynamique quantique. On considère maintenant
le système {atome + cavité}.
En l'absence de couplage entre l'atome et la cavité, les niveaux d'énergie de
ce système sont représentés en figure
figure 7.
niveaux d'énergie
À
n = 51, 1 photon
fu
at
n = 91, 0 photon
io
Nu, +
n = 50, 1 photon
fu
Cav
n = 90, 0 photon
Figure 7 Niveaux d'énergie du système
{atome + cavité} en l'absence de couplage
En présence de couplage entre l'atome et la cavité, le niveau {n = 50 + 0
photon dans la cavité} garde la même
énergie. Il est pris comme niveau de référence des énergies.
En présence de couplage, l'état {atome n = 50 + 1 photon dans la cavité} a une
énergie w_ tandis que l'état
{atome n = 51 + aucun photon dans la cavité} a une énergie Aw,. L'état {atome n
= 51 + 1 photon dans la
cavité} voit quant à lui son énergie augmentée de +hQ?/(26).
Q 45. Reproduire la figure 7 sur votre copie et dessiner en pointillés la
position des quatre états considérés
en présence de couplage.
Q 46. En l'absence de couplage entre la cavité et l'atome, la différence
d'énergie entre les niveaux n -- 50
et n = 51 est Aw,,. Que vaut la différence d'énergie Aw', entre les niveaux n =
50 et n = 51 en présence d'un
couplage cavité-atome dans le cas où la cavité ne contient pas de photon ? En
déduire la variation de la pulsation
Oph
Au{0P = w',--w,, de l'atome correspondante.
Q 47. Déterminer de même l'expression de Ag tiPn) dans le cas où la cavité
contient 1 photon.
Afin de détecter la présence ou non d'un photon dans la cavité, on crée un
atome de Rydberg initialement dans
l'état n = 50, comme indiqué en introduction de ce sujet et illustré dans la
figure 1. Une impulsion micro-onde
place l'atome dans une superposition des états n = 50 et n --= 51. Les deux
états quantiques acquièrent un
déphasage D, = Awystea Où tv est la durée d'interaction entre l'atome et la
cavité. Comme nous venons de le
voir, ce déphasage dépend de la présence ou non d'un photon dans la cavité. Une
deuxième impulsion micro-onde
en sortie de cavité fait interférer ces deux états quantiques. On règle les
impulsions micro-ondes de manière à ce
que l'atome se retrouve dans l'état n = 50 en l'absence de photon dans la
cavité et dans l'état n = 51 en présence
d'un photon dans la cavité. On détecte alors l'état de l'atome à l'aide du
dispositif étudié en sous-partie ID.
L'état de l'atome renseigne sur la présence d'un photon dans la cavité sans
pour autant avoir détruit celui-ci.
2019-05-10 12:11:14 Page 7/11 (C)EATETSS
| Î
ps | HN
Te
n=50
0,0 0,5 1,0 1,9 2,0 2,5
temps (s)
Figure 8 Mesure non destructive de la présence d'un photon dans la cavité,
adapté
de« Mesure quantique non destructive répétée de la lumière : états de Fock et
trajectoires
quantiques » - Christine Guerlin - Thèse de doctorat de l'Université Paris VI
(14 décembre
2007)
Îl est alors possible d'envoyer plusieurs atomes à la suite comme indiqué sur
la figure 8 : une détection dans
n = 90 est représentée par un trait bleu vers le bas, une détection dans n = 51
par un trait rouge vers le haut.
Dans cette mesure, un photon (d'origine thermique) est apparu dans la cavité à
1,1 ms et a disparu à 1,5 ms.
Îl a ainsi été capturé pendant 0,4 ms. Pendant cette durée, il a parcouru une
distance de 1,2 x 10° km, soit
l'équivalent de À fois la circonférence de la Terre !
Données et formulaire
Masse de l'électron m, = 9,11 x 10 kg
Charge élémentaire e = 1,60 x 10 C
Permittivité diélectrique du vide Ep -- 8,89 X 10 Fm !
Constante de Planck h = 6,63 x 10 * J:s, À = 1.05 x 10 * J:s-rad !
Célérité de la lumière dans le vide ce = 3,00 x 10 mess !
Figure 9 Base sphérique
Volume infinitésimal en coordonnées sphériques
dV = r° sin 0 dr d'do
Opérateur gradient en coordonnées sphériques
Of. lof. 1 Of.
df= Ze, + 2,4 TT
grad J 9" | r 00 0 rsin00p
Opérateur laplacien d'un scalaire en coordonnées sphériques
1 Of 1 Of. Of I of
Af=--=-- 2) 5 ( )
J r? Ôr (r Or T r2 sin 0 06 \" 06 " r? sin" 0 04°
2019-05-10 12:11:14 Page 8/11 CO) 8Y-Nc-sA
Annexe
La plupart des documents et les textes entre guillemets de cette annexe sont
issus de la thèse de doctorat de
l'université Paris VI d'Alexia Auffèves, soutenue le 29 juin 2004 « Oscillation
de Rabi à la frontière classique-
quantique et génération de chats de Schrôüdinger ». Certaines figures et
données expérimentales ont été adaptées
pour les besoins de l'épreuve.
Le phénomène d'ionisation
« L'ionisation d'un atome désigne l'émission vers le continuum d'un électron
initialement dans un état lié. Elle
peut advenir par interaction de l'atome avec une onde lumineuse
(photo-ionisation) ou, comme dans notre cas,
avec un champ électrique quasi statique. »
Prenons une assemblée de N atomes identiques que l'on place dans un champ
électrique extérieur Æ que l'on
augmente linéairement au cours du temps. L'augmentation est lente si bien que
le champ peut être considéré
comme quasi statique. On relève le nombre d'atomes ionisés par unité de temps
d\N/dt. La dépendance en Æ
de AN /dt est représentée sur la figure 10.
1800 -
1600 + t,
1400 - Mu
Je
1200 oi
EH
1000 - UT
-- HE
] OE
u sh
800 Æ u
| EH
600 ï U
e EH
400 -- É [1
2 | EH
00 - ed ...
0 + nn
| E
C
-200
100 | 200 | 300
Figure 10 Variation de dN/dt en fonction de E
(unité arbitraire)
Le champ critique, ou champ d'ionisation, E,., est la valeur du champ
électrique pour laquelle le signal d'ionisation
est le plus élevé.
Présentation du détecteur
On cherche à déterminer si l'atome de Rydberg étudié est dans l'état n = 50 ou
n = 51.
Un des deux détecteurs utilisés dans l'expérience est présenté en figure 11.
Les atomes de Rydberg pénètrent dans
la zone d'ionisation, entre les électrodes parallélépipédiques a et b.
L'électron arraché à l'atome traverse alors
l'électrode b qui est percée d'un diaphragme de 6 mm de diamètre. Il entre dans
la zone de focalisation, constituée
d'une succession d'électrodes (électrodes c à e), avant de parvenir au
multiplicateur d'électrons (ME) situé juste
derrière l'électrode f. Le multiplicateur d'électrons permet, à partir d'un
électron incident, d'obtenir un courant
électrique mesurable. On peut ainsi relever l'instant où l'électron parvient au
multiplicateur d'électrons. On
négligera la durée mise par l'électron pour franchir la zone de focalisation.
La zone d'ionisation (figure 11) pourra être assimilée à un condensateur plan
(l'effet du trou dans l'électrode b
sur le champ électrostatique sera négligé, de même que l'influence de la zone
de focalisation). L'électrode b est
portée à un potentiel V, = 32 V fixe. L''électrode a est portée à un potentiel
V,(t) ajustable.
Tout électron arraché à un atome se trouvant devant le diaphragme parvient au
multiplicateur d'électrons.
Réglage du détecteur
On prend comme origine des temps l'instant où l'atome est excité dans l'état de
Rydberg circulaire, au niveau
de la boîte B de la figure 1.
Protocole 1
« On prépare un atome de vitesse fixée et on commence par repérer à quel
instant précis t,. l'atome ainsi
préparé est au centre du diaphragme. Pour cela on applique [à V,(t)] une rampe
d'ionisation très raide qui
permet d'ioniser instantanément tous les niveaux dans lesquels pourrait se
trouver l'atome. Lorsqu'on balaye le
déclenchement de cette rampe dans le temps, on obtient un électron si l'atome
se trouve dans le diaphragme et
rien sinon. » Pour chaque instant t de déclenchement de la rampe, on réitère
l'expérience avec le même nombre
N d'atomes. On relève pour chaque instant { le nombre d'atomes N, ionisés. Le
résultat est présenté en figure 12.
2019-05-10 12:11:14 Page 9/11 (C)EATETSS
do Ho >
SOrm
15mm
Figure 11 Présentation générale du détecteur et zoom sur la zone d'ionisation
800 -
700 - Ang Un ns.
=
- /
E
600 - / \
J / =
500 -- = \
1 E
400 --
Z 300- /
200 - "
100 - | \ |
0 - suuss _...
-100
500 505 510 515 520 525 530
Temps (US)
Figure 12 Pointé du centre du diaphragme de
la zone d'ionisation
Protocole 2
Une fois t, connu on peut faire varier V.(t) de manière affine et plus lente
que dans le protocole 1, en partant
de la valeur V,. La variation est choisie de manière à ce que les champs
d'ionisation E,.:9 et Æ,;:, des états
de Rydberg circulaires n = 50 et n = 51 soient balayés pendant que l'atome se
trouve dans la zone devant le
diaphragme. On réitère l'expérience pour un grand nombre d'atomes de même
vitesse, la moitié étant préparés
dans l'état n = 50, l'autre moitié dans l'état n = 51. On relève pour chaque
instant # le nombre d'atomes N,
ionisés. Le résultat de l'expérience est donné en figure 13.
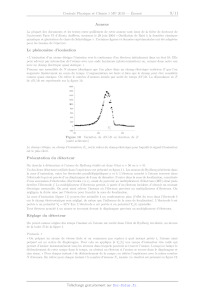
La rampe est choisie de manière à ce que l'ionisation soit sélective : chaque
courbe en cloche correspond à un
état de Rydberg (n = 50 ou 51) défini.
(é-- 0)
c?
ou 2 (figure 13). Les ajustements donnent : a, = 512,8 : b, = 515,4ps ; EUR, =
1,0 ps: a) = 559,1 ; b, = 519,2 ps:
Co = 0,9 ps.
On ajuste les deux signaux 1 et 2 par une fonction gaussienne de la forme N, =
a; exp (- | avec à = 1
2019-05-10 12:11:14 Page 10/11 CHENE
= ---- Ajustement du signal 1 seulement
500 - =: # soc: ---- Ajustement du signal 2 seulement
D
400 - " 500 -
400 +
300 - a
300 -
200 - m "
200 -
æ "" 100 -
[I o
0 + mt" "snsmpsn oi
511 512 513 514 515 516 517 518 519 520 521 522 523 511 512 513 514 515 516 517
518 519 520 521 522 523
Temps (45) Temps (15)
Nombre d'événements
D
Nombre d'événements
26" Signal 2
2 Signal 1
Nombre d'ionisations N, pour chaque instant t où Ajustement des deux signaux
par une fonction gaus-
la rampe est appliquée sienne
Figure 13
Principe de la détection
À l'aide de l'étalonnage effectué dans le procotole 2, on se fixe un instant t,
qui délimite la frontière entre les
2 états de Rydberg : un électron qui parviendra au multiplicateur d'électrons
avant t, sera attribué à l'un des
deux états de Rydberg, un électron qui parviendra au multiplicateur d'électrons
après t, sera attribué à l'autre
état de Rydberg.
ee oeFrFINeee
2019-05-10 12:11:14 Page 11/11 (GO) sY-Nc-sA
