CCINP Physique et Chimie MP 2019
| Thème de l'épreuve | "S'il vous plaît... dessine-moi un mouton !". |
| Principaux outils utilisés | thermodynamique, mécanique, optique géométrique, solutions aqueuses, oxydoréduction, cinétique chimique, diagramme E-pH |
| Mots clefs | diffusion de chaleur, mouton, modélisation, lactose, méthode de Bertrand, lait, chaux |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)














Rapport du jury
(télécharger le PDF)



Énoncé obtenu par reconnaissance optique des caractères
SESSION 2019 MPPC003
GP
CONCOURS
COMMUN
INP
ÉPREUVE SPÉCIFIQUE - FILIÈRE MP
PHYSIQUE - CHIMIE
Mardi 30 avril:8h-12h
N.B. : le candidat attachera la plus grande importance à la clarté, à la
précision et à la concision de
la rédaction. Si un candidat est amené à repérer ce qui peut lui sembler être
une erreur dénoncé, il le
signalera sur Sa copie et devra poursuivre sa composition en expliquant les
raisons des initiatives
qu'il a été amené à prendre.
Les calculatrices sont autorisées
Le sujet est composé de quatre parties totalement indépendantes.
La plupart des sous-parties le sont également.
1/16
« S'il vous plait... dessine-moi un mouton ! »
Le sujet s'intéresse à un mammifère particulier, le mouton, un des tous
premiers domestiqués par
l'homme, entre le 11° et le 9° siècle avant J.-C. en Mésopotamie. C'est un
animal clé dans l'histoire
de l'agriculture.
On appelle bélier le mâle adulte, brebis la femelle adulte, agneau le jeune
mâle et agnelle la jeune
femelle.
Comme tous les ruminants, leur système digestif complexe leur permet de
transformer la cellulose
de leur alimentation en acides gras volatils et en glucides simples. A la belle
saison, 1ls se nourrissent
dans les pâturages d'herbe broutée au ras du sol et on leur donne du foin en
hiver.
Jusqu'à nos jours, le mouton est utilisé pour ses produits laitiers, sa viande,
sa laine et son cuir, de
façon artisanale ou semi-industrielle. Sa viande et son lait ont été les
premières sources de protéines
consommées par l'homme dans le passage de la chasse-cueillette à l'agriculture.
La partie I étudie comment l'animal maintient sa température et son
comportement social.
La partie IT s'intéresse à deux des cinq sens de celui-ci.
La partie III s'intéresse aux propriétés chimiques de son lait.
La partie IV s'intéresse aux conditions d'élevage.
Ces parties sont toutes indépendantes les unes des autres, comme beaucoup de
sous-parties.
Données
-- L'opérateur gradient d'une fonction A(M\t) en situation unidimensionnelle
vaut en
, y -- "> OA(Zt) -- , 7
coordonnées cartésiennes grad(A(Z,t)) -- EUR; et en coordonnées sphériques
7 x OA(rt),
grad(A(r,t)) = Cr:
-- En coordonnées cartésiennes, l'opérateur divergence en situation
unidimensionnelle vaut
... [7 dAG)
div (AG)) =
-- En optique de Gauss, la formule de conjugaison de position sur l'axe (point
objet À, point
image A') des deux plans de front conjugués à travers une lentille mince de
centre optique
Ï Ï
| 1 EL
O et de distance focale f est : SG 5
2/16
-- On donne Îles potentiels standards des couples redox à 298 K :
produit
Couple d'oxydati OS | Cu'/CwO Fe**/Fe'* O2/H0 MnO4 /Mn°*
redox des glucides
/glucides
Een volts | Ordre de 0,04 0,77 1,23 1,51
grandeur -- 0,2
-- Sauf indications contraires, toutes les constantes d'équilibres chimiques en
solutions
aqueuses sont données à 298 K, température T à laquelle le produit ionique K,
de l'eau
vaut 10 !* et la quantité RT-Ln(10)/F de la formule de Nernst vaut 0,06 V-mol !.
F représente le Faraday, c'est-à-dire la charge d'une mole de charges
élémentaires e.
-- Masses molaires en g'mol :
hydrogène M(H) = 1,0 carbone M(C) = 12,0 oxygène M(O) = 16,0
chlore M(CI) = 35,5 calcium M(Ca) = 40,0 cuivre M(Cu) = 63,5
-- La constante des gaz parfaits vaut R = 8,31 J-K"! mol !.
-- La charge élémentaire vaut e = 1,60-107!°C.
-- Le nombre d'Avogadro vaut N, = 6,02:10** mol |.
Partie I - La température du mouton
Document (vigiferme.org, pour le bien-être de l'animal et de l'éleveur,
consulté en 2018)
Exposition à de basses températures
Les moutons sont naturellement adaptés pour supporter de très basses
températures mais leur
résistance au froid dépend de plusieurs facteurs : la race, l'âge, l'état du
pelage.
Un mouton qui a une épaisse toison et qui est protégé de l'humidité pourra
supporter des températures
qui descendent en dessous de -- 15 °C, un mouton tondu doit être protégé du
froid. [...| Lorsque le
temps est humide, que les températures sont basses et qu'il y a du vent, la
situation est critique pour
les moutons. Le plus important est qu'ils ne soient pas mouillés jusqu'à la
peau. La laine de certaines
races, lorsqu'elle est épaisse, peut repousser l'humidité plusieurs jours.
C'est le cas des races de
montagne mais pour d'autres, à la laine très fine, le pelage est moins
protecteur.
Les moutons qui ont froid se serrent les uns contre les autres.
Les agneaux nouveau-nés sont très sensibles aux basses températures, au vent et
à l'humidité. Leur
fine couche de laine et de graisse ne les protège que très peu. Les brebis
prêtes à mettre bas doivent
être isolées en bergerie et y rester au moins deux semaines après la naissance.
Le taux de mortalité
des agneaux qui viennent de naitre atteint plus de 25 % dans certains élevages.
Ils succombent le plus
souvent dans les heures qui suivent leur naissance par hypothermie plutôt que
par maladie.
.
3/16
Exposition à de hautes températures
Les moutons supportent mieux le froid que les températures élevées. Ils peuvent
mourir d'un coup
de chaleur. Ce risque est beaucoup plus élevé chez les moutons qui ne sont pas
tondus, car la laine
empêche la sueur de s'évaporer. C'est une des raisons pour laquelle 1l faut
tondre les moutons au
printemps.
Cas de la Confort sans Adaptation très Inadaptation pouvant
brebis non adaptation ou Adaptation difficile pr P p
difficile entraîner la mort
tondue adaptation facile
Température de---15°Càa-8°C | d--30°Ca-15 °C | en dessous de -- 30 °C
eicure de -- 8 °C à 25 °C et et et
de 25 °C à 35 °C de 35 °C à 40 °C au-dessus de 40 °C
La température d'un mouton en bonne santé se situe entre 38,5 et 39,5 °C.
Sa longueur moyenne va de 1 m à 1,50 m.
La tonte a lieu 1 à 2 fois par an produisant 2 à 8 kg de laine par an.
Fin document
Nous allons essayer de construire un modèle thermodynamique pour expliquer
comment la brebis
maintient sa température de consigne 8e = 39 °C et mieux comprendre les
éléments du document
ci-dessus.
L.1 - Propriétés de la toison de laine
La laine, matière première renouvelable, est une fibre aux propriétés uniques :
flexible, légère,
élastique, solide protégeant du chaud comme du froid, difficilement inflammable
(s'enflamme à
600 °C), isolant phonique, absorbeur d'humidité, facile à tendre et 100 %
biodégradable. La fibre de
laine est à croissance continue avec de grandes écailles qui en font le tour.
Les écailles se recouvrent
peu et sont très saillantes. La section est circulaire. Sa substance est de la
kératine, matière complexe
association d'une vingtaine d'acides aminés. La laine a des affinités
différentes avec l'eau qui font
que la fibre s'enroule en frisures. Ces dernières enferment une grande quantité
d'air, ce qui limite la
conduction. De plus, la kératine est hydrophile pour la vapeur d'eau mais
hydrophobe pour l'eau
liquide. L'adsorption d'eau (désorption d'eau) s'accompagne d'une production
(dégagement) de
chaleur par la fibre. Les fils de laine ont un diamètre qu1 varie de 20 um pour
les moutons Mérinos à
40 um pour les races écossaises.
Une toison de laine va être caractérisée par une valeur de conductivité
thermique Maine Supposée
homogène et une valeur de capacité thermique massique Ciaine. On considèrera
par la suite une laine
« moyenne » caractérisée par une conductivité thermique Maine = 0,040 W-m !-K'!.
Q1. La loi de Fourier, relative à la diffusion thermique, traduit le lien entre
la densité volumique de
transfert thermique et le gradient de température : ] O7 À - gradT.
Quelle est la dimension de la conductivité thermique À ?
4/16
On considère un parallélépipède, de longueur L, de hauteur H et d'épaisseur e
petite (e << min(L, H)), constitué d'un matériau homogène de conductivité À, de masse volumique u et de capacité thermique massique c (figure 1). Le problème est supposé unidimensionnel, la température ne dépend que de la variable z et du temps t. x L Figure 1 - Géométrie du conducteur thermique Q2. Sur quelle direction est le vecteur densité jo de courant thermique ? De quelles variables dépend-il ? Les températures, sauf avis contraire, sont en °C. Q3. Faire un bilan énergétique sur la tranche de matériau comprise entre z et z + dz et en déduire l'équation différentielle à laquelle obéit la température T(z.t). Q4. Que devient-elle en régime stationnaire ? Le vecteur jo dépend-il de z ? Q5. On suppose que le matériau est en présence de thermostats qui imposent à tout moment une température Tr en Z=0etT,,, en z = e. Que vaut la puissance thermique @ qui traverse le matériau en fonction de e, À, H, L, Tyyée et Tiortie ? Q6. Définir puis exprimer la résistance thermique du matériau en fonction de ses caractéristiques géométriques et de sa conductivité. Que signifie, du point de vue thermique, mettre des résistances en parallèle et mettre des résistances en série ? On peut mesurer expérimentalement la conductivité thermique de la laine à partir d'un échantillon de celle-c1 par la méthode de la plaque chaude gardée (figure 2, page 6). L'échantillon est formé de deux « plaques » de laine identiques d'épaisseur e et de surface S séparées par une plaque chaude. Un même flux thermique o, engendré par effet Joule dans un conducteur électrique inséré dans la plaque chaude, traverse les échantillons. Les plaques d'échantillon sont encadrées chacune par une plaque froide. Les températures Te, Tr des plaques chaude et froides sont mesurées en régime permanent par des thermocouples. 5/16 Q7. Exprimer l'expression de la conductivité Maine de l'échantillon en fonction de ©, e, S, Te et Tr. Échantillons de laine Plaque froide T+ Isolant «---- Plaque chaude Te Plaque froide T+ Figure 2 - Principe de la plaque chaude gardée 1.2 - Équilibre thermique d'une brebis (situation de confort) On modélise la brebis debout par un parallélépipède plein, de température uniforme ea = 39 °C, de longueur L = 100 cm et de section carrée de côté H = 30 cm. Le corps de la brebis est entouré d'une épaisseur qui peut varier de e = em = 10 cm de laine avant la tonte à e = em = 0,5 cm après la tonte. La situation est représentée en figure 3 et en figure 4 (page 7). Q8. Exprimer la résistance Raï de cette carapace de laine en négligeant les effets de bords, en fonction de L, H, e et Maine. Evaluer son ordre de grandeur pour les deux épaisseurs limites. RO nee ns a Dane ARE UE RL Figure 3 - Modélisation de la brebis 6/16 avant dos \ NC N L=ilm D e : épaisseur de laine H = 30 cm (æ) Figure 4 - Modélisation de la toison Seules les parties lainières du dos et de l'avant ont été schématisées. On doit tenir compte de deux autres phénomènes d'échanges thermiques : la conducto-convection (d'autant plus importante que le vent est fort) et le rayonnement thermique toujours présent. Q9. La loi de Newton, relative au phénomène de conducto-convection, correspond à un vecteur de densité thermique reçu par la brebis égal à Jo = --h "(Ti -- Tair)n avec Text la température de la surface extérieure de la brebis en contact avec l'air de température Taïr et le vecteur unitaire normal n orienté de la brebis vers l'extérieur. On prendra un coefficient de Newton laine/air égal à h = 4,0 Wm *K !. En déduire en fonction de h, L et H la résistance de conducto-convection R& à introduire dans notre modèle de brebis. Évaluer son ordre de grandeur. Le phénomène de rayonnement introduit une résistance supplémentaire R+. Comme la température de l'air est assez proche de celle de l'animal, la puissance P; due au rayonnement thermique sortant de la surface extérieure de la brebis s'exprime sous la forme Pr = KA(T ext -- T'air) avec À l'aire de la surface extérieure de la brebis, Tx+ la température de cette surface en contact avec l'air de température Taïr. La constante K a pour valeur K = 5,0 Wm °K{. Q10. Exprimer la résistance thermique de rayonnement R: en fonction de K, L et H. Q11. Faire un schéma du montage de ces trois résistances placées entre la température interne de la brebis Tint-- 0e -- 39 °C et la température de l'air Tai. Evaluer numériquement les deux valeurs R1 et R2 des résistances équivalentes de la brebis non tondue et de la brebis tondue. La brebis non tondue est dans un confort climatique pour la température de l'air égale à To= S °C. En plus des phénomènes de diffusion, conducto-convection et rayonnement, 1l y a évaporation d'eau par sudation. La brebis émet de la vapeur d'eau par les voies respiratoires en toute situation : m=5,8-10 °g.s ". Elle en émet deux fois plus par sa surface cutanée quand elle vient d'être tondue : m'=2m et que la température extérieure est supérieure à 5,1 °C. 7/16 L'enthalpie massique standard de vaporisation de l'eau, supposée indépendante de la température, vaut AH° sp = 2 500 kKJ-kg |. Q12. En déduire la puissance p,,, apportée à la brebis par son métabolisme dans une situation de confort Juste avant la tonte. On l'exprimera en fonction de m, L, R1, Tint et Tair, puis on en fera l'évaluation numérique pour Tair = T, = 5 °C. Q13. Répondre à la même question pour la brebis juste après la tonte pour la température de confort T,=5°C. L.3 - Déséquilibre thermique d'une brebis (situations de stress et de danger) La thermorégulation est due à des productions internes de chaleur (thermogenèse liée au métabolisme et à l'activité physique) et à des déperditions de chaleur au niveau de Îla respiration et de la peau (thermolyse). Dans une situation où l'air environnemental est en dehors de la zone de confort, la brebis va se réchauffer ou se refroidir et éventuellement transpirer. On négligera la capacité thermique de la toison devant celle du corps de la brebis. On assimile la brebis à un volume d'eau de masse volumique u = 1 000 kg-m * et de capacité thermique massique c = 4 200 J-K°!-kg !. On admet que les variations de température sont suffisamment lentes pour utiliser les notions de résistances. On note p_ la puissance apportée par le métabolisme. Q14. à) En appliquant le premier principe de la thermodynamique à la brebis non tondue dans une situation (1) où la température Tai de l'environnement est différente de To = 5 °C, montrer que l'équation différentielle relative à la température T(t) de la brebis s'écrit : dT() 1 (Ti -Tair) a 'tr (T(t) -- Tair) ---- | On exprimera t, en fonction de u, c, L, H, R1 et (T1 -- Tair) en fonction de 0e, To, R1 et (Pa Pin) ' b) Exprimer la température T(t) en fonction de t, T1, t, et 04 en supposant que la température initiale de la brebis est T(t = 0) -- Gea. c) Calculer t,. Calculer Ti en °C pour p -- p., avec une température d'environnement égale à T'air = |7 °C. Q15. D'après les données du document (pages 2 et 3), la brebis non tondue reste dans sa zone d'adaptation pour une température extérieure variant de -- 8 °C à + 15 °C. En déduire entre quelles limites peut varier la puissance apportée par le métabolisme de l'animal dans cette situation (1) sans qu'il y ait danger pour lui. On suppose donc que la brebis reste à sa température d'équilibre 0ea = 39 °C. Q16. En appliquant le premier principe à la brebis tondue dans une situation (2) où la température Tair de l'environnement est supérieure à To -- 278 K = 5 °C, montrer que l'équation différentielle relative à la température T(t) de la brebis peut se mettre sous la forme dT( + L (T(t) _ Tair) _ UT = Tair) dt T T dans laquelle les notations T, et t, sont des constantes à déterminer. Exprimer t;/7,. Commenter. En supposant que la possibilité de variation de la puissance métabolique soit celle obtenue à la question Q15, jusqu'à quelle température extérieure la brebis tondue peut-elle s'adapter à la chaleur ? 8/16 Q17. Faire un schéma de montage électrique équivalent aux situations (1) et (2) en indiquant les valeurs des éléments du montage en fonction de T,, T, t, et t,, R, et R.. Tracer l'allure de T(t) dans une situations de type (1) (brebis non tondue) à partir d'une température initiale T(t = 0) = 844= 39 °C avec Pm -- Pmo et une température de l'air égale à 17 °C. Tracer l'allure de T(t) pour la situation (2) (brebis tondue) à partir d'une température initiale T(t= 0) = 0e = 39 °C et une température de l'air égale à 25 °C sachant que la valeur de T,-T.. vaut 2,6 °C. Pour assurer leur survie, 1l leur faut une alimentation suffisante en sources de glucides. Ce sont les réactions chimiques issues du glucose qui fournissent l'énergie du métabolisme. Les réactions d'oxydation du glucose C6H1206 par le dioxygène respiré formant de l'eau et du dioxyde de carbone sont les sources d'énergie thermique. Q18. Écrire le bilan chimique pour une mole de glucose. Sachant que cette réaction est caractérisée par une enthalpie standard de réaction égale à AYH = -- 2 800 kJ-mol !, quelle est l'énergie thermique apportée par litre de dioxygène respiré (pris à 5 °C à la pression de 1 bar) ? En utilisant les résultats de la question Q12 (page à), quelle quantité d'oxygène la brebis doit- elle respirer par minute en situation de confort ? 1.4 - Réponse d'un groupe de brebis Les brebis se serrent les unes contre les autres en situation de stress thermique dû au froid extérieur. Supposons que le berger ait un troupeau de 6 brebis non tondues. Plusieurs regroupements sont possibles comme indiqué en figure 5. Cas 0 L Cas 2° Cas 2 Cas 1 Cas 1° Figure 5 - Regroupements possibles de 6 brebis Q19. Évaluer la diminution de surface en contact avec l'air par rapport aux brebis isolées dans les cas |, 1", 2 et 2° en fonction de H et X = L/H = 3,3 (Longueur L et section carrée de côté H telles que définies dans la figure 4, page 7). Quel sera le cas de plus faible conductance thermique ? Dans quelle configuration les brebis ont-elles intérêt à se regrouper ? Quelle sera la diminution relative moyenne de métabolisme nécessaire au maintien de la température interne induite par le regroupement ? Certaines ont-elles intérêt à changer de place de temps en temps ? 9/16 Partie II - La vie du mouton IL.1 - Ouie Les moutons ont une bonne audition. Le principe de l'oreille est le même que celle de l'oreille humaine mais le spectre audible est plus large car les ovins entendent les ultrasons. L'oreille des ovins est constituée de trois parties : l'oreille externe avec un pavillon « déformable » qui collecte les «sons » pour les conduire au tympan, l'oreille moyenne qui transmet avec amplification vers l'oreille interne qui est un transducteur mécano-électrique qui fournit des signaux au nerf auditif. Le schéma de principe est représenté figures 6 et 7. Le tympan est une membrane plane de surface s sans épaisseur et de masse m qui se déplace parallèlement à elle-même de x(t) par rapport à une position d'équilibre. Il est soumis à une force de 2 dx --, \ / frottement Ï = -- ue (a est le coefficient de frottement), à une force engendrée par le « son » incident de la forme N = N(t}e,, à une force de rappel t=-kxe, (k est la constante de raideur) et à une force de surpression par rapport à l'équilibre F=- pse, créée par la cavité d'air entre le tympan et l'oreille interne. L'oreille interne est modélisée par une membrane sans épaisseur de masse m', de surface s' soumise dx' --> dt -->
t'=-k'x'e, (k'est la constante de raideur) et à une force de surpression
F'=ps'e,. La surpression
p(t) = p(x(t), x'(t)) est, dans une hypothèse d'adiabaticité et de faibles
déplacements, égale à
à une force de frottement f=--- a" e, (a est le coefficient de frottement), à
une force de rappel
P ne y
=Y 0(- s'x'+5sx) en supposant l'air comme un gaz parfait caractérisé par un
coefficient Y = 1,4.
P Vo PP £8az P P
Conduit auditif
Air (Volume Vo
pression Po)
Oreille interne
Tympan Cavité de l'oreille
moyenne
Figure 6 - Situation sans stimuli sonore
X
Air (Volume
| Vo +S'X -- SX,
| pression Po + p)
s S"
Figure 7 - Situation avec stimuli sonore
10/16
Q20. Écrire les équations différentielles « croisées » relatives aux
déplacements x(t) du tympan et
x"'(t) de l'oreille interne.
Pour étudier le spectre audible, nous étudions la réponse à un signal sonore
harmonique. On remplace
les grandeurs physiques par leurs grandeurs complexes associées N(t) =
Niexp(-i(t)).
On néglige les frottements.
E SS" Po Po s' Po 7 k°
Q21. On pose Qc = NE Vo OO, = Ye Vo et Do = |:
X !
Exprimer le rapport q == des amplitudes complexes de déplacement X, de
l'oreille interne et
P PPOIT qe P P P A0
"2 m2 »
X, du tympan en fonction de oe?, @9", % et Q,". Pour quelle pulsation aura-t-on
résonance en
absence de frottement ? Quel(s) rôle(s) joue le frottement ? Tracer l'allure de
la courbe |q| en
fonction de & en tenant compte du frottement.
Q22. La masse m' de la membrane de l'oreille interne est égale à 15 mg et sa
raideur vaut
k'=3 500N-m |. On obtient une résonance pour une fréquence f; = 4,5 kHz. Quel
est le volume
Vo de la cavité de l'oreille, sachant que la surface de la membrane de
l'oreille interne vaut
s' = 0,06 cm" ? Que signifie le fait que le mouton entend des ultrasons
inaudibles pour
l'homme ?
II.2 - Vue
4 mort
fi
11/16
Les pupilles des humains sont circulaires, celles des ovins sont rectilignes.
Les yeux des moutons tournent sur eux-mêmes du même angle que l'inclinaison de
la tête, ce qui
rend leurs pupilles linéaires toujours parallèles au sol. Ces pupilles
horizontales leur permettent une
excellente vision périphérique : un angle de vision d'environ 300° à 350°, ce
qui leur permet de voir
derrière eux en broutant. Les humains ont une vision périphérique d'environ
170° à 190°.
Par contre, les moutons n'ont pas une bonne profondeur de champ. En vision
binoculaire, ils ne voient
qu'avec un angle de 25° à 50° alors que l'homme voit dans un champ de 110° à
130°. Ils ont peur
des ombres et recherchent des endroits bien éclairés. Les éleveurs exploitent
ces propriétés pour les
déplacer.
Q23. Expliquer par un croquis comment le déplacement des yeux vers l'arrière de
la tête permet
d'augmenter le champ de vision périphérique. Expliquer pourquoi les bergers
conduisent les
troupeaux comme on le voit sur la photo page 11.
L'oe1l réduit d'un mouton et celui d'un homme sont basés sur le même principe,
comme indiqué en
figure 8.
. rétine:
iris |
axe optique
Figure 8 - OEil réduit de mammifère
Les moutons voient naturellement net des objets proches et ne voient pas des
objets plus éloignés.
Dans l'oe1l de mouton, la distance d entre la lentille d'entrée (cristallin) et
la rétine est de l'ordre de
25 mm, dans l'oe1l humain de 15 mm. Le Punctum Proximum est pour le mouton de 5
cm et pour
l'homme de 15 cm. Le Punctum Remotum vaut 2 m pour le mouton.
Q24. Évaluer la distance focale de l'oeil du mouton qui n'accommode pas du tout
et de celui qui
accommode au maximum. On appelle pouvoir d'accommodation la différence des deux
valeurs
de vergence correspondantes. Comparer à celui de l'oe1l humain.
Partie III - La composition et les qualités du lait de brebis
Le lait est une substance très complexe, comportant un grand nombre d'espèces
moléculaires
différentes. Le principal sucre du lait est le lactose, molécule qui a un
pouvoir rotatoire. Sous l'effet
d'enzymes, le lactose est transformé en acide lactique. Par rapport au lait de
vache, le lait de brebis
contient plus de protéines, de lipides, de calcium et magnésium et la même
quantité de lactose par
litre.
12/16
Dosage du lactose par la méthode « officielle »
On utilise la méthode de Bertrand : on oxyde le lactose RCHO du lait par de la
« liqueur de Fehling »
(solution bleu foncé, assimilée à du sulfate cuivrique CuSO4 en milieu basique
pH = 14) en excès. Il
se forme un précipité rouge brique d'oxyde de cuivre Cu20 et des produits
d'oxydation du lactose.
Après élimination des 1ons cuivriques restants, on oxyde le précipité d'oxyde
cuivreux Cu20O par du
sulfate ferrique Fe2(SO4)}3. On dose ensuite les ions ferreux Fe** obtenus par
le permanganate de
potassium KMnO! (solution de couleur violette). Le résumé de ces opérations
successives est sur la
figure 9.
lactose Cu2° Cu20 Fe" Fe"* MnO4
Produits ;
d'oxydation Cu2O Cu** Fe" Fe" Mn°*
du lactose
Étape 1 Étape 2 Étape 3
(avec oxydation d'autres glucides) (après élimination du Cu(I)
excédentaire)
Figure 9 - Les étapes de la méthode de Bertrand
Q25. Écrire les réactions chimiques des étapes 2 et 3. Calculer la constante de
l'équilibre de l'étape 3
écrite pour une mole de permanganate MnO: .
Le protocole est décrit ci-dessous.
Verser dans un erlenmeyer de 200 mL, 40 mL de liqueur de Fehling fraichement
préparée avec 5 mL
de lactosérum. Faire bouillir pendant 3 minutes. Laisser refroidir. On doit
observer un liquide bleu
qui surnage. Verser le liquide bleu et rincer le solide rouge avec de l'eau
distillée bouillante. Laisser
refroidir puis verser dans l'erlenmeyer une solution de sulfate ferrique
acidifiée par de l'acide
sulfurique. Agiter. On obtient une solution verte avec dissolution du précipité
rouge. La solution
obtenue est dosée par du permanganate de potassium de concentration molaire EUR
= 0,02 mol-L !. La
fin de réaction est repérée par la goutte de permanganate pour laquelle la
solution prend une teinte
rose.
Q26. Pourquoi dans le protocole doit-on s'assurer de la présence du liquide
bleu surnageant ?
Pourquoi faut-1l préparer la solution de permanganate de potassium à la
dernière minute ?
Pourquoi faut-il isoler l'oxyde cuivreux et ne pas obtenir le produit sec ?
Pourquoi la fin de réaction est-elle repérée par une couleur rose ?
Les réactions de la première étape ne sont pas « stoechiométriques » par
rapport au lactose car 1l y a
plusieurs produits d'oxydation possibles et d'autres glucides. On utilise donc
les tables de Bertrand,
qui correspondent au protocole cité, construites expérimentalement pour
diverses concentrations en
lactose. Elles fournissent la masse m* de lactose dans la prise d'essai à
partir de la masse m de cuivre
13/16
présent dans l'oxyde Cu20. La lecture de la table de Bertrand du protocole
utilisé indique qu'une
quantité de lactose égale à m* -- 240 mg dans la prise d'essai correspond à 67
mg de cuivre contenu
dans Cu20.
Q27. Établir le lien entre la masse de cuivre contenue dans l'oxyde cuivreux et
le volume de
permanganate versé à l'équivalence. Quelle est la valeur du volume de
permanganate versé
pour obtenir l'équivalence pour un lait qui contient 48 g de lactose par litre ?
La fraicheur d'un lait est liée à son acidité exprimée en degrés Dornic,
sachant que 1 °D correspond
à 0,1g d'acide lactique par litre de lait et que plus le lait est frais, moins
1l est acide.
Le lactose, de masse molaire 342 g-mol |, donne par hydrolyse de l'acide
lactique AH de masse
molaire 90 g-mol ! :
lactose + H20 = 4 AH (acide lactique)
soit avec les formulations moléculaires :
C12H22011 + H20 = 4 C3H6Où3.
C'est la présence d'acide lactique, de pKaA = 3,9 qui donne une saveur
légèrement acide au lait frais.
Un lait de brebis est considéré comme frais s1 son degré Dornic est inférieur
ou égal à 18 °Dornic.
Q28. Le dosage de 10 mL d'un lait de brebis qui contient 48 g de lactose par
litre est réalisé avec une
solution de soude de concentration 1/9 = 0,111 mol-L !. Pour obtenir le
changement de teinte
de l'indicateur coloré, on verse 2,1 mL de la solution titrante. En déduire
l'acidité de ce lait en
°Dornic. Est-il frais ? Pourquoi appelle-t-on cette solution titrante la soude
Dornic ?
Q29. Le lait «tourne » quand son degré Dornic dépasse 18°. Quelle masse de
lactose s'est-elle
dénaturée par litre de lait quand le degré vaut 21 °D. Quel sera le degré
Dornic s1 on laisse le
lait (dosé en Q28) à l'air libre ?
Partie IV - Bien-être animal. Hygiène et entretien des bergeries
Les locaux doivent être sains donc régulièrement désinfectés. L'entretien des
sols peut se faire par
l'eau de Javel (et/ou l'eau oxygénée qui peut servir à nettoyer les ongles des
sabots pour éviter le
piétin qui est une maladie) et on enduit de chaux les murs intérieurs des
bergeries.
IV.1 - Fabrication de l'eau de Javel
Q30. Le chlore CI est caractérisé par Z = 17 : indiquer sa structure
électronique ainsi que celle de
l'ion chlorure C1 . Indiquer les états d'oxydation du chlore dans le dichlore
Ch, l'ion chlorure
CI , l'ion hypochlorite CIO et l'acide hypochloreux HCIO.
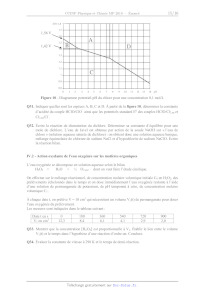
On donne en figure 10 (page 15) le diagramme potentiel-pH qui tient compte de
ces espèces pour
une concentration C = 10 'mol-L !.
14/16
1,3 OR
1,2 DA
1,1 C D
1
0,9 mu
LL:
0,8
0 l 2 3 4 5 6 7 8 9 10 11 12 13 14 pH
Figure 10 - Diagramme potentiel-pH du chlore pour une concentration 0,1 mol/L
Q31. Indiquer quelles sont les espèces À, B, C et D. À partir de la figure 10,
déterminer la constante
d'acidité du couple HCIO/CIO ainsi que les potentiels standard E° des couples
HCI10/Cl aq et
Clz.aq/CI .
Q32. Écrire la réaction de dismutation du dichlore. Déterminer sa constante
d'équilibre pour une
mole de dichlore. L'eau de Javel est obtenue par action de la soude NaOH sur «
l'eau de
chlore » (solution aqueuse saturée de dichlore) : on obtient donc une solution
aqueuse basique,
mélange équimolaire de chlorure de sodium NaCI et d'hypochlorite de sodium
NaCIO. Écrire
la réaction bilan.
IV.2 - Action oxydante de l'eau oxygénée sur les matières organiques
L'eau oxygénée se décompose en solution aqueuse selon le bilan
H202 = HO + 1% O7 dont on veut faire l'étude cinétique.
On effectue sur le mélange réactionnel, de concentration molaire volumique
initiale Co en H2O, des
prélèvements échelonnés dans le temps et on dose immédiatement l'eau oxygénée
restante à l'aide
d'une solution de permanganate de potassium, de pH tamponné à zéro, de
concentration molaire
volumique C1.
À chaque date t, on prélève V = 10 em qui nécessitent un volume V.(t) de
permanganate pour doser
l'eau oxygénée du prélèvement.
Les mesures sont indiquées dans le tableau suivant :
Datetens 0 180 360 540 720 900
Viencm 12,3 8,4 6,1 4,1 2,9 2,0
Q33. Montrer que la concentration [H,0;] est proportionnelle à V.. Établir le
lien entre le volume
V.(t) et le temps dans l'hypothèse d'une réaction d'ordre un. Conclure.
Q34. Évaluer la constante de vitesse à 298 K et le temps de demi-réaction.
15/16
Q35. Toutes choses égales par ailleurs, la vitesse de réaction est multipliée
par 5 quand on passe de
298 K à 348 K, quelle grandeur pouvez-vous en déduire ?
I1V.3 - Chaulage des murs
La « chaux éteinte » Ca(OH}2 est obtenue par action de l'eau sur la chaux vive
CaO fabriquée dans
les fours à chaux. On en badigeonne les murs pour détruire les matières
premières organiques riches
en eau. Le caractère alcalin très marqué tue microbes et bactéries.
Dans les fours à chaux, on réalise la calcination du carbonate de calcium CaCO3
(contenu dans les
roches calcaires réduites en petits morceaux). On introduit un mélange de
roches et de bois par le
haut du four qu'on chauffe par le bas. On maintient une température égale à 1
173 K. La chaux vive
est récupérée en bas du four en fin de cuisson puis elle est éteinte dans des
fosses alimentées avec de
l'eau de rivière. On la place dans des tonneaux pour l'utiliser en maçonnerie.
\ . T - fusi
Espèce chimique A°H en kJ-mol ! S? en J-mol !-K"! empérte de Son
CaO solide -- 600 105 2 850
CaCO; solide -- 1 100 225 1 100
CO: gaz -- 350 270
Q36. Écrire la réaction chimique de calcination qui est la décomposition du
carbonate en chaux vive
et dioxyde de carbone.
Q37. À partir du tableau ci-dessus calculer les variations standard d'enthalpie
AYH et d'entropie A°S
de la réaction. On les suppose indépendantes de la température et on ne tient
pas compte de la
fusion du carbonate de calcium qui, engagé dans des roches, fond à une
température plus grande
que 1 100 K. Commenter les signes. Le système pourrait-il être auto-entretenu
dans un réacteur
adiabatique avec une introduction des roches à 300 K ?
Q38. Exprimer la variation d'enthalpie libre standard A°G(T). Exprimer la
pression partielle du gaz
carbonique, quand l'équilibre est réalisé, en fonction de T. Que vaut-elle à 1
000 K ?
Commenter. Le maintien d'une pression partielle en CO: inférieure à cette
valeur est-elle
favorable à la fabrication de chaux ? En est-1l de même s1 on ajoute, à
pression totale constante,
un constituant gazeux chimiquement inerte ?
Q39. Le four à chaux traite 2 kg de roches concassées par seconde en entrée.
L'entrée des roches se
fait à 300 K. La réaction de calcination est totale à 1 173 K. Quelle est la
puissance thermique
nécessaire à la réalisation de la calcination à 1 173 K s1 on admet que les
roches sont du
carbonate de calcium pur dont la capacité calorifique vaut C = 900 J-kg !-K°1?
Q40. Quelle est la réaction qui se produit dans les fosses d'extinction de la
chaux ? Donner la
composition quantitative de l'eau de chaux dont on suppose le pH égal à 12,3,
sachant que le
produit de solubilité de Ca(OH), vaut K;= 5,0-10 *.
FIN
Les photos qui illustrent le sujet proviennent du site
pixabay.com/fr/photos/moutons, consulté en 20168.
16/16
IMPRIMERIE NATIONALE --- 191146 - D'après documents fournis
