CCINP Physique MP 2018
| Thème de l'épreuve | Questionnements et découvertes autour de l'atome le plus simple de l'univers |
| Principaux outils utilisés | mécanique classique, mécanique quantique, optique ondulatoire, magnétisme |
| Mots clefs | hydrogène, électron, Michelson, moment magnétique, spectre, raie à 21 cm |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
👈 gratuite pour ce corrigé si tu crées un compte
- -
Énoncé complet
(télécharger le PDF)














Rapport du jury
(télécharger le PDF)



Énoncé obtenu par reconnaissance optique des caractères
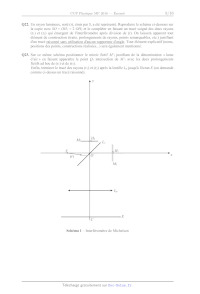
SESSION 2018 ! ! ! MPPH008 ! ÉPREUVE SPÉCIFIQUE - FILIÈRE MP! !!!!!!!!!!!!!!!!!!!!" PHYSIQUE Vendredi 4 mai : 8 h - 12 h! !!!!!!!!!!!!!!!!!!!!" N.B. : le candidat attachera la plus grande importance à la clarté, à la précision et à la concision de la !"#$%&'()*+,'+-)+%$)#'#$&+./&+$0.)"+1+!.2"!.!+%.+3-'+2.-&+4-'+/.054.!+6&!.+-).+.!!.-!+#7")()%"8+'4+4.+ /'9)$4.!$+/-!+/$+%(2'.+.&+#.:!$+2(-!/-':!.+/$+%(02(/'&'()+.)+.;24'3-$)&+4./+!$'/()/+#./+')'&'$&':./+3-7'4+ a été amené à prendre.! ! !!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!" " ! ! ! ! ! ! Les calculatrices sont autorisées ! ! ! ! ! L'énoncé de cette épreuve comporte 16 pages, dont 3 pages d'annexe. ! ! ! ! ! ! ! ! ! ! ! ! ! ! ! ! ! 1/16 ! Questionnements et découvertes autour de l'atome le plus simple de l'univers Dans ce sujet, on propose d'étudier quelques étapes clés de l'étude des niveaux d'énergie de l'atome d'hydrogène. Le problème est constitué de 7 parties, quasiment indépendantes, même s'il y a un fil conducteur entre elles. Il est conseillé au candidat de faire une première lecture rapide du sujet afin d'en retirer une vue d'ensemble. Les paragraphes rédigés en italique donnent des explications permettant de situer chaque partie dans son contexte scientifique historique, avec leurs hypothèses d'étude. Les constantes fondamentales intervenant dans le problème sont rappelées ci-dessous avec leurs valeurs numériques données avec 5 chiffres significatifs : charge élémentaire : e = 1,6022.10!19 C charge de l'électron : !"e charge du proton : # e masse de l'électron : me = 9,1094.10!31 kg masse du proton : mp = 1,6726.10!27 kg rayon de Bohr : aB = 5,2919.10!11 m vitesse de la lumière dans le vide : c = 2,9979.108 m.s!1 splitéabilité magnétique du vide : $0 = 4%.10!7 H.m!1 1 permittivité diélectrique du vide :"&0 = = 8,8542.10!12 F.m!1 $0 c 2 constante de Planck : h = 6,6261.10!34 J.s h constante de Planck réduite : ! ' = 1,0546.10!34 J.s 2% 2 m - e2 * ( = 2,1799.10!18 J constante énergétique de Rydberg : Ry ' e2 ++ 2! , 4%& 0 () l'électron-volt, unité d'énergie : 1 eV = 1,6022.10!19 J On donne lexpression du Laplacien en coordonnées cylindriques 2 2 1 / - /f * 1 / f / f 0f (r , . , z ) ' # et lexpression de deux intégrales et leur valeur : +r (# r /r , /r ) r 2 /. 2 / z 2 : 2 pour tout réel r0 > 0 : 1 r exp(!r / r0 ) dr ' r02 0 % 4 10 sin . d. ' 3 . 3 Même si elles ne sont pas systématiquement rappelées dans l'énoncé, le candidat utilisera à son initiative dans cette liste toute constante qu'il jugera nécessaire pour répondre aux questions posées. Les applications numériques demandées seront réalisées avec 4 chiffres significatifs pour les questions Q1 à Q17, puis avec 3 chiffres significatifs à partir de la question Q18. 2/16 Partie I Modèle historique de Bohr de l'atome d'hydrogène (1913) Dans le modèle planétaire de Bohr de l'atome d'hydrogène, l'électron (vu comme ponctuel en M) tourne autour de son proton (lui aussi ponctuel et supposé immobile en O) en décrivant une orbite ! circulaire de rayon r = OM (figure 1). On note u z le vecteur unitaire normal au plan de l'orbite. ! ! L'électron est repéré par ses coordonnées polaires (r,') comme indiqué sur la figure 1 et (ur , u' ) est la base locale correspondante. On néglige l'interaction gravitationnelle entre l'électron et le proton. r O '" M Figure 1 Trajectoire circulaire de l'électron autour du proton supposé immobile Q1. Rappeler l'expression de la force électrique exercée par le proton sur l'électron. Q2. Par l'application du théorème de la quantité de mouvement, déduire la norme v de la vitesse de l'électron en fonction entre autres du rayon r de l'orbite. Q3. Rappeler l'expression de l'énergie potentielle électrostatique Ep de l'électron. Montrer que l'énergie cinétique Ec de l'électron vérifie : Ec ( ! E p / 2 . Q4. Exprimer la norme L du moment cinétique en O de lélectron en fonction de r, me, e, et &0. En 1913, Bohr a postulé que L est un multiple entier de " en posant L ( n ", où n est un entier naturel strictement positif et où " est la constante de Planck réduite. Pour de tels états du modèle de Bohr, dits stationnaires, l'électron, en mouvement circulaire uniforme, bien qu'accéléré, ne rayonne pas d'énergie. Q5. De l'égalité L ( n " , déduire que la relation de quantification du rayon rn de l'orbite caractérisée par l'entier n s'écrit sous la forme rn ( aB n 2 , avec a B le rayon de Bohr, qu'on exprimera en fonction de me, e, &0 et " . Ry Q6. En déduire que lénergie mécanique En de lélectron vaut En ( ! 2 , avec Ry la constante n énergétique de Rydberg. Q7. Quelle est la signification du rayon de Bohr ? Donner la valeur de a B en picomètres et celle de Ry en électron-volts. 3/16 Q8. Donner la vitesse vn de l'électron sur l'orbite caractérisée par l'entier n. On l'exprimera en fonction de n, Ry et me. Donner la valeur numérique de v1 . Le mouvement de l'électron vous semble-t-il relativiste ? Justifier. Partie II Une résolution simplifiée de l'atome de Bohr par l'équation de Schrödinger (1926) On rappelle l'équation de Schrödinger pour une particule non relativiste de masse m décrite par la ! ! fonction d'onde ! (r , t ) dans un champ d'énergie potentielle E p (r ) ! ! ! ! "2 &! ( r , t ) i" %$ #! (r , t ) " E p (r )! (r , t ) &t 2m ! où r désigne le vecteur position d'un point M quelconque de l'espace (M est repéré par ses coordonnées cartésiennes, cylindriques ou sphériques, d'origine O) et # est l'opérateur Laplacien. Q9. On s'intéresse aux états stationnaires d'énergie E de l'électron de l'atome d'hydrogène : on note ! ! ! (r , t ) % ' (r ) e$i E t / " . Écrire l'équation de Schrödinger indépendante du temps concernant la partie spatiale de la ! fonction d'onde ' (r ) (On n'explicitera à ce stade ni la fonction énergie potentielle ni le Laplacien). Afin de simplifier la résolution de l'équation obtenue en Q9, nous nous limiterons à considérer que l'électron n'est spatialement détectable qu'en un lieu de points formé de cercles dans le plan d'équation z = 0, concentriques au point O où se trouve le proton (supposé ponctuel) et avec des rayons de valeurs quantifiées. Les points M où est évaluée la fonction d'onde sont ainsi repérés par leurs coordonnées polaires (r = R,(), d'axe Oz, avec r contraint à prendre des valeurs R discrètes ! (que l'on cherche à déterminer). ' (r ) est alors une fonction continue de la variable ( : on la notera ' (( ) . Q10. Expliciter la fonction énergie potentielle électrostatique de l'électron évoquée à la question Q3 et pour laquelle on impose r = R. Q11. Sachant que Ep = 2E (résultat déduit de Q3), montrer que ' (( ) vérifie l'équation différentielle suivante : " 2 d 2' (( ) % E ' (( ). 2me R 2 d( 2 m R e2 Résoudre cette équation pour les états liés de l'électron en posant ) 2 % e 2 . 4*+ 0 " Q12. En remarquant que ' (( " 2* ) % ' (( ) , déterminer une relation de quantification des valeurs de R, puis des énergies E. Commenter ces résultats. 4/16 Partie III Spectre de raies de l'hydrogène Cette partie nest pas indépendante des précédentes. On rappelle que l'émission de lumière par un atome est due aux transitions entre deux états stationnaires (stationnaires au sens de Bohr (partie I), ou, au choix, au sens de la mécanique quantique (partie II)). Q13. Quelle est l'énergie du photon émis lors de la transition entre un état atomique d'énergie Esup vers un état d'énergie plus faible Einf ? Montrer dans le cas de l'atome d'hydrogène que la longueur d'onde ,nn- de la raie d'émission correspondant à la transition de l'état d'énergie En vers l'état d'énergie En' (avec n' < n) vérifie . 1 1 1 / la relation de Ritz % RH 0 2 $ 2 1 . On explicitera la constante RH en fonction de Ry, h n 3 ,n n2 net c. Q14. Calculer les valeurs numériques des longueurs donde des quatre premières raies d'émission de la série de Balmer prédites par la formule de Ritz, c'est-à-dire les raies correspondant aux transitions des états n = 3, 4, 5, 6 vers létat n' = 2 (représentées et nommées dans la partie gauche de la figure 2 de la partie IV, page 6). Le tableau 1 ci-dessous indique les valeurs expérimentales établies en 1885. Recopiez ce tableau sur votre copie en le complétant par les valeurs numériques précédemment calculées. Les intervalles d'incertitudes expérimentales englobent-ils les valeurs de Ritz ? Nom de la raie H45 H6 H7 H8 656,3 nm 9 0,3 nm 486,1 nm 9 0,2 nm 434,0 nm 9 0,2 nm 410,2 nm 9 0,2 nm ,Ritz ,exp (valeurs de 1885) Tableau 1 Longueurs d'onde des premières raies de la série de Balmer Partie IV Corrections relativistes de Sommerfeld (1916) : introduction de la constante de structure fine Le modèle de Bohr fut un premier succès dans la prévision du spectre démission de l'hydrogène. Mais les progrès de la spectroscopie ont rapidement conduit à observer que certaines raies vues initialement comme monochromatiques présentaient en fait une structure fine sous la forme de multiplets de raies voisines. C'est le cas, par exemple, de la raie H4 qui fut observée comme un doublet par Michelson et Morley dès 1887, mais qui, plus tard, se révèlera être formée de raies plus nombreuses. Sur la partie droite de la figure 2 (page 6) se trouve la carte actuelle simplifiée des niveaux d'énergie et des multiplets de raies qui composent la raie H4 (noter le changement d'échelle: facteur de zoom : 104 par rapport au spectre de la série de Balmer à gauche). La première explication théorique de ces multiplets a été fournie par Sommerfeld en 1916 grâce à e2 , nommée un traitement relativiste amélioré du modèle de Bohr utilisant la constante 4 % 4* +0 " c constante de structure fine. 5/16 Énergie n=6 n=5 n=4 Structure fine simplifiée de la raie H!$ n=3 104 n=2 104 (n pour Q13 et Q14) H- H. H/ Énergie H! Figure 2 Premières raies de la série de Balmer (à gauche) et structure fine (simplifiée) de la raie H!$(à droite) Q15. En explicitant Ry dans l'expression de vn obtenue en Q8, donner ! en fonction de v1 et de c. En déduire la dimension de !. Q16. Donner la valeur numérique de ! , puis celle de son inverse 1 / ! (que l'on utilise bien plus volontiers). Au terme de son calcul, Sommerfeld aboutit à l'expression des niveaux d'énergie En ,l suivants, indicés par deux entiers (n, l) avec n " 1 et l = 0, 1, 2,..., n #$1 : En, l , # Ry * 3 '' 2 1 * n 1 + # ! ( ( % % où ! est la constante de structure fine introduite ci-dessus. n 2 () n 2 ) l + 1 4 & %& Trois années auparavant, Bohr avait trouvé (question Q6) l'expression suivante à un seul indice R entier : En , # 2y . n 6/16 Q17. Commenter la formule de Sommerfeld en liaison avec la formule de Bohr et la faible valeur de !0 Combien de sous-niveaux d'énergie ce calcul prévoit-il pour les niveaux n = 2 et n = 3 de la formule de Bohr ? Q18. Ces sous-niveaux constituent la structure fine de la raie H!$. En reproduisant sur votre copie la partie droite de la figure 2 (page 6), identifier chacun de ces niveaux d'énergie par leurs indices (n, l) respectifs. En déduire, en fonction de Ry et ! , l'expression de l'écart 1E f , E2,1 # E2,0 entre les deux sous-niveaux n = 2. Calculer la valeur numérique de 1E f en électron-volts. Q19. On rappelle que le nombre d'onde 2 d'une radiation est l'inverse de sa longueur d'onde. Exprimer en fonction de h, c, et 1Ef , l'écart 12 , 2 a # 2 b des nombres d'onde 2 a et 2 b des radiations émises lors des deux transitions (a) et (b) suivantes : (a) : obtenue par désexcitation depuis le niveau (n = 3, l = 1) vers le niveau (n = 2, l = 0) (b) : obtenue par désexcitation depuis le niveau (n = 3, l = 1) vers le niveau (n = 2, l = 1). Calculer 12 en cm#1, unité habituelle des spectroscopistes. Immédiatement après l'annonce du résultat négatif de leur expérience consacrée à confirmer l'existence de l'éther luminifère, Michelson et Morley mentionnèrent dans une publication l'observation de la raie H! comme un doublet de nombre d'onde moyen 2 m = 15 237,40 cm#1 et d'écart spectral 12 exp = 0,360 cm#1 (valeurs expérimentales de 1887). Q20. De quelle couleur est ce doublet ? Calculer son écart relatif en nombre d'onde 12 exp / 2 m . Comparer cet écart relatif à celui du doublet jaune du sodium (34 = 589,0 nm et 35 = 589,6 nm). Partie V Résolution interférométrique d'un doublet spectral Les moyens spectroscopiques conventionnels (spectroscope à prisme ou à réseau) peuvent se révéler insuffisants quand il s'agit de résoudre un doublet à très faible écart spectral. On peut alors avoir recours à des méthodes interférométriques. Il est question dans cette partie de l'utilisation de l'interféromètre de Michelson. Le schéma 1 de principe d'un interféromètre de Michelson réglé en lame d'air est donné page 8. On note Ox et Oy deux axes perpendiculaires définissant les directions des deux bras de l'interféromètre. S est une source lumineuse ponctuelle située sur Ox. M1 et M2 sont deux miroirs plans parfaitement réfléchissants, disposés perpendiculairement à Ox en H1 et respectivement à Oy en H2. Le trait incliné à 45°, noté Ls, schématise un groupe de deux lames semi-réfléchissantes à faces parallèles. Ce groupe est supposé n'introduire aucune différence de marche sur les trajets lumineux. Lp désigne une lentille mince convergente placée à la sortie de l'interféromètre de manière à ce que son axe optique soit confondu avec l'axe Oy. Un écran E est placé dans le plan focal image de Lp. On note C le foyer image de Lp. Q21. Nommer les lames qui composent Ls. Qu'est-ce qui les distingue ? Expliquer la nécessité pratique d'utiliser deux lames. 7/16 Q22. Un rayon lumineux, noté (r), émis par S, a été représenté. Reproduire le schéma ci-dessous sur la copie avec SO = OH1 = 2 OH2 et le compléter en faisant un tracé soigné des deux rayons (r1) et (r2) qui émergent de l'interféromètre après division de (r). On laissera apparent tout élément de construction (traits, prolongements de rayons, points remarquables, etc.) justifiant d'un tracé raisonné sans utilisation d'aucun rapporteur d'angle. Tout élément explicatif (noms, positions des points, constructions réalisées...) sera également mentionné. Q23. Sur ce même schéma positionner le miroir fictif M1 justifiant de la dénomination « lame dair » en faisant apparaître le point Q1 intersection de M1 avec les deux prolongements fictifs ad hoc de (r1) et de (r2). Enfin, terminer le tracé des rayons (r1) et (r2) après la lentille Lp jusqu'à l'écran E (on demande comme ci-dessus un tracé raisonné). y M2 H2 Ls H1 S (r) x O M1 Lp E C Schéma 1 Interféromètre de Michelson 8/16 Q24. Indiquer quelle est la forme des franges d'interférences observées sur l'écran (aucune justification n'est demandée). Comment nomme-t-on ces franges ? Q25. En appelant e l'épaisseur de la lame d'air et en prenant l'indice optique de l'air égal à 1, exprimer la différence de marche ! au centre C de l'écran. Q26. On étudie le cas où la source de lumière utilisée présente un doublet spectral de nombres d'ondes "1 et "2. Donner l'expression des ordres d'interférence p1 et p2 en C pour chaque radiation du doublet en fonction de !, "1 et "2. Q27. Pour quelles valeurs de la différence p1 # p2 y-a-t-il brouillage en C ? En pratique la totalité de la figure d'interférences est affectée et on perd la visibilité des franges partout sur l'écran. En déduire, en fonction de l'écart spectral $"%&%"'%#%"(, la variation D! de la différence de marche entre deux situations consécutives de brouillage. Comment nomme-t-on ces situations ? Application numérique : dans le cas du doublet H)%(écart spectral $" exp = 0,360 cm#1), calculer la variation De de l'épaisseur de la lame d'air pour passer d'une situation de brouillage à la situation de brouillage directement consécutive. 130 cm Source de lumière Miroirs Miroirs Verre semi-argenté Epaisse table en pierre 110 cm Verre simple Lunette Miroir ajustable Miroirs Figure 3 Schéma des trajets lumineux dans l'interféromètre de Michelson et Morley de 1887 (source : http://ondes-relativite.info/DominiqueCabala/chap4_histo.htm) 9/16 Q28. À l'entrée de leur interféromètre historique de 1887, Michelson et Morley ont utilisé un dispositif à prismes muni d'une fente pour sélectionner la raie H! présente dans le spectre solaire. Ils ont observé des brouillages périodiques lors de la translation du miroir mobile de leur interféromètre. Partant du contact optique (bras de longueurs rigoureusement égales à L0), ils ont compté un total de 6 brouillages de part et d'autre du contact optique (3 de chaque côté) pour un déplacement du miroir égal à 1/160e de la longueur L0. Calculer la valeur de L0 pour l'interféromètre de Michelson de 1887. Q29. L'interféromètre, construit dans un sous-sol du campus de l'Université de Cleveland aux EtatsUnis, était monté sur une table en granite rectangulaire posée sur un cylindre de bois flottant dans du mercure. La table faisait environ 130 cm " 110 cm de cotés. La longueur L0 des bras de l'interféromètre était synthétisée grâce à deux groupes de miroirs permettant plusieurs allers-retours du faisceau sur chaque voie, comme représenté sur la figure 3 (page 9). À partir de la figure 3 (page 9), donner, en expliquant votre calcul, une estimation grossière de la longueur d'un bras de l'interféromètre. L'ordre de grandeur obtenu est-il en accord avec la valeur L0 trouvée à la question Q28 ? Partie VI Calcul d'une structure fine par l'interaction spin-orbite Une interprétation globale satisfaisante de l'ensemble des spectres observés, ainsi que des dédoublements de raies obtenus lors de l'application d'un champ magnétique extérieur (effet Zeeman), n'a pu voir le jour qu'avec les travaux de Pauli, puis de Goudsmit et Uhlenbeck en 1925 conduisant à introduire le spin. Dans ce cadre nouveau, on explique la structure fine des raies spectrales par une levée de dégénérescence des niveaux d'énergie produite par l'interaction entre le moment magnétique de spin de l'électron et le champ magnétique créé par le proton en mouvement autour de l'électron dans le changement de référentiel. Q30. Dans cette question, on reprend le modèle de Bohr de la partie I, figure 1 page 3 : dans le référentiel du laboratoire, le proton est immobile en O et l'électron décrit une orbite circulaire ! de rayon r centrée sur le proton, à la vitesse v. Exprimer en fonction de r, me, v et u z le moment cinétique orbital en O de l'électron, noté L . ! Q31. En se plaçant dans le référentiel de lélectron, c'est le proton qui est en mouvement circulaire ! autour de l'électron. Donner les expressions du champ magnétique B ressenti par l'électron ! ! dû au mouvement du proton en fonction de #0, e, v, r et u z , puis de #0, e, me, r et L . ! On rappelle à cet effet l'expression du champ magnétique b créé par une spire circulaire de ! # I ! ! courant d'intensité I, d'axe Oz et de rayon r, en son centre : b $ 0 u z , le sens de u z étant 2r relié à celui de I par la "règle du tire-bouchon". ! Q32. On note # s le moment magnétique de spin de l'électron. ! ! e ! On rappelle que # s $ g e % e S où S est le moment cinétique de spin, % e $ & le rapport 2me gyromagnétique de l'électron et ge = 2,0023 le facteur de Landé de l'électron. 10/16 ! On rappelle également que l'énergie potentielle d'un dipôle magnétique # interagissant avec ! ! ! un champ magnétique extérieur B est : E $ & # .B . ! ! On note Eso l'énergie d'interaction de # s avec le champ B (indice "so" pour "spin-orbite"). Montrer que cette énergie dinteraction s'écrit : 3 ! ! a L. S ) , ESO $ g e! 2 Ry * B ' 2 . + r ( " 3 aB ! 2 R y 2 #0 $ On utilisera pour cela l'identité % e , dans laquelle ! est la constante de structure 2"2 fine introduite à la fin du paragraphe en italique de la partie IV (page 5), Ry est la constante énergétique de Rydberg et aB est le rayon de Bohr. ! 1 La projection sur u z du moment cinétique de spin de l'électron est quantifiée : S z $ . " , celle du 2 moment cinétique orbital l'est aussi : Lz $ ml " où ml est un entier relatif tel que & l / ml / l avec l $ 0, 1, 2..., n & 1. Q33. Citer, en la décrivant succinctement (particules utilisées, principe de la manipulation, résultats) l'expérience historique qui a prouvé la quantification du moment cinétique et magnétique. ! ! ! En faisant intervenir le moment cinétique total J $ L 0 S , chaque état atomique est caractérisé par un triplet de nombres (n, l, j) avec n le nombre quantique principal (n 1 1), l le nombre quantique de moment cinétique orbital ( l $ 0, 1, 2..., n & 1 ) et j un troisième nombre (associé à la quantification ! 1 1 1 de J ), tel que j $ si l $ 0 et j $ l & ou l 0 si l 1 1 . 2 2 2 Dans ce modèle à trois nombres quantiques (n, l, j) la formule classique de ESO (obtenue en Q32) doit être remplacée par la forme suivante !! 3 ) , ! ! a .S L , ) E SO ,n , l , j $ g e! 2 R y * 222 3 n , l (r ) 2 * B ' d 3 r ' 2 ' " * + r ( ( + 2 !! , ! 3)" avec L.S $ * j ( j 0 1) & l (l 0 1) & ' , l'intégrale triple portant sur tout l'espace, 3 n ,l (r ) désignant 4( 2 + ! la valeur de la fonction d'onde de l'électron au point de l'espace repéré par le vecteur position r ! dans un système de coordonnées sphériques avec pour origine le proton et d 3r étant la notation couramment utilisée pour désigner un élément de volume. Avec les notations 4 r , 6 , 7 5 habituelles (utilisées par exemple dans le document 1, en annexe, ! page 14) : d 3r $ r 2 sin 6 dr d6 d7 . 3 3 ! ,a ) Q34. Commenter le remplacement de la quantité * B ' par l'intégrale 222 3 n , l (r ) + r ( Calculer cette intégrale pour n = 2 et l = 1. , r ) 1 1 r ! sin 6 exp * & On donne pour cela : 3 2,1 (r ) $ '. 3/2 (4aB ) - aB + 2aB ( 11/16 2 , a ) 3! * B' d r. + r ( Q35. On s'intéresse à la structure fine du niveau n = 2 de l'atome d'hydrogène. Faire un décompte des différents états (2, l, j) possibles et exprimer en fonction de ge, ! et Ry leurs énergies d'interaction spin-orbite correspondantes. On note E somin, n " 2 (respectivement E somax , n " 2 ) la plus petite (respectivement la plus grande) des valeurs prises par Eso dans le cas où n = 2. min Donner l'expression de la différence $Eso , n " 2 " Esomax , n " 2 # E so , n " 2 en fonction de ge, ! et Ry. L'introduction du spin par Uhlenbeck et Goudsmith en 1925 a permis d'expliquer la levée de dégénérescence des niveaux d'énergie (structure fine et effet Zeeman), mais il subsistait une difficulté pour l'écart des niveaux de la structure fine : la valeur calculée en considérant un facteur de Landé ge ! 2 pour l'électron conduisait au double de la valeur attendue. On retrouvait le bon résultat si on posait ge = 1, mais c'était alors l'effet Zeeman qui était incorrectement traité. En 1927, Llewellyn Thomas parvint à montrer que la valeur ge ! 2 n'est à remettre en question pour aucun des deux effets, mais qu'il faut corriger l'expression de l'interaction spinorbite dans le référentiel du laboratoire par un facteur 1/2 à cause d'un effet relativiste. Ce résultat (appelé précession de Thomas) a définitivement démêlé le lien étroit entre spin et relativité. Donner l'expression corrigée de $Eso , n " 2 après l'analyse de Thomas. La comparer à $Ef trouvée en Q18 à partir de la formule de Sommerfeld. Partie VII Encore plus fin (!) : la structure hyperfine du niveau fondamental de l'atome d'hydrogène Après plusieurs années passées à étudier la structure de la Voie lactée par des moyens optiques, l'astronome néerlandais Jan Oort réalisa l'importance d'une fenêtre d'observation dans le domaine des ondes radio afin de contourner le problème de l'absorption de la lumière visible par les nuages de poussière galactiques. L'hydrogène étant l'élément le plus abondant dans l'univers, Oort demanda à son élève H.-C. Van de Hulst d'étudier la possibilité d'une raie spectrale dans le domaine radio en rapport avec l'hydrogène. Celui-ci aboutit en 1944 à la prévision d'une raie due à la structure hyperfine du niveau fondamental de l'atome d'hydrogène. Cette raie, appelée raie de l'hydrogène à 21 cm, a été observée pour la première fois en 1951 par Ewen et Purcell. Cette nouvelle fenêtre d'observation astronomique a permis de découvrir la forme spirale des bras de notre galaxie. À l'aide notamment des documents 1, 2, 3 et 4 fournis en annexe (pages 14 à 16), répondre aux questions suivantes. Q36. Justifier le choix et la valeur de la fréquence suggérée par Morrison et Cocconi (document 4). Calculer, en électron-volts, l'écart en énergie $Ehf exp (indice "exp" pour expérimental) entre les deux niveaux hyperfins de l'atome d'hydrogène impliqués dans la raie à 21 cm (en fait 21,1 cm pour être plus précis)% 12/16 Q37. Rappeler l'unité de moment magnétique dans le Système International. On appelle magnéton de Bohr (&B), respectivement magnéton nucléaire (&N), la norme du moment magnétique de spin de l'électron, respectivement du proton. Donner les valeurs numériques de &B et de &N. Q38. Établir une formule (classique) d'estimation de l'écart énergétique entre les deux niveaux hyperfins de l'état fondamental de l'atome d'hydrogène (on prendra le rayon de Bohr aB comme la distance séparant le proton de l'électron). On attend une expression $Ehf,classique faisant intervenir &0, &B, &N, et aB . Q39. La résolution de l'équation de Schrödinger donne en fait $Ehf = (16/3) ' $Ehf,classique. Application numérique : calculer $Ehf. La valeur trouvée est-elle cohérente avec la valeur expérimentale $Ehf exp de la question Q36 ? Q40. Il est indiqué dans le document 4 (page 16) que la longueur d'onde 21 cm peut servir d'unité de mesure. Pouvez-vous citer un exemple de transition hyperfine intervenant dans la définition d'une unité SI ? FIN 13/16 ANNEXE - Documents utiles pour la partie VII Document 1 Expression du champ magnétique créé en un point M de coordonnées sphériques ! ! (!"#"$) par un moment magnétique ! " ! u z : z ! ! ( 2 ! cos* ! ! sin * ! % B ( r ,* , , ) " 0 & ur ) u* # r3 4+ ' r 3 $ M *0 r y O ,0 x Document 2 Rappels de mécanique quantique et tableau de valeurs pour l'électron et le proton ! ! Le moment magnétique de spin ! et le moment cinétique de spin S d'une particule sont liés par la ! ! formule ! " g - S où - est le rapport gyromagnétique de la particule et g son facteur de Landé. Particule Moment cinétique de spin Sz (en projection sur un axe Oz quelconque) Rapport gyromagnétique Facteur de Landé Électron Proton 1 . " 2 1 . " 2 -e " / e 2me g e = 2,0023 14/16 -p " e 2m p g p = 5,5857 Document 3 Extrait de texte sur la structure hyperfine, consultable à l'adresse suivante : http://www.futura-sciences.com/sciences/actualites/physique-raie-21-cm-cle-astrophysique-cosmologie L'atome d'hydrogène possède des niveaux d'énergie hyperfins résultant de l'interaction entre le moment magnétique de spin de son électron (appelé magnéton de Bohr) et le moment magnétique de spin de son proton (appelé magnéton nucléaire). Selon que ces deux spins sont parallèles ou antiparallèles, le niveau d'énergie de l'atome n'est pas le même et une transition avec émission d'un photon d'une longueur d'onde de 21 cm est possible. Une transition quantique dans l'atome d'hydrogène + + Copyright © 2005 Pearson Prentice Hall, Inc. 15/16 Document 4 La raie à 21 cm !" un moyen de communication avec une éventuelle intelligence extraterrestre ? En 1959 Morrison et Cocconi suggérèrent que la meilleure fréquence pour chercher des signaux provenant de sources extraterrestres intelligentes serait 1420 MHz. Dans le cadre du programme américain SETI (acronyme pour "search for extra-terrestrial intelligence") mis en place dans les années 1960, les premiers signaux émis depuis la Terre pour établir un contact avec une éventuelle intelligence extraterrestre ont été envoyés en 1974 par le grand radiotélescope situé à Arecibo (Puerto Rico). Plusieurs sondes spatiales (Pioneer 10, Voyager 1 et Voyager 2) ont également été lancées dans le but d'explorer des régions externes au système solaire. Sur la sonde Pioneer 10, lancée le 2 mars 1972, une plaque en aluminium anodisé a été fixée, comportant une gravure pouvant servir de message. Bien qu'aucune communication avec Pioneer 10 ne soit plus possible depuis janvier 2003, la sonde poursuit actuellement son voyage au-delà du système solaire... 16/16 I M P R I M E R I E N A T I O N A L E 18 1055 D'après documents fournis La plaque montre un homme et une femme à l'échelle de la sonde et la position du Soleil (position of Sun) par rapport à 14 pulsars et au centre de la Galaxie. En haut à gauche, une représentation de la transition hyperfine de l'atome d'hydrogène donne une longueur d'onde de 21 cm, qui peut servir d'unité de mesure. Ainsi, la hauteur de la femme à droite est donnée en numérotation binaire comme étant 8 fois la longueur d'onde de la raie de l'hydrogène (binary equivalent of decimal 8). Les pulsars sont identifiables par leur fréquence de rotation en binaire, exprimée comme un multiple entier de celle de la raie dhydrogène. En bas, le Système solaire et la planète d'origine de la sonde sont représentés avec les distances relatives des planètes (planets of Solar System and binary relative distances), également en numérotation binaire. © Nasa
