Mines Chimie MP 2012
| Thème de l'épreuve | Le dibrome |
| Principaux outils utilisés | atomistique, cristallographie, diagramme potentiel-pH, cinétique |
| Mots clefs | dibrome |
Corrigé
:👈 gratuite pour tous les corrigés si tu crées un compte
👈 l'accès aux indications de tous les corrigés ne coûte que 1 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - -
👈 gratuite pour ce corrigé si tu crées un compte
- - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)




Rapport du jury
(télécharger le PDF)


Énoncé obtenu par reconnaissance optique des caractères
A 2012 Chimie MP
ECOLE DES PONTS PARISTECH,
SUPAERO (ISAE), ENSTA PARISTECH,
TELECOM PARISTECH, MINES PARISTECH,
MINES DE SAINT-ETIENNE, MINES DE NANCY,
TELECOM BRETAGNE, ENSAE PARISTECH (FILIERE MP)
ECOLE POLYTECHNIQUE (FILIERE TSI)
CONCOURS D'ADMISSION 2012
EPREUVE DE CHIMIE
Filière : MP
Durée de l'épreuve : 1 heure 30 minutes
L'usage d'ordinateur ou de calculatrice est interdit
Sujet mis à la disposition des concours :
Cycle International, ENSTIM, TELECOM INT, TPE-EIVP.
Les candidats sont priés de mentionner de façon apparente sur la première page
de la copie :
CHIMIE 2012-Filière MP
Cet énoncé comporte 8 pages de texte.
Si au cours de l'épreuve, un candidat repère ce qui lui semble être une erreur
d'énoncé, il est invité à le
signaler sur sa copie et à poursuivre sa composition en expliquant les raisons
des initiatives qu'il aura
été amené à prendre.
DEBUT DE L'ENONCE
LE DIBROME
Des données utiles pour la résolution du problème sont fournies à la fin de
l'énoncé.
A température ambiante, le dibrome de formule Br2 est un liquide brun-orangé
très volatil
dégageant des vapeurs toxiques de même couleur. Le sujet, composé de deux
parties
indépendantes, s intéresse successivement aux caractéristiques du dibrome dans
ses différents
états (solide, liquide et gazeux) et aux caractéristiques cinétique et
thermodynamique d'une
réaction permettant la synthèse de dibrome en laboratoire.
Page 1/8 Tournez la page S.V.P.
Chimie 2012 - Filière MP
A) Le dibrome dans ses différents états
L'atome de brome et la molécule de dibrome :
1- Rappeler les règles générales permettant d'établir la configuration
électronique d'un
atome dans l'état fondamental et les appliquer à l'atome de brome. Souligner
les électrons de
valence.
2- En déduire la position du brome dans la classification périodique. A quelle
famille
chimique appartient-il ? Citer un autre élément appartenant àla même famille.
3- Citer deux propriétés communes aux éléments appartenant à cette famille
chimique.
4- Proposer une formule de Lewis pour la molécule de dibrome.
Le dibrome à l'état liquide et gazeux:
5- Justifier la couleur du dibrome en vous servant de son spectre d'absorption,
donné ci-
après.
250 300 350 400 450 500 550 600
Figure 1: spectre d'absorption du dibrome gazeux
Structure cristalline du dibrome solide :
Le dibrome cristallise dans une maille faces centrées ayant la forme d'un
paralléle'pipe'de rectangle (structure dite orthorhombique). Chaque noeud du
réseau est
occupé par l'entité Br2. Les paramètres de maille ont pour valeurs
approximatives :
a = 0,4 nm ; b = 0,7nm; c = 0,9 nm.
6- Dessiner cette maille, combien de molécules Brz contient-elle ? Justifier.
7- Donner l'expression de la masse volumique du dibrome solide. Faire
l'application
numérique (en unités SI.) et comparer a la masse volumique de l'eau.
Page 2/ 8
Chimie 2012 -- Filière MP
B) Etude thermodynamique et cinétique d'une réaction de synthèse du dibrome en
laboratoire.
Cette partie s'intéresse aux caractéristiques thermodynamique et cinétique d
'une
réaction permettant la synthèse de dibrome en laboratoire. Le dibrome peut
ainsi être
synthétisé juste avant d 'être utilisé, ce qui évite la conservation risquée de
flacons de
dibrome.
Etude préliminaire du diagramme potentiel-pH du brome :
Le diagramme potentiel--pH simplifié de ! élément brome figure 2) a été élaboré
en
considérant les espèces Br2(aq), Br_(aq), BrO3_(aq) et HBrO3(...Ï). Aux
frontières, toutes les espèces
ont même concentration de travail c..., = 1,0.10'3 mol.L'].
1,0 2,0 3,0 4,0 5,0 6,0 7,0 8,0
Figure 2 : Diagramme potentiel --pH du brome a 298 K
8- Déterminer le degré d'oxydation du brome dans les espèces considérées.
9- Attribuer les différents domaines du diagramme potentiel-pH en justifiant
votre
raisonnement.
10- Calculer la valeur du potentiel à la frontière entre les domaines A et B.
11- Déterminer le pKa du couple HBrO3(a®/Br03_(w. Justifier.
Page 3/8 Tournez la page S.V.P.
Chimie 2012 - Filière MP
12- Déterminer par le calcul la valeur de la pente de la frontière entre les
domaines A et C
puis vérifier la cohérence avec le diagramme.
13- D'après le diagramme potentiel--pH, l'espèce B n'a pas de domaine de
prédominance
en milieu basique. Donner une explication à ce phénomène.
Le dibrome peut être synthétisé en laboratoire en faisant réagir du bromate de
sodium
(NaBrO3) et du bromure de sodium (NaBr). L équation de la réaction est la
suivante :
BI"O3_(aq) + 5 Bf_(aq) + 6 H30+ : 3 BI'2(aq) + 9 H20(1) (I)
14- Comment s'appelle ce type de réaction d'oxydo-réduction ?
15- Ecrire les demi--équations électroniques relatives aux deux couples redox
intervenant
dans la réaction (1).
Etude thermodynamique de la réaction (1) :
On effectue la synthèse du dibrome en mélangeant un même volume d'une solution
de
bromate de sodium (NaBrO3) de concentration 2,0.10'3 mol.LJ et d'une solution
de bromure
de sodium (NaBr) de concentration 1,0.10'2 mol.L'l. Une coloration brune
apparaît après un
certain temps.
16- Montrer, sans calcul, que la réaction (1) est quantitative dans un domaine
de pH dont
on précisera les bornes.
17- La réaction (1) est réalisée dans des conditions où on constate que 90% des
ions
bromate ont réagi une fois l'équilibre atteint. Déterminer la concentration en
espèces bromées
et la valeur du pH à l'équilibre.
Etude cinétique de la réaction (1) :
L 'étude cinétique de la réaction (I) montre que la réaction admet un ordre
vis-d-vis de
chacun des réactifs. On se propose de déterminer les ordres partiels de
réaction ainsi que la
constante de vitesse.
On notera respectivement a, b et c les ordres partiels des espèces BrO3_(aq),
Br_(aq) et
H3O+, et k la constante de vitesse de la réaction. On considérera que les
ordres restent
inchangés tout au long de la réaction.
18- Exprimer la vitesse volumique de la réaction en fonction des concentrations
des
espèces considérées, des ordres partiels et de la constante de vitesse.
Page 4/ 8
Chimie 2012 - Filière MP
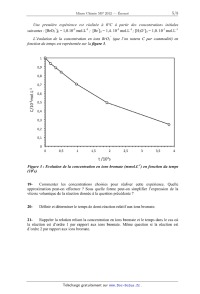
Une première expérience est réalisée à 0°C à partir des concentrations initiales
suivantes .- [Bro3']0 = 1,0.10'3 mol.L" ; [Bf]0 = 1,4. ..."1 mol.L" ; [H3o+]0 =
1,0. ..."1 mol.L"
L'évolution de la concentration en ions BrO3_ (que l 'on notera C par
commodité) en
fonction du temps est représentée sur la figure 3.
fÇ,i"1Ü3r'HIÜI.L1
0 0,5 1 1,5 l 2 5 3 3 5 11
t ;"1ü3s
Figure 3 : Evolution de la concentration en ions bromate (mmol.L"} en fonction
du temps
(nfs)
19- Commenter les concentrations choisies pour réaliser cette expérience. Quelle
approximation peut-on effectuer ? Sous quelle forme peut-on simplifier
l'expression de la
vitesse volumique de la réaction donnée àla question précédente ?
20- Définir et déterminer le temps de demi-réaction relatif aux ions bromate.
21- Rappeler la relation reliant la concentration en ions bromate et le temps
dans le cas où
la réaction est d'ordre 1 par rapport aux ions bromate. Même question si la
réaction est
d'ordre 2 par rapport aux ions bromate.
Page 5/8 Tournez la page S.V.P.
Chimie 2012 -- Filière MP
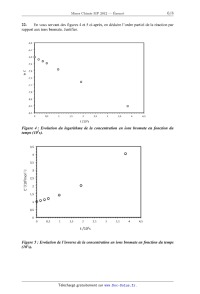
22- En vous servant des figures 4 et 5 ci-après, en déduire l'ordre partiel de
la réaction par
rapport aux ions bromate. Justifier.
lnC
a 0,5 1 1,5 2 2,5 3 3,5 4 4,5
t/lÛ3s
Figure 4 : Evolution du logarithme de la concentration en ions bromate en
fonction du
temps (llfs).
C'1/103mùl'1.|
0 0,5 1 1,5 2 2,5 3 3,5 4 4,5
t ;" 1Ü35
Figure 5 : Evolution de l'inverse de la concentration en ions bromate en
fonction du temps
(10%).
Page 6/ 8
Chimie 2012 -- Filière MP
Plusieurs autres expériences ont été réalisées à 0°C pour une même concentration
initiale en ions bromate [BrO{]o = 1,0.10'3 mol.L'l et pour des concentrations
variables en
ions bromure et oxonium. Dans chaque expérience, la vitesse initiale a été
déterminée. Les
résultats sont rassemblés dans le tableau suivant :
[Br--]o (mol.L'1) [H3O+]o (mol.L'1) Vitesse initiale (mol.L'l.s'1)
N°1 0,10 0,10 4,110"5
0,15 0,10 6,2.10'5
0,10 0,20 16,4.10'5
23- Déterminer l'ordre partiel par rapport aux ions bromures et l'ordre partiel
par rapport
aux ions H3O+.
24- Calculer la constante de vitesse k de la réaction. Préciser clairement son
unité.
Données :
Constante d'Avogadro : NA= 6,0.1023 mol'l.
Constante des gaz parfaits :R= 8,3 J .K'l.mol'1
Constante de Nernst à 298 K : Æln10 = 0,06V
F
Z(Br)=35
M(Br)= 80g/mol
Cercle chromatique simplifié :
Pourpre
Rouge : {_}-- Violet :
z620-800nm " "' OE4OO-410nm
Orange : Bleu :
z580-620 nm z410-480 nm
Jaune : Bleu cyan:
z560 - 580 nm z480 -490 nm
Vert:
% 490-560 nm
Page 7/8 Tournez la page S.V.P.
Chimie 2012 - Filière MP
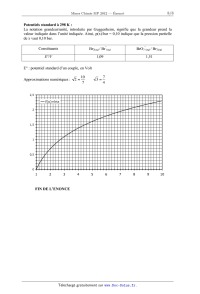
Potentiels standard à 298 K :
La notation grandeur/unité, introduite par Guggenheim, signifie que la grandeur
prend la
valeur indiquée dans l'unité indiquée. Ainsi, p(X)/bar = 0,10 indique que la
pression partielle
de X vaut 0,10 bar.
Constituants BI"2(aq) / Br_(aq) B1'03_(aq) / BI"2(aq)
E°/V 1,09 1,51
EO : potentiel standard d'un couple, en Volt
. . _ 1
Approxnnaüons numér1ques : \/_ ... 70 \/5 z 1
FIN DE L'ENONCE
Page 8/ 8
