e3a Physique et Modélisation PSI 2016
| Thème de l'épreuve | Citerne de gazole et chimie des carburants |
| Principaux outils utilisés | électrostatique, électronique, mécanique des fluides, solutions aqueuses, cinétique chimique, oxydoréduction, diagrammes E-pH, thermodynamique |
| Mots clefs | citerne, vidange, condensateur plan, pertes de charge, carburant, gazole, combustion, polluant |
Corrigé
: 👈 gratuite pour tous les corrigés si tu crées un compte👈 l'accès aux indications de tous les corrigés ne coûte que 5 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)














Rapport du jury
(télécharger le PDF)


Énoncé obtenu par reconnaissance optique des caractères
119
CONCOURS ARTS ET MÉTIERS ParisTech - ESTP - POLYTECH
Épreuve de Physique - Chimie PSI
Durée 4 h
Si, au cours de l'épreuve, un candidat repère ce qui lui semble être une erreur
d'énoncé, d'une
part il le signale au chef de salle, d'autre part il le signale sur sa copie et
poursuit sa
composition en indiquant les raisons des initiatives qu'il est amené à prendre.
L'usage de
L'usage de calculatrices est autorisé.
AVERTISSEMENT
Remarques préliminaires importantes : il est rappelé aux candidat(e)s que
! Les explications qualitatives des phénomènes étudiés interviennent dans la
notation au même titre que les développements analytiques et les applications
numériques ; les résultats exprimés sans unité ne sont pas comptabilisés ;
! Tout au long de l'énoncé, les paragraphes en italique ont pour objet d'aider
à la
compréhension du problème ;
! Tout résultat fourni dans l'énoncé peut être admis et utilisé par la suite,
même
s'il n'a pas été démontré par le(la) candidat(e) ;
! Les questions comportant le verbe "calculer" demandent une application
numérique ;
! Les données numériques nécessaires à la résolution sont regroupées en fin
d'énoncé ;
! Le document réponse devra être complété puis remis avec la copie.
La présentation, la lisibilité, l'orthographe, la qualité de la rédaction, la
clarté et la
précision des raisonnements entreront pour une part importante dans
l'appréciation
des copies. En particulier, les résultats non justifiés ne seront pas pris en
compte. Les
candidats sont invités à encadrer les résultats de leurs calculs.
Tournez la page S.V.P
A
Il est interdit aux candidats de signer leur composition ou d'y mettre un signe
quelconque pouvant indiquer sa provenance.
Tournez la page S.V.P.
"
"
Le problème est constitué de trois parties totalement indépendantes.
La première consiste en létude dun capteur de niveau de gazole dans une
citerne. La seconde
sintéresse à la vidange dune telle citerne de gazole. La dernière partie de
cette épreuve est consacrée
à la chimie des carburants.
Ce sujet comporte 16 pages dont un document-réponse à rendre avec la copie
(Annexe 3)
PREMIÈRE PARTIE
CAPTEUR de NIVEAU
FORMULAIRE DANALYSE VECTORIELLE
Composition dopérateurs :
(
(
)
)
(
(
!!!" !!!!!"
"
rot grad f = 0
!!!!!"
div grad f = f
)
!!!" "
div rot a = 0
!!!" !!!" "
!!!!!"
" " "
rot rot a = grad ( div a ) - a
)
A / Champ électrostatique dun condensateur plan
Considérons 2 plaques métalliques planes, de surface S, perpendiculaires à laxe
(Ox), caractérisées par
les abscisses respectives x = 0 et x = e et portées respectivement aux
potentiels V1 et V2.
Nous supposerons que les dimensions transversales de ces plaques sont assez
grandes pour pouvoir
négliger les effets de bord. Ainsi nous supposerons que le potentiel entre les
2 plaques ne dépend que de
x et sécrit V(x).
En outre, on suppose que ces 2 plaques constituent un condensateur : lespace
entre ces 2 armatures est
vide et elles portent des charges électriques opposées (Q2 = -Q1 avec Q2 charge
portée par la plaque
dabscisse x = e).
A1. Etablir léquation vérifiée par le potentiel V(x) entre les plaques du
condensateur.
A2. Résoudre cette équation en utilisant les potentiels V1 et V2 et la distance
e.
"
A3. En déduire une première expression du champ électrostatique E entre les 2
plaques à laide de V1, V2
et e.
Quelles sont les propriétés de ce champ ? Quelle est lallure des lignes de
champ en supposant
V1>V2 ?
!"
"
!
A4. Le champ étant nul à lextérieur, établir une deuxième expression du champ
électrostatique E entre les
2 plaques en fonction de Q1, S et 0 où 0 est la permittivité du vide.
A5. En déduire lexpression de la capacité C0 du condensateur plan à laide de e,
S et 0.
B / Capacité du capteur
On souhaite mesurer la hauteur h de gazole dans une citerne à laide dun capteur
capacitif. Ce dernier
peut être assimilé à un condensateur plan de capacité C(h), fonction de h et
constitué de 2 armatures
rectangulaires en cuivre de hauteur H, de largeur L et distantes de e.
H correspond également à la hauteur maximale de gazole dans la citerne.
Lespace entre les armatures est rempli en partie de gazole sur une hauteur h et
en partie dair.
*(+&),&'
*$,-&,."+&/)'
"()'
'$
#$
#$
!"#$%&'
%$
%$
&$
On admet que la capacité dun condensateur plan rempli dun isolant de
permittivité relative r vaut
S
C= 0 r "
e
B1. Montrer que lassociation en parallèle de deux condensateurs de capacités C1
et C2 est équivalente à
un seul condensateur de capacité Ceq = C1 + C2 .
B2. En déduire lexpression de C(h) en fonction de h, H, L, e, r (permittivité
relative du gazole) et 0.
B3. Vérifier que C(h) peut sécrire numériquement suivant la formule suivante :
C(h) = 118.(1,00 + 4,00.h) avec C(h) en pF et h en m
Calculer les valeurs Cmin et Cmax de C(h) quand la citerne est respectivement
vide et pleine.
!
Tournez
la page
S.V.P.
Tournez
la page
S.V.P.
C / Chaine de mesure
La chaine de mesure est décrite de manière synoptique sur le schéma ci-dessous.
Lobjectif est dobtenir
une tension v3(t) proportionnelle à C(h).
,"
#$%&'()"
#$%$#*&*+"
45,6"
+*.&)'""
0-1-2&$3.'"
,-).-/'"
!"#$%&
!'#$%&
478"
8"
!(#$%"
Un monostable est un circuit possédant deux états en sortie. Un état stable
(durée indéfinie) et un état
instable de durée T0 fixe. Le passage à l'état instable se produit sous l'effet
d'une impulsion de
commande délivrée par le signal dhorloge de période T = 2,00 ms et dont létat
haut a une durée très
petite devant T (voir document ci-après). On impose T0 < T. Le condensateur étudié en partie B est inséré dans le circuit électronique (non étudié ici) du monostable ; on admet que dans ces conditions T0 (appelée durée propre du monostable) est proportionnelle à C(h) : T0 = R.C(h) où R est un facteur de proportionnalité. La notice technique du monostable indique par ailleurs quen fonctionnement normal : · T0 est supérieure à 10,0 µs · La bascule de létat stable à létat instable se réalise quasi-instantanément sur front montant du signal dhorloge. · La bascule de létat instable à létat stable se réalise quasi-instantanément au bout dun temps T0 · Létat instable en sortie a pour valeur U0 = 5,00 V ; létat stable en sortie a pour valeur 0,00 V. C1. Expliquer qualitativement pourquoi il est nécessaire dimposer T0 < T. C2. Déterminer la plage de variation de R pour que le monostable fonctionne correctement. C3. On choisit dorénavant R = 2,00 M. Déterminer la plage de variation de T0 lors du fonctionnement du capteur capacitif. !" " C4. Tracer sur la copie, en justifiant, une allure du graphe de v2(t) pour t entre 0 et 2T en y plaçant U0, T0 et T. C5. Etablir lexpression de la valeur moyenne V2moy de v2(t) à laide de U0, T et T0. En déduire la plage de variation de V2moy lors du fonctionnement du capteur capacitif. C6. On désire obtenir en sortie du filtre mentionné dans le schéma synoptique v3(t) = V2moy. Proposer un montage simple, constitué dun conducteur ohmique de résistance R1 = 220 k et dun condensateur de capacité C1, réalisant cette opération. Déterminer une condition sur la valeur numérique de C1 afin dobtenir en sortie du filtre cette valeur moyenne. On souhaite visualiser le résultat de la mesure de h à laide dun afficheur numérique. Pour cela, on utilise préalablement un CAN (convertisseur analogique numérique) permettant la numérisation de la tension v3 en un nombre N binaire exprimé sur 8 bits. La valeur maximale admise en entrée du CAN est Vmax = 5,00 V. La valeur minimale est 0,00 V. C7. Que vaut le pas (ou quantum) q du CAN ? C8. En déduire la plus petite variation de hauteur de liquide h mesurable. C9. Que vaut la valeur Nmin de N (exprimé en base 10) quand la citerne est vide ? Que vaut la valeur Nmax de N (exprimé en base 10) quand la citerne est pleine ? On se restreint au cas particulier où T0 = 1,00 ms. On donne la décomposition en série de Fourier de la tension v2(t) : v2 (t ) = V2,moy + 2 U0 1 2 " ! ' 2k + 1sin #% ( 2k + 1) T t &$ k =0 C10. En raisonnant uniquement sur la première harmonique de v2(t) (c'est-à-dire k = 0), déterminer une condition sur C1 de manière à ce que la fluctuation de v3(t) due à cette harmonique nengendre pas en sortie du CAN de modification de la valeur du nombre binaire N correspondant à V2moy. DEUXIEME PARTIE VIDANGE de la CITERNE D / Ecoulement parfait La citerne est munie dun orifice par lequel le gazole peut sécouler. On suppose que toutes les conditions sont réunies pour quon puisse appliquer la relation de Bernoulli entre un point A de la surface libre du gazole et un point B au niveau de louverture (voir figure ci-après) : 1 VB2 -VA2 + g ( zB - zA ) + ( pB - pA ) = 0 " 2 ( ) où est la masse volumique du gazole, VA (respectivement VB) correspond à la vitesse moyenne (encore appelée vitesse débitante) de lécoulement supposée constante au niveau de la section SA (respectivement SB), pA (respectivement pB) correspond à la pression de lécoulement supposée constante au niveau de la section SA (respectivement SB), g est lintensité du champ de pesanteur. ! Tournez la page S.V.P. Tournez la page S.V.P. #' 1)2&*.&' SA : section de la citerne au niveau du point A (en m²) ()*''+'%"',*&--)$.'/0' #" (' ·" !"#$%&' $" SB : section de lorifice découlement au niveau du point B (en m²) SB << SA " 3'4'5&'%6")*'+'%"',*&--)$.'/0'' ·" 7' D1. Quelles sont les conditions dapplication de la relation de Bernoulli ? D2. Comment se traduit la conservation de la masse lors de lécoulement ? En déduire une relation entre les vitesses moyennes en A et B. D3. Sachant que la section en A est nettement plus grande que celle en B, exprimer la vitesse moyenne VB de lécoulement en B à laide de h et g. D4. La citerne est initialement pleine. Exprimer le temps nécessaire T pour la vidanger complètement, à laide de SA, SB, H et g. Calculer T. E / Prise en compte dune perte de charge singulière Au niveau du convergent (rétrécissement de section sur la ligne de courant AB), on constate une zone de perturbation caractérisée énergétiquement par une « perte de charge singulière » : le bilan dénergie se traduit par une perte dénergie mécanique volumique modélisable par la formule suivante : 1 1 VB2 -VA2 + g ( zB - zA ) + ( pB - pA ) = - KC VB2 2 2 ( ) avec Kc 0,55 (sans dimension) E1. Déterminer une nouvelle expression de VB en tenant compte de la perte de charge singulière. E2. Exprimer à nouveau le temps nécessaire T pour vidanger complètement la citerne, à laide de T et Kc. Calculer T. Commenter. !" " F / Prise en compte dune perte de charge régulière On accroche au niveau de B une conduite cylindrique verticale de grande longueur et de diamètre d = 2a. La figure ci-contre ne représente quune portion ! =C1C2 de cette conduite. Létude de lécoulement entre C1 et C2 nécessite alors la prise en compte de la dissipation dénergie par frottement dû à la viscosité du gazole. Dans la suite, on considère que le gazole est un fluide incompressible, de masse volumique constante , de viscosité dynamique , en écoulement stationnaire. On suppose de plus que lécoulement est laminaire et que le champ de vitesse est à symétrie cylindrique " " " V ( r ) = V ( r ) ez avec V(r) > 0 et une vitesse nulle le long des parois et maximale sur laxe de
la conduite. Les pressions
sont supposées constantes pour une altitude donnée : pC1 est la pression en C1
à laltitude zC1, pC2 est la
pression en C2 à laltitude zC2.
&"
&"
#%"
'"
#%"
'"
*"
!"
()%"
#$"
#$"
&#$"
"
""""" "! "
!"
!"
On isole par la pensée un cylindre de fluide de rayon r inférieur à a et de
longueur ! #"Ce cylindre subit des
forces pressantes en C1 et C2, son poids et des forces visqueuses modélisées
par la loi suivante :
"
dV "
f =
ez "
dr
Où "représente la surface latérale de contact entre le fluide contenu dans le
cylindre et celui à lextérieur
du cylindre.
!
Tournezlala
page
S.V.P.
Tournez
page
S.V.P.
F1. Faire un bilan de quantité de mouvement pour ce cylindre et établir la
relation suivante :"""
dV
= - ( p!C1 - p!C2 ) r """
dr
avec p! = p + gz "et un facteur que lon exprimera à laide de et "
#"$%&&'()'*"+'",-.('"/'".
! r2 "
!C1 - p!C 2 ) .
V
r
=
V
F2. Montrer que V(r) sécrit : ( )
max #1- 2 $ . Exprimer Vmax à laide de , a et ( p
a
%
&
F3. Déterminer lexpression du débit volumique QV à laide de , a et ( p!C1 - p!C
2 ) .
F4. En déduire lexpression de la vitesse moyenne Vmoy dans une section de la
conduite (encore appelée
vitesse débitante) à laide de , a et ( p!C1 - p!C 2 ) .
La « perte de charge régulière » (due à la dissipation dénergie à cause des
frottements visqueux) est
définie par pr =
1 2 !
V
2 moy d
où " est une constante sans dimension dépendant de la nature de
lécoulement et de la rugosité de la conduite," " la longueur de la conduite et
d son diamètre.
# -p
# = -p "pour une canalisation de section constante."
C1
r
On a par ailleurs:" pC2
F5. Déterminer lexpression de à laide de , , Vmoy et a.
F6. Rappeler lexpression du nombre de Reynolds Re pour une conduite cylindrique
en fonction de son
diamètre d, de la vitesse moyenne Vmoy, de la masse volumique et de la
viscosité .
Pour un écoulement laminaire, en déduire lexpression de à laide du nombre de
Reynolds, Re.
F7. Calculer le nombre de Reynolds Re à laide des données numériques fournies
en fin de sujet.
F8. Rappeler comment le nombre de Reynolds, Re peut être utilisé pour
caractériser la nature de
lécoulement.
Lhypothèse découlement laminaire utilisée jusquà la question F7 est-elle valide
?
G / Remplissage du réservoir dune voiture
On utilise une pompe centrifuge pour déplacer le gazole de la citerne au
réservoir dune voiture. Le schéma
suivant modélise simplement le circuit du fluide (la citerne étant enterrée, on
a bien évidemment zE > zA)
La « perte de charge singulière » (due à la dissipation dénergie à cause des
coudes, des raccords entre
canalisations de diamètres différents...) est définie par ps = K
1
2
Vmoy
où K est une constante sans
2
dimension dépendant de la nature de la singularité rencontrée. On admettra que
la pompe utilisée ici
génère une perte de charge singulière de coefficient Kpompe = 6.
!"
"
G1. Utiliser le document, page 12, intitulé « Données numériques » pour
déterminer la valeur numérique du
coefficient Ktotal correspondant à lensemble des singularités détaillées sur le
schéma ci-dessus. On
prendra soin de préciser les différents termes intervenant dans Ktotal.
G2. Calculer la valeur totale des pertes de charge singulières
fournies en fin de sujet.
ps ,tot à laide des données numériques
G3. La totalité des longueurs droites de la conduite vaut approximativement ! =
10 m.
On admettra la valeur suivante pour le coefficient de perte de charge régulière
: = 2,45.10-2.
Calculer la valeur totale des pertes de charge régulières
fournies en fin de sujet.
pr ,tot à laide des données numériques
Linsertion dun élément actif (ici la pompe électrique) dans le circuit du
fluide modifie le bilan énergétique
appliqué au gazole. En tenant compte des pertes de charge, on admet la relation
suivante appliquée entre
les points A et E :
1
P
VE2 -VA2 + g ( zE - zA ) + ( pE - pA ) = - ( pr ,tot + ps,tot ) + u
2
QV
(
)
"
où Pu est la puissance utile fournie par la pompe au fluide et QV est le débit
volumique.
G4. Calculer le débit volumique dans les conduites QV à laide des données
numériques fournies.
G5. Sachant que la pompe a un rendement de 80%, déterminer lexpression de Pe,
puissance électrique
alimentant la pompe. Calculer Pe (on prendra zE - zA 5 m).
!
Tournez
la page
S.V.P.
Tournez
la page
S.V.P.
TROISIEME PARTIE
AUTOUR DE LA CHIMIE DES CARBURANTS
H / Etude de la combustion complète du gazole
Lire le texte fourni en ANNEXE 1 et intitulé « la combustion des carburants »
puis répondre aux questions
suivantes.
H1. Ecrire la réaction de combustion complète de gazole dans lair : les
affirmations des lignes 15 à 19
sont-elles valides ?
H2. Le taux démission de CO2 (indiqué sur le document 2 en ANNEXE 1) est-il en
accord avec la
consommation du véhicule ?
H3. Vérifier quil sagit dune réaction doxydoréduction. Quelle est la molécule
oxydée ? Justifier.
H4. Déterminer lenthalpie standard de réaction associée à cette transformation
chimique. On fera le calcul
à partir dune équation de réaction écrite pour un coefficient de 1 pour le
gazole. Laffirmation des lignes
21 à 25 est-elle valide ?
H5. Justifier thermodynamiquement que la réaction est totale à 298 K.
H6. Déterminer et calculer la température de flamme adiabatique maximale TF
liée à cette transformation.
H7. La température de flamme réellement atteinte est en général plus faible.
Proposer des explications.
I / Etude de quelques polluants azotés
I1. Daprès le texte, quelle est la cause de la présence de polluants composés
doxygène et dazote dans
les gaz déchappement des véhicules ?
La transformation suivante est une des nombreuses transformations se déroulant
dans les gaz
déchappement des moteurs à explosion :
NO2 + CO ! NO + CO2
On souhaite étudier la cinétique de la transformation. Dans ce but, on réalise
plusieurs expériences à
différentes concentrations initiales et on mesure la vitesse initiale de la
réaction. Les résultats sont reportés
dans le tableau ci-dessous.
Expérience
Concentration initiale en
NO2 (mol.L-1)
Concentration initiale en
CO (mol.L-1)
Vitesse initiale
(mol.L-1.s-1)
1
0,1
0,1
0,5.10-2
2
0,1
0,4
8,0.10-2
3
0,2
0,1
0,5.10-2
I2. Déterminer les ordres partiels par rapport à chacun des réactifs.
Donner une valeur numérique de la constante de vitesse.
I3. Proposer une formule de Lewis pour chacune des entités intervenant dans
cette transformation.
!"#
#
Dans latmosphère, le dioxyde dazote NO2 entre dans une chaine de plusieurs
réactions menant à la
fabrication dozone O3, gaz toxique. On obtient par ailleurs de nombreux
produits dérivés et notamment du
pentaoxyde de diazote N2O5.!En atmosphère humide, N2O5 réagit au cours dun
mécanisme non détaillé ici
mais dont le bilan est le suivant :
N2O5 (g) + H2O(liq) ! 2 NO3- (aq) + 2 H+ (aq)
On obtient donc une solution aqueuse dacide nitrique. Cette réaction
atmosphérique (supposée totale)
amplifiée par les polluants issus des pots déchappement contribue au phénomène
des pluies acides.
On souhaite ici utiliser cette réaction pour déterminer la concentration en N2O5
(g)
présent dans les gaz
déchappement dun moteur thermique dun groupe électrogène alimenté avec du
gazole. Pour cela, on fait
barboter 1 m3 de gaz déchappement dans un 1L deau. On admet que la totalité des
nitrates NO3- se
retrouve en solution aqueuse acide. On souhaite alors doser les nitrates NO3-
(aq) suivant le protocole décrit
en ANNEXE 2.
I4. Dans le cadre dun diagramme potentiel-pH, déterminer léquation de la droite
donnant les variations du
potentiel du couple NO3-(aq) / NO2-(aq) en fonction du pH. On prendra [NO3-(aq)
] = [NO2-(aq)] comme
convention de frontière.
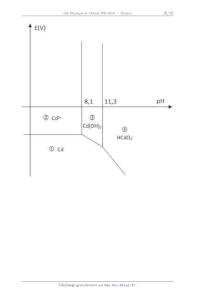
I5. Calculer le coefficient directeur de la frontière oblique séparant les
domaines ! et " du diagramme
potentiel pH simplifié du Cadmium.
I6. En utilisant le document-réponse (en fin de sujet en ANNEXE 3 et à rendre
avec la copie), justifier
graphiquement que la réaction entre le cadmium métallique et les ions nitrate
est quantitative.
Ecrire léquation de la transformation chimique correspondante, en milieu acide.
I7. Pourquoi a-t-on choisi une longueur donde de 540 nm ?
I8. La loi de Beer-Lambert est-elle vérifiée au cours du protocole réalisé ?
I9. Déterminer la concentration massique en acide nitrique initialement présent
dans la solution S0.
En déduire la concentration massique initiale en N2O5 (exprimée en mg par m3 de
gaz déchappement).
Fin de lépreuve.
!!
Tournez
la page
S.V.P.
Tournez
la page
S.V.P.
DONNEES NUMÉRIQUES
Pour la première partie:
0 = 8,85.10-12 F.m-1
r = 5,00
H = 1,00 m
L = 4,00 cm
e = 3,00 mm
Permittivité du vide :
Permittivité relative du gazole :
Hauteur du capteur capacitif :
Largeur du capteur capacitif :
Distance entre les armatures :
Pour la seconde partie:
Section de la citerne au point A :
Section de louverture au point B :
Rayon des sections des conduites et des coudes :
Intensité du champ de pesanteur :
Masse volumique du gazole :
Viscosité dynamique du gazole :
Vitesse moyenne des les conduites :
SA = 1,00 m²
SB = 1,00.10-3 m²
a = 1,80 cm
g = 9,81 m.s-2
= 840 kg.m-3
= 5.10-3 kg.m-1.s-1
Vmoy = 4,50 m.s-1
Coefficient K pour les pertes de charge singulière :
#
#
Coude brusque :
Coude arrondi de rayon de courbure RC et de diamètre d ( est en
degré) :
#
#
#
Pour la troisième partie:
Eléments chimiques :
Elément
Masse molaire
atomique (g.mol-1)
Numéro atomique
Electronégativité
(échelle de Pauling)
H
C
N
O
1,0
12,0
14,0
16,0
1
6
7
8
2,20
2,55
3,04
3,44
Formule chimique de lair : 3,7 mol de N2 pour 1,0 mol de O2
Données thermodynamiques : constante thermodynamique R = 8,314 J.mol-1.K-1
composé
fH0 (kJ.mol-1)
0
-1
-1
CPm (J.mol .K )
0
-1
-1
Sm (J.mol .K )
gazole (liq)
O2 (vap)
CO2 (vap)
H2O(vap)
N2(vap)
- 245
0
- 393
- 242
224,6
29,4
44,2
30,0
0
27,9
329
205
214
189
192
où fH0, CPm0 et Sm0 sont respectivement lenthalpies standard de formation, la
capacité thermique
molaire standard (à pression constante) et lentropie molaire standard des
espèces à 298 K (ces
grandeurs sont supposées constantes).
!"#
#
ANNEXE 1 :
DOCUMENT 1 : Texte extrait du site de lassociation adilca : www.adilca.com ©
Association pour la Diffusion d'Informations sur les Lois physiques de
l'Automobile.
Association à but non lucratif créée en mai 2000 à l'initiative d'anciens
élèves des sections
scientifiques du Conservatoire National des Arts et Métiers de Paris.
LA COMBUSTION DES CARBURANTS
Les carburants
#$
!%$
Cest la proportion des composants qui permet de distinguer les carburants.
Lanalyse en laboratoire dun échantillon de gazole pur non additivé montre que
celui-ci est
constitué (en masse) de 87 % de carbone (symbole chimique C) et 13 % dhydrogène
(symbole
chimique H) [...]
Ces proportions permettent détablir les formules chimiques fictives de chacun
de ces carburants,
formules qui seront utilisées par la suite pour calculer tous les autres
paramètres de la
combustion. Ainsi, le gazole a pour formule chimique fictive C7,25H13, lessence
C7H16, le GPL
C3,5H9.
La combustion des hydrocarbures
!#$
La stoechiométrie désigne létude des proportions idéales déléments qui
autorisent une réaction
chimique complète, propre et sans gaspillage.
Les lois de la stoechiométrie appliquées à la combustion des hydrocarbures nous
montrent que
pour brûler 1 kg de gazole, il faut disposer de 14,3 kg dair (soit, étant donné
la composition de
lair, 10,9 kg de diazote et 3,4 kg de dioxygène) ; la réaction produit 10,9 kg
de diazote (ce gaz
étant chimiquement neutre, il na pas participé à la combustion), 3,2 kg de
dioxyde de carbone
(CO2) et 1,2 kg deau (H2O). [...]
&%$
Lénergie libérée par la combustion
&#$
Connaissant la composition massique dun hydrocarbure, il est alors facile den
déduire lénergie
quil peut libérer lors de sa combustion la combustion dun kg de gazole de
formule C7,25H13 libère
une énergie nette denviron 42 millions de joules, soit, compte tenu de la masse
volumique du
produit (840 kg.m-3), environ 35 millions de joules par litre [...]
La combustion en conditions réelles
"%$
"#$
Sagissant de la combustion des carburants dans le cadre du fonctionnement dun
moteur
dautomobile, une stoechiométrie parfaite est toujours difficile à garantir.
En effet, non seulement le carburant peut présenter des différences de
composition selon les
pays et les distributeurs, mais en plus, la masse dair introduite dans le
moteur, jamais
parfaitement pure, varie en permanence en fonction de la température ambiante
et de la pression
atmosphérique.
Les rejets polluants
Lorsque les lois de la stoechiométrie sont respectées, les gaz déchappement ne
contiennent que
de lazote gazeux (N2), du dioxyde de carbone (CO2) et de leau à létat de vapeur
(H2O). Mais
que se passe-t-il lorsque les lois de la stoechiométrie ne sont plus respectées
?
!"
Tournez la
Tournez
lapage
pageS.V.P.
S.V.P.
"$#
"%#
%$#
Pour simplifier le problème, considérons deux configurations opposées : mélange
riche (trop de
carburant, pas assez dair) et mélange pauvre (peu de carburant, trop dair).
Dans la première configuration, certains atomes qui constituent la molécule
dhydrocarbure ne
trouvent pas de partenaire oxygène en nombre suffisant puisque lair manque, ils
ne sont donc
pas oxydés complètement et se retrouvent dans les gaz déchappement sous forme
de particules
carbonées, dhydrocarbures imbrûlés (symbole chimique HC) ou de monoxyde de
carbone
(symbole chimique CO), gaz quil ne faut surtout pas confondre avec le CO2 : lun
est très
toxique, lautre pas du tout.
Dans la seconde configuration, un excès dair (cest toujours le cas lorsque le
moteur est
suralimenté) fortement comprimé à température élevée (cest particulièrement le
cas des moteurs
diesel) peut entraîner la formation de monoxyde dazote (symbole chimique NO),
suite à une
réaction entre loxygène (O2) et lazote (N2) de lair aspiré. Une fois expulsé,
le monoxyde dazote
présente la particularité de se transformer spontanément en dioxyde dazote
(symbole chimique
NO2), générant au passage une mutation de loxygène atmosphérique en ozone
(symbole
chimique O3), deux gaz très toxiques pour les organismes vivants.
DOCUMENT 2 : Fiche technique partielle dune voiture diesel :
Réservoir : 45 L
Consommation moyenne : 4,5 L aux 100 kms
Emission de CO2 : 121 g / km
!"#
#
ANNEXE 2 :
Dosage des nitrates NO3- (aq) dans une solution acide.
La solution S0 à doser a un volume dun litre et a été obtenue en faisant
barboter 1 m3 de gaz de
pot déchappement.
! Mode opératoire :
1) Faire passer la totalité de la solution S0 dans une colonne à
chromatographie contenant des
grains de Cadmium métallique Cd.
2) Prélever précisément 50 mL du filtrat et les placer dans une fiole jaugée de
100 mL. Ajouter
précisément 1 mL de solution de réactif R0 fournie par le labo. La solution se
colore en rose.
Compléter au trait de jauge.
A partir dune solution mère (appelée S1) acide et contenant des ions nitrates de
concentration connue, on a fabriqué (au laboratoire) plusieurs solutions filles
par dilution
successives auxquelles on a appliqué le même protocole expérimental. Elles sont
nommées
S2, S3, S4 et S5.
3) Régler le spectrophotomètre sur la longueur donde égale à 540 nm puis faire
« le blanc » à
leau distillée. Mesurer labsorbance des solutions traitées à partir de S1, S2,
S3, S4, S5 et S0.
! Tableau des résultats :
Solution
Concentration
massique initiale
en nitrate (mg/L)
Absorbance A
Eau
distillée
S5
S4
S3
S2
S1
S0
0
0,20
0,40
0,60
0,80
1,00
?
0,000
0,127
0,254
0,382
0,509
0,636
0,231
! Documents et données complémentaires :
· Potentiel standard du couple NO3- / NO2- :
E° = 0,94 V
· Allure du diagramme potentiel-pH simplifié
du Cadmium
&'()#
· Réaction entre les nitrites NO2-(aq) et R0 :
NO2-(aq)
+ R0 " P0
*+!#
$
Réaction totale et mole à mole
R0 et P0 sont des espèces non explicitées
(formules non utiles)
-.+/0#
!!+,#
%#
12'5%)3#
$%#
&#
%1253-#
P0 est la seule espèce absorbante : elle est
colorée en rose
""#
#
#
!"
Tournez la page S.V.P.
Document-réponse, à compléter et à rendre avec la copie
!"#
Il est interdit aux candidats de signer leur composition ou d'y mettre un signe
quelconque pouvant indiquer