CCINP Physique 2 PSI 2004
| Thème de l'épreuve | Matériaux et procédés dans l'industrie électronucléaire. Différents types de moteurs. |
| Principaux outils utilisés | diagrammes d'Ellingham, diagrammes potentiel-pH, courbes intensité-potentiel, thermochimie, oxydoréduction, solutions aqueuses, cycles thermodynamiques, électrocinétique, systèmes mécaniques en rotation |
| Mots clefs | moteur à, explosion, loi de Laplace, diagramme de Watt, diagramme de Clapeyron, gaz parfait, rendement, moteur a courant continu, hacheur, couplage, électromécanique, loi des mailles, théorème de l'énergie cinétique, oscillogrammes, effet Joule, moteur synchrone |
Corrigé
: 👈 gratuite pour tous les corrigés si tu crées un compte👈 l'accès aux indications de tous les corrigés ne coûte que 5 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)














Énoncé obtenu par reconnaissance optique des caractères
SESSION 2004
. PSIP209
CONCOURS (0MMUNS POlYÏECNNIOUES
EPREUVE SPECIFIQUE -- FILIERE PSI
PHYSIQUE 2
Durée : 4 heures
Les calculatrices sont autorisées.
***
N. B. : Le candidat attachera la plus grande importance à la clarté, à la
précision et àla concision de la rédaction.
Si un candidat est amené à repérer ce qui peut lui sembler être une erreur d
'énonce', il le signalera sur sa copie et devra
poursuivre sa composition en expliquant les raisons des initiatives qu 'il a
été amené à prendre.
***
L'épreuve comporte un problème de physique et un problème de chimie. Les
candidats traiteront les
deux problèmes dans-l'ordre de leur choix et les rédigeront de façon séparée.
Le sujet comporte 15
pages et un document-réponse à joindre à la copie.
Durées approximatives : chimie - 2 heures
physique - 2 heures
PROBLÈME DE CHIMIE
MATÉRIAUX ET PROCÉDÉS DANS L'INDUSTRIE ÉLECTRONUCLÉAIRE
L'industrie électronucléaire française utilise en grande majorité des réacteurs
à eau pressurisée dans
lesquels le combustible est de le dioxyde d'uranium, sous forme de pastilles
contenues dans une
gaine en alliage de zirconium, l'ensemble étant immergé dans de l'eau servant
de fluide caloporteur.
Les trois parties de ce problème s'intéressent successivement au combustible, à
la gaine et à l'eau
de refroidissement.
1. Le combustible
A partir de la pechblende U308, minerai principal d'uranium, On prépare une
solution aqueuse de
sulfate d'uraner UO;SO.; qu'on transforme en diuranate de diammonium (NH4)2U207
puis en
trioxyde d'uranium. Ce dernier est réduit par le dihydrogène pour donner U02
solide. Ce composé
ne peut servir de combustible nucléaire que s'il est enrichi en isotope 235U,
fissile, alors que
l'isotope 238U, majoritaire, ne l'est pas. Pour ce faire, on traite U02 par le
fluorure d'hydrogène pour
former UF4 gazeux qu'on fait réagir avec le difluor pour obtenir UF6 azeux. Ce
dernier est soumis
à un procédé de diffusion gazeuse qui permet d'amener la teneur en 23 UF6 de
0,7% à plusieurs pour
cent. L'hexafluorure ainsi enrichi est réduit par le dihydrogène en présence de
vapeur d'eau ; on
obtient ainsi U02 enrichi qui est mis en forme pOur donner les pastilles
utilisables dans les
réacteurs.
Question 1 (QI): Quel est le nombre de protons dans 235U, dans 238U ? Quel est
le nombre
d'oxydation de l'uranium dans U02 , U03 , UOzSO4 ?
Q2 : Quels sont les trois ions présents dans U30g supposé purement ionique ?
Q3: Quelle est la forme de la molécule UF6 ? Quel est l'angle de liaison
F--U--F dans cette
molécule ?
Q4 : Le dioxyde d'uranium cristallise dans le système cubique. A partir de sa
masse volumique,
déterminer la multiplicité de sa maille (nombre de groupements formulaires par
maille).
On s'intéresse à la réduction des oxydes d'uranium par le dihydrogène.
QS : En utilisant les données thermodynamiques données au @ IV,tracer les
droites d'Ellingham
relatives aux trois couples UO3/U30g, U30g/U02 et U02/U (bilans tous rapportés
à la consommation
d'une mole de molécules 02).
On présentera distinctement ]les expressions des lois affines A,G°-- - f(T)
relatives a chacun de ces
couples, exprimées en ]. mol--', et on effectuera le tracé sur la Figure 1 du
document-- --réponse annexé
à ce sujet, qui devra être joint à la copie. On indiquera clairement sur le
diagramme la formule de
chaque phase solide dans son domaine d'existence.
Q6: Déduire du diagramme ce qui se passe si on chauffe UO3 sous P(Oz) : 1 bar ?
A quelle
température ? (On se contentera de la précision de la solution graphique). -
Q7: Rappeler la variance du système gazeux H2- 02- H20à al'équilibre dans le
cas général.
Observer la position sur le diagramme de la droite d' Ellingham relative au
couple HzO/Hz avec
P(H20) : P(H2) : 1 bar ; déduire de la position de cette droite la phase solide
obtenue à l'équilibre
quand on soumet UO3 à un tel mélange H20/H2 en excès, à la température de 1 000
K. Pourquoi la
pression partielle de dioxygène n'est-elle alors pas quelconque '?
Q8 : Placer dans le diagramme la droite relative au couple H20/Hz dans les
conditions de pression
de ces deux gaz où la réduction des oxydes d'uranium à 1 000 K va jusqu'à
l'uranium métal. Quand
on fixe la pression de dihydrogène à 1 bar, quelle est la pression maximale de
vapeur d'eau que doit
contenir le dihydrogène pour obtenir, à cette température, l'uranium métal '?
(On pourra égaler les
pressions partielles de dioxygène des deux couples mis en jeu et on s'aidera du
diagramme en se
contentant de la précision de lecture sur l'axe des ordonnées. On rappelle que
la droite HzO/Hz
tracée dans le diagramme l'est, comme toutes les droites d'Ellingham, pour une
mole 02 échangée).
Conclure sur la possibilité industrielle d'une telle réduction.
II. La gaine
Les gaines de zirconium (en fait un alliage peu chargé en éléments mineurs) se
présentent sous la
forme de tubes très longs dans lesquels sont empilées les pastilles de
combustible. Le zirconium a
été choisi en raiSon de sa très grande transparence aux neutrons produits par
la fission,
contrairement au hafnium, son homologue supérieur dans la colonne IV de la
classification
périodique, qui absorbe très fortement les neutrons et qui doit impérativement
être éliminé du
zirconium (zirconium dit « déhafnié »).
Q9 : Quelle est la structure électronique du zirconium '? Quel est le numéro
atomique du hafnium ?
On étudie les propriétés du zirconium métal en présence d'eau à température
ordinaire. Les espèces
considérées sont le zirconium métal (Zr)s, le cation zirconium (Zr4+)aq, la
zircone: dioxyde de
zirconium (ZrOz)s, l'anion (HZrO{),....
Q10 : Quel est le nom complet de l'anion (HZrO{)aq ?
Q11 : Au degré d'oxydation + IV, calculer les limites de stabilité en pH de la
zircone solide, du
côté acide (équilibre avec Zr4+) et du côté basique (équilibre avec HZrO{). On
considérera que les
espèces dissoutes du zirconium sont à la concentration de 1 x 10"6 mol.L".
SChématiser le résultat
de ces calculs par un diagramme de prédominance uniaxe.
Q12 : Dans chacun des trois domaines de pH où l'espèce prédominante du
zirconium (IV) est ainsi
définie, écrire l'équilibre entre cette espèce et le métal. Appliquer la loi de
Nemst et préciser
l'évolution avec le pH du potentiel de chacun des couples Considérés (on ne
calculera pas les
potentiels standard inconnus). On considérera, comme à la question précédente,
une concentration
de 1 >< IO"6 mol.L'l pour les espèces dissoutes. Q13 : Tracer le diagramme potentiel--pH pour cette concentration sur la Figure 2 du document- réponse annexé au présent sujet, qui devra être remis avec la copie. Placer dans chaque domaine ainsi défini le nom de l'espèce prédominante. Observer la position de la droite de réduction de l'eau et conclure quant à l'éventuelle corrosion du zirconium dans l'eau. Q14 : En situation industrielle, on utilise le zirconium dans son domaine_de passivation. Fournir deux adjectifs qualifiant un produit de corrosion pour que le matériau métallique qui lui donne naissance soit protégé par une passivation efficace. Dans le cas du zirconium, on calculera les volumes molaires .(2 de (ZrOz)s et de (Zr),, puis le facteur d'expansion volumique f, défini ainsi : QZr0 2 f: r La valeur trouvée pour le coefficient d'expansion volumique de formation de la zircone à partir du zirconium permet de conclure à une très bonne efficacité de la passivation. Pourquoi '? Q15 : Quel commentaire pouvez-vous faire concernant le type des contraintes mécaniques qui apparaissent alors dans l'oxyde ? En situation de corrosion accélérée, on observe une perte de passivité; comment imaginez-vous le mécanisme de cette perte de passivité quand la couche d'oxyde s'épaissit ? Q16 : Tracer l'allure du diagramme intensité-potentiel à pH : 0 (domaine de corrosiOn) pour une électrode de zirconium immergée dans un électrolyte indifférent (par exemple NaZSO4 0,1 mol.L"'). Même question à pH : 6 (domaine de passivation). On représentera en traits pointillés les demi-- réactions d'oxydation et de réduction et en traits pleins les courbes résultantes. On précisera de façon claire les équations des demi-réactions redox représentées. III. Le milieu aqueux caloporteur L'eau de refroidissement des assemblages-combustible contient de l'acide borique H3BO3 (6,18 g.L"), qui assure, par son atome de bore, une absorption d'une partie des neutrons émis par la fission. Q17 : Quelle est la structure électronique de l'atome de bore ? En déduire la formule développée de H3B03. Quelle est la forme de cette molécule ? Q18: L'acide borique est un monoacide faible. Quel est le pH à 298 K d'une solution aqueuse contenant 6,18 g.L" d'acide borique ? Q19: En fait, l'exploitant des centrales nucléaires & fixé à 8 la valeur de pH optimale, où la solubilité des divers produits susceptibles d'apparaître est minimale. Que proposez--vous d'ajouter au milieu pour atteindre cette valeur ? IV. DONNÉES : Numéros atomiques : H:,1 ; B:5 ; O:8 ; Zr:40 ; U:92. Masses molaires atomiques (g.mol' 1) : H: 1,0 ; B = 10,8 ; 0: 16,0 ; Zr=91,2 ; U=238,}0. Constante des gaz parfaits : R = 8,314 J.K"'.mol" Nombre d'Avogadro : N = 6,023 x 1023 mol--1 Enthalpies standard de formation à 298 K (AfH°298 en U .mol'l) : U03 :- 1 223,8 ; U30g : -- 3 574,8 ; U02 : -- 1 085,0 Entropies standard à 298 K (S°... en J.K".mol'l) : U : 50,2 ; UO3 : 96,1 ; U30g : 282,6 ; U02 : 77,0 ; 02 : 205,2 ; (H20)g : 188,8 ; Hz : 130,5. Maille cristalline : U02 : cubique ; paramètre de maille : a = 546,82 pm. Masses volumiques : U02 : 10,96 x 103 kg.m"3 ; Zr : 6,5 >< 103 kg.nf3 ; ZrO; : 5,6 >< 103 kg...."3 Constantes d'équilibre à 298 K : (Zf'")aq + 4 01r : (Zr02)s+ 2 H20 ' log K1 : 55,12 (ZrOz)s + OH" : - (HZrO{)... log K2 : -- 4,80 Potentiel redox standard à 298 K : . (Zr4+)aq / (Zr)s : e° : -- 1,44 V/ESH Constante à 298 K : RT ln lO/Î= 0,06 V Constante d'acidité : H3BO3 N H2B03' + H+ pKa : 9,2 Fin du Problème de Chimie. PROBLEME DE PHYSIQUE DIFFERENTS TYPES DE MOTEURS Le sujet comporte trois parties qui peuvent être traitées indépendamment. Dans chaque partie, le candidat pourra trouver des questions pouvant également être traitées indépendamment. PREMIERE PARTIE MODELE D'UN MOTEUR D'AUTOMOBILE A EXPLOSION . Le cycle à « quatre temps » d'un cylindre d'un moteur à explosion d'automobile peut être décrit de façon simplifiée par le cycle classique de Beau de Rochas. On se propose d'étudier la validité de ce modèle de cycle et d'évaluer, à partir des données techniques d'un constructeur (et en particulier de la consommation) le rendement et la puissance. La puissance sera comparée à celle annoncée dans la notice technique. On décompose un cycle de fonctionnement en quatre phases correspondant chacune à un aller simple du piston (il s'agit des « quatre temps » du moteur). Premier temps: étape EA (admission) En E, le piston est en position haute (le volume disponible est VE). La soupape d'admission s'ouvre. Le mélange air-carburant entre dans le cylindre à pression atmosphérique supposée constante (PE : 105 Pa) et température constante (température d'admission : TE : 80°C). En A, le piston est en position basse (le volume disponible est VA). Deuxième temps : étape AB (compression) La soupape d'admission se ferme et le piston comprime le mélange: l'étape AB est une compression adiabatique réversible du mélange qui amène le piston en position haute. On note PB la pression du mélange en B. Troisième temps : étapes BC et CD (explosion et détente) En B, une étincelle provoque la combustion exothermique du mélange : la pression passe quasi-- instantanément de PB à PC à volume constant. L'étape CD est une détente adiabatique réversible du mélange (mélange air et gaz brûlés). En D, le piston est en position basse (le volume disponible est VA). Quatrième temps : étapes DA et AE (échappement) En D, la soupape d'échappement s'ouvre sur l'atmosphère. DA est une transformation quasi-instantanée à volume constant: en A, le gaz est ramené à la pression atmosphérique. Pendant cette transformation DA, on suppose que le gaz n'a pas le temps de s'échapper (la quantité de gaz reste donc constante pendant cette transformation). Au cours de l'étape AE, le gaz est expulsé dans l'atmosphère à pression et température constantes. Simplification du cycle : On ne tiendra pas compte des étapes EA et AE au cours desquelles le système constitué par le gaz contenu dans un cylindre est un système ouvert. On considérera que tout se passe comme si : - dans chaque cylindre, une quantité de gaz constituant un système fermé décrivait indéfiniment le cycle ABCDA _ -- le transfert thermique reçu par le fluide était issu d'une source chaude fictive (alors qu'il provient d'une réaction chimique interne). On supposera, dans tout le problème, que l'automobile roule à 90 km/h en 5ème vitesse. La vitesse du véhicule est évidemment proportionnelle àla vitesse de rotation de l'arbre moteur. On donne ci--dessous des données extraites de la notice technique d'une automobile (moteur classique à quatre cylindres) : - dimensions du cylindre : alésage x course du piston : 80 mm x 80 mm -- cylindrée (4 cylindres) : 1400 cm3 (la cylindrée correspond donc à 4(VA -- VE) ) -- rapport volumétrique : a : VA/VE : 10 - vitesse pour 1000 tr/mn (en 5ème vitesse) : 30 km/h - consommation (en litres de carburant pour 100 km effectués à 90 km/h en 5ème vitesse) : 5 L 60 - Figure 1 : courbe P(Q) de la puissance mécanique (en kW) en fonction de la vitesse de rotation de l'arbre moteur (en tours/minute) 50 40 30 Puissance en kW 20 10 0 0 1000 2000 3000 4000 5000 6000 7000 Vitesse en tours/minute Figure 1 Données et hypothèses relatives au carburant et au mélange : Nature du carburant : * - formule brute CgH18 - masse molaire MC : 114 g/mol - masse volumique p = 720 kg/m3 -- la combustion du carburant fournit un transfert thermique de 6.103 kJ/mole. L'air étant fortement en excès par rapport au carburant, on assimilera, pour tout le cycle, le mélange à un gaz parfait diatomigue de coefficient isentropigue y : cp/cv : 1,4_ et de masse molaire M = 29 g/mol. Rappels : - constante de Boltzmann : k : 1,38.10'23 J.K'1 - constante des gaz parfaits : R = 8,31 J.mol".K" On étudie dans ce qui suit le cycle suivi par le mélange gazeux contenu dans un cylindre. 1.1. Tracer l'allure du cycle ABCDA dans le diagramme de Watt (pression en ordonnée, volume en ' ' abscisse). « 1.2. Transformation AB : 1.2.1. A partir des données techniques du constructeur et sachant que le véhicule roule à 90 km/h, déterminer la durée tAB de la compression AB sachant que l'arbre moteur effectue deux tours lors d'un cycle complet. 1.2.2. Quelle hypothèse relative à la transformation AB le résultat trouvé permet--il de valider ? 1.2.3. Le mélange étant assimilé à un gaz parfait diatomique, on rappelle que l'énergie cinétique moyenne d'une molécule vaut 5/2 kT (où T est la température absolue en kelvins). Donner dans ces conditions un ordre de grandeur de la vitesse moyenne d'agitation thermique des molécules dans l'état A. 1.2.4. En comparant cette vitesse à la vitesse moyenne du piston au cours de la transformation AB, quelle hypothèse relative à la transformation AB peut--on ainsi admettre '? 1.2.5. Déterminer littéralement puis numériquement la pression PB et la température TB (on donnera le résultat en degré Celsius) du mélange gazeux dans l'état B. 1.3. Transformation BC : 1.3.1. En présentant clairement les étapes du calcul, calculer en litres puis en mol la quantité de carburant consommée par cycle et par cylindre (on notera nc le nombre de moles et on rappelle que le moteur comporte quatre cylindres). 1.3.2. En déduire le transfert thermique QBC fourni dans un cylindre par la combustion du carburant. 1.3.3. Ce transfert thermique est reçu par le mélange contenu dans un cylindre. Déterminer littéralement puis numériquement : a) le nombre de moles n de mélange contenu dans un cylindre, b) la température TC (résultat en degré Celsius) et la pression PC du mélange dans l'état C. 1.4. Transformation CD : Même question (température TD et pression PD du mélange) pour l'état D. 1.5. Déterminer littéralement et numériquement le travail fourni par le gaz au cours d'un cycle. 1.6. Rendement : 1.6.1. Donner la définition du rendement thermodynamique n du moteur. 1.6.2. a) Exprimer n en fonction uniquement des températures T A, TB, TC et T9. b) En déduire la valeur numérique du rendement. 1.7. Puissance : On se place toujours dans les mêmes conditions (5ème vitesse, 90 km/h). On considère maintenant le moteur constitué de ses quatre cylindres. 1.7.1. Déterminer la puissance P,}, du moteur à partir des résultats de l'étude théorique précédente (questions 1.2. à 1.5.) . 1.7.2. Déterminer la puissance P du moteur à partir de la courbe P(Q) du constructeur. 1.7.3. Comment justifier que l'on trouve P... < P '? DEUXIEME PARTIE MOTEUR A COURANT CONTINU - COMMANDE PAR UN HACHEUR On s'intéresse maintenant à l'utilisation d'un moteur électrique à courant continu en traction automobile. On rappelle (figure 2) le schéma équivalent du moteur à courant continu à excitation séparée : u représente la tension aux bornes de l'induit (rotor), i l'intensité du courant le traversant. 2.1. Etude du moteur à courant continu Le moteur étant soumis à un couple résistant constant Cr : 60 N .m , un essai réalisé avec u : 120V a donné les résultats suivants : -- f.é.m. E = 100 V - vitesse de rotation 0 = 3200 tourslminute Figure 2 - Le moment d'inertie de la partie mobile entraînée par le moteur vaut ] = 1,5 kg.m2 et la relation entre la vitesse de rotation du moteur et la vitesse v du véhicule est : o= >..v avec À=35tr.mn"/(km.h").
2.1.1. Rappeler les relations (expressions littérales puis numériques) existant
entre les grandeurs
électriques E et i et mécaniques Q et C (C : couple moteur); pour les
expressions
numériques, on précisera les unités employées pour E, i, Q et C.
2.1.2. Déterminer la valeur de R, résistance de l'induit.
2.1.3. On considère un fonctionnement à couple moteur C constant (C = 60 Nm )
et on étudie la
phase de << mise en vitesse » d'un véhicule sur une route horizontale. Le moment du couple résistant varie alors suivant une loi du type Cr : aQ + b avec a = 0,01 N.m/ (rad.s") et b = 5 N.m . ' Calculer le temps At1 mis par le véhicule pour passer de 0 à V = 50 km/h. 2.2. Commande par hacheur Pour alimenter le moteur à courant continu à partir d'une source (batteries) délivrant une tension continue fixe Eg, on réalise le montage à deux interrupteurs K; et K2 de la figure 3. Une bobine d'inductance L est placée en série avec le moteur. La résistance de la bobine est négligée. . ...«nu...-.........-.........«u..n...unnl .................................................. SOUFCC moteur CC Figure 3 Les interrupteurs K1 et K2 sont supposés idéaux. 2.2.1. Qu'est--ce qu'un « interrupteur idéal » ? 2.2.2. Quel est le rôle de la bobine d'inductance L dans ce montage ? 2.2.3. Préciser les états de fonctionnement autorisés pour les interrupteurs K1 et K2 compte tenu de la nature de la source et de la charge du hacheur (on justifiera en rappelant les règles d'association des sources auxquelles il faut faire référence) . 2.2.4. On considère dans tout ce qui suit un fonctionnement en régime périodique établi de période T. On considèrera de plus que la résistance R de l'induit est négligeable et que la * f.é.m. E est toujours positive. L'oscillogramme de la figure 4 fournit un relevé de tensions effectué alors que la source EO fournit une puissance P = 3 kW. La voie 1 représente la tension V. La voie 2 représente la tension obtenue par une sonde de courant: cette tension est proportionnelle à l'intensité i du courant traversant le moteur (sensibilité de la sonde : 1 volt par ampère). Base de temps : 10 ,us par carreau Voie 1 : - mode DC - 20 V par carreau Voie 2 (entre les deux curSeurs figurant -- arme en pointillés) : -- mode AC - 0,1V par carreau -- OCH1 Figure 4 On s'intéresse au fonctionnement sur une période entre les instants 0 et T. On note OtT l'instant de commutation à partir duquel la tension V vaut 0 (V = 0 pour GT 5 t < T ). 2.2.4.1. Représenter le circuit électrique (comprenant le moteur à courant continu) qui équivaut au montage de la figure 3 dans chaque phase de fonctionnement ( 0 S t < ocT d'une part et OLT s t < T d'autre part). 2.2.4.2. Ecrire les équations d'évolution i(t) de l'intensité du courant en fonction du temps (on notera I... et IM les valeurs minimale et maximale de i) : a)pour 0 s t < aT b)pour aT s t < T 2.2.4.3. Représenter rapidement, sur des figures distinctes, les graphes de i... et ile en fonction du temps. 2.2.4.4. Déduire de l'oscillogramme de la figure 4 et des conditions de réalisation de l'essai correspondant (il ne s'agit pas de l'essai initial pour lequel E = 100 V mais de celui présenté à la question 2.2.4.) : a) la valeur de E0 b) la valeur de oc correspondant à l'essai réalisé c) la valeur de E correspondant à l'essai réalisé (1) la valeur de L e) la valeur moyenne du courant débité par la source EO
f) la valeur moyenne du courant circulant dans l'induit.
2.2.5. Dans le cas d'un moteur à courant continu réel (si on prend en compte la
résistance R),
pourquoi a--t--on intérêt, pour améliorer le rendement, à limiter l'ondulation
du courant dans
l'induit (c'est-à-dire à limiter les variations du courant autour de sa valeur
moyenne) ?
TROISIEME PARTIE
PRINCIPE DU MOTEUR SYNCHRONE
3.1. Stator de la machine synchrone : production d'un champ tournant
On constitue un système (81) de deux soléno'1'des identiques de même axe Ox et
montés en série de
sorte qu'un courant d'intensité i ; circule dans le même sens dans les deux
solénoïdes (figure 5).
Figure 5
Dans ces conditions, le champ magnétique au centre O du système (81) peut se
mettre sous la
_
forme : B, = K. i, e: (K est une constante et e: est le vecteur unitaire de
l'axe Ox).
On place maintenant deux systèmes (SI) et (82) identiques au précédent selon la
configuration de la
figure 6 (les axes Ox et Oy de (81) et (82) sont perpendiculaires et se coupent
en 0).
Chacun des systèmes (81) et (SZ) a une résistance totale R et une inductance
totale L.
On branche en parallèle entre les bornes A et B d'une source de tension
sinuso'1'dale idéale de f.é.m.
u = U \/-2_ casa; t :
- le système (81) en série avec une résistance Ro d'une part,
-- le système (82) en série avec une résistance de même valeur R0 et avec un
condensateur de
capacité C d'autre part.
En régime permanent sinuso'1'dal, les intensités réelles i 1( t) et i2(l) des
courants circulant dans (SI) et
(SZ) sont de la forme :
i1(t) : I,\Æ c0s(coet-- $;) et i2(t) : 12\/--2- cos(cwt-- gag) .
..... illlllllli .""...--
i1
C :
.. ................................. > ..
i2
Figure 6
3.1.1. En utilisant les propriétés de symétrie du champ magnétique, justifier
la direction du champ
magnétique B, créé par le système (81) au point 0.
3.1.2. Donner les expressions de I 1, 12, tamp; et tançp2 en fonction de U, R,
RO, L, C et (a).
3.1.3. 3) Les valeurs de R, L et ca; étant imposées, quelles valeurs faut-il
donner à R0 et C pour que :
]; =Iz et que ç02-- ça; : 7t/2 ?
b) Que valent alors @] et ça; ? '
3.1.4. En considérant remplies les conditions précédentes (1; = 12 et w --- w;
: 7c/2), déterminer les
composantes sur Ox et sur Oy du champ magnétique total 5 en 0 (on notera BT son
module
que l'on exprimera en fonction de U, K et Lan).
3.1.5. a) Justifier l'appellation de « champ tournant » pour ce champ
magnétique total Ë .
b) Préciser à quelle vitesse ce champ tourne dans le plan Oxy.
3.2. Entraînement du rotor du moteur synchrone
La partie mobile du moteur synchrone (rotor) est constituée d'un bobinage
alimenté par un courant
continu et assimilable à un aimant de moment magnétique M , de module Mo
constant. On suppose
que IÎ/Ï est animé dans le plan Oxy d'un mouvement de rotation uniforme autour
de l'axe Oz
(perpendiculaire à ce plan) àla vitesse angulaire a) .
Le mouvement s'effectue dans une partie de l'espace où règne un champ
magnétique B supposé
uniforme d'amplitude BT qui, lui, tourne dans le plan Oxy autour de l'axe Oz à
la vitesse angulaire
@ ( ah n'étant pas a priori égale à a)).
On note e; le vecteur unitaire de l'axe Oz et 90 la valeur initiale de l'angle
(Ü , Ë ) (cf. figure 7).
Figure 7
3.2.1. Exprimer 9(t). En déduire la valeur instantanée du couple Ï" (t) = I'
(t). E; exercé par le
champ Ë sur le rotor.
3.2.2. Pourquoi le moteur synchrone ne peut--il fonctionner que pour une
vitesse angulaire a) égale
à ca; ? '
3.2.3. On se place dans le cas ca: ca; :
3.2.3.]. Exprimer la valeur F0 de F(t) .
3.2.3.2. Quelle condition l'angle 9 : (IÎIÎ , Ë) entre Ü et Ë en régime
permanent doit--il
vérifier pour que cette machine fonctionne effectivement en moteur '?
3.2.3.3. Quelle est, dans ce cas (fonctionnement en moteur), la puissance
mécanique Pméca
' fournie par le moteur ?
3.2.3.4. On suppose que la machine, fonctionnant en moteur, entraîne une «
charge » qui
impose au moteur un couple résistant de module constant 1", (les autres couples
résistants étant négligés).
Quelle condition doit vérifier F, pour que le moteur puisse effectivement
entraîner la
charge ?
Fin du Problème de Physique.
A,G° (J.mo|")
200000
--200000
--400000 ... '9'
-600000
-800000
-1000000
--1200000
Potentiel (V/ESH)
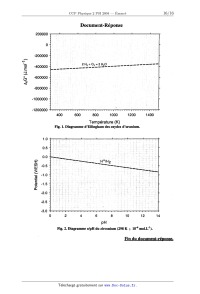
Document--Réponse
'2H2 "'. 02 =2 H20
. : I ' ' -- - ___--___ "'»
400 600 800 1000 1200 1400
Température (K)
Fig. ]. Diagramme d'Ellingham des oxydes d'uranium.
2 4 6 8 10 12 14
Fig. 2. Diagramme e/pH du zirconium (298 K ; 10"6 mol.L").
Fin du document-réponse.