X/ENS Chimie PC 2016
| Thème de l'épreuve | Stockage de l'énergie. Autour des allènes. |
| Principaux outils utilisés | thermodynamique, oxydoréduction, mélanges binaires, chimie organique, orbitales moléculaires |
| Mots clefs | lithium, batterie, allène |
Corrigé
: 👈 gratuite pour tous les corrigés si tu crées un compte👈 l'accès aux indications de tous les corrigés ne coûte que 5 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)








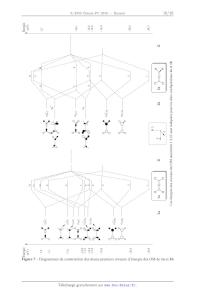






Rapport du jury
(télécharger le PDF)






Énoncé obtenu par reconnaissance optique des caractères
ÉCOLE POLYTECHNIQUE ÉCOLES NORMALES SUPÉRIEURES ÉCOLE SUPÉRIEURE DE PHYSIQUE ET DE CHIMIE INDUSTRIELLES CONCOURS D'ADMISSION 2016 FILIÈRE PC COMPOSITION DE CHIMIE A (XEULC) (Durée : 4 heures) L'utilisation des calculatrices n'est pas autorisée pour cette épreuve. Premier problème STOCKAGE DE L'ÉNERGIE Le lithium (Z = 3) est un métal blanc, brillant, qui s'oxyde facilement en présence d'air ou d'humidité. Il a été découvert en 1817 par Johan August Arfwedson dans un aluminosilicate naturel, mais c'est Jons Jacob Berzelius qui lui a donné le nom de lithion (du grec lithos, la pierre) pour rappeler son origine minérale. Il s'agit du plus léger de tous les éléments métalliques (sa masse volumique vaut 0,53 g.cm-3) et ses températures de fusion et ébullition sont respectivement de 181 °C et 1336 °C. Le lithium possède de nombreuses applications dans des secteurs très variés. Les usages dominants sont ceux de l'industrie du verre et des céramiques, suivis de ceux des lubrifiants et des batteries. C'est pour le secteur du stockage de l'énergie que la demande en lithium connaît actuellement la plus forte croissance. Les Documents 1, 2, 3, et 4 situés en annexe aux pages 6 à 8 illustrent d'une part le mode de production du métal, et d'autre part son rôle essentiel dans la composition de batteries que l'on retrouve par exemple dans l'électronique portable (du fait de leur légèreté) ou pour l'électrification des véhicules (du fait de leurs excellentes capacités de stockage). Des données physico-chimiques utiles pour l'ensemble du premier problème sont également disponibles en annexe, dans le Document 5. Première partie : l'extraction et la préparation du métal lithium Deux types de ressources sont exploitées pour l'extraction du lithium : les saumures des grands lacs salés (salars) et les minéraux à lithium comme les pegmatites granitiques. L'extraction du lithium à partir des saumures des salars d'altitude est particulièrement importante, car elle compte pour près de la moitié de la production mondiale actuelle en lithium, et 75 % des réserves mondiales estimées en lithium y sont localisées, principalement en Amérique du Sud. Les questions 1 à 6 se rapportent au Document 1 dans lequel les données en pourcentages, notamment sur le Schéma 1, se réfèrent à des grandeurs massiques. 1. Calculer l'augmentation relative en pourcent de la concentration massique des ions lithium dans les saumures après l'étape d'évaporation, sachant que la densité des saumures initiales vaut 1,25. Discuter l'intérêt de cette étape. 2. Préciser la nature des sels qui précipitent à partir des saumures dans les différents bassins (avant leur transport à l'usine de Carmen), en commentant l'ordre de précipitation observé. Les produits de solubilité des sels considérés seront supposés indépendants de la température. 1 3. Préciser la nature des principaux anions présents au départ dans ces saumures. 4. Sachant que le bore peut complexer jusqu'à quatre ligands monodentates, expliquer en prenant l'exemple de l'éthane-1,2-diol comment le bore est éliminé des saumures après l'étape de passage dans les bassins. Proposer une équation-bilan possible pour cette transformation. 5. Déterminer quel cation est ensuite éliminé des saumures, et donner le principe de cette étape. 6. Expliquer pourquoi la suspension doit être chauffée lors de l'ajout du carbonate de sodium. Le carbonate de lithium (Li2CO3) brut ainsi obtenu subit alors une étape de purification avant d'être transformé en chlorure de lithium (LiCl) selon le mode opératoire décrit dans le Document 2. Dans les questions 7 à 10, on indiquera avec soin l'état physique de chaque espèce dans les réactions demandées. 7. Ecrire l'équation de dissolution du carbonate de lithium dans l'eau, opération généralement réalisée sous faible pression de dioxyde de carbone. Identifier les sels restant en suspension. 8. Donner l'équation-bilan de la réaction conduisant au carbonate de lithium purifié (à 99 %). 9. La transformation du carbonate de lithium en chlorure de lithium s'opère à 200 °C par action du chlorure d'hydrogène gazeux. Ecrire l'équation-bilan de la réaction. 10. Donner l'expression littérale de l'enthalpie standard de cette réaction à 200 °C. Le calcul conduit à une valeur de - 90 kJ.mol-1. 11. Étudier si l'avancement de la réaction est sensible à une augmentation de pression, ou à un changement de température. Commenter le choix industriel de la température de 200 °C. Le lithium est finalement obtenu par une électrolyse ignée (électrolyse à haute température) du chlorure de lithium à 450 °C. Cette électrolyse est décrite dans l'extrait de brevet du Document 3. 12. Légender les parties du montage du Schéma 2 du Document 3, numérotées de 1 à 7. Indiquer les polarités de chaque électrode. Il n'est pas demandé de reproduire le montage du Schéma 2. 13. Ecrire toutes les réactions redox susceptibles de se produire aux deux électrodes dans le mélange de sels fondus (liquides ioniques) utilisé à 450 °C, tel que décrit dans le Document 3. 14. Déterminer les potentiels standard des couples Li+/Li et K+/K à 450 °C, en prenant pour référence le couple Ag+/Ag. À cette température les enthalpies libres standard de formation de KCl(l) et LiCl(l) (ramenées à une mole de dichlore) valent : f G (KCl( l) ) = - 816 kJ.mol-1 et f G (LiCl( l) ) = - 740 kJ.mol-1 respectivement. 0 0 À 450 °C, dans le milieu de sels fondus utilisé pour effectuer l'électrolyse, le résultat ° - ° + E (Cl2 /Cl ) - E (Ag /Ag) = 1,23 V sera également admis. 15. Préciser si les systèmes Li+/Li et K+/K sont rapides ou lents dans ces conditions. En tenant compte du résultat de la question 14, déduire quel dépôt est observé à la cathode, puis écrire l'équation-bilan de l'électrolyse. 16. Repérer la(es) réaction(s) que l'on souhaite empêcher à l'anode en la protégeant. Justifier le fait qu'il ait fallu effectuer un séchage supplémentaire de LiCl avant l'électrolyse. 17. Interpréter l'origine de la circulation naturelle du milieu d'électrolyse et envisager les bénéfices au niveau du fonctionnement de l'électrolyseur. 18. Représenter schématiquement le diagramme binaire solide-liquide isobare du mélange KCl-LiCl sous Patm sachant qu'il présente un eutectique qui fond à 353 °C pour une fraction molaire en LiCl 2 de 0,592. Indiquer la nature des phases en présence dans les différents domaines du diagramme. Commenter la dernière phrase du Document 3, en expliquant pourquoi il est conseillé de se placer près de la composition eutectique et en utilisant un excès de chlorure de lithium. 19. Justifier l'utilisation d'une tension de 6,0 V pour cette électrolyse, en illustrant le propos à l'aide de courbes intensité-potentiel. 20. Estimer la consommation électrique nécessaire pour produire 1 kg de lithium (en kWh) en utilisant cette cellule qui a un rendement faradique de 0,85. Évaluer le volume de saumure initial correspondant en faisant une hypothèse raisonnable sur le rendement d'extraction des ions Li+. Deuxième partie : les batteries au lithium Une cellule de batterie lithium-polymère (Li-Po), comme celle qui est représentée sur la Figure 1, peut être constituée d'une électrode de lithium métal, d'un électrolyte contenant des ions Li+ ([Li+] = 1 mol.L-1) au sein d'un gel polymère organique et d'une électrode composite à base d'oxyde de manganèse de type -MnO2 (variété cristalline de MnO2). Le composé actif -MnO2 de structure cubique est synthétisé en plusieurs étapes. La première consiste en la réduction, en solution aqueuse acide, des ions permanganate par l'acide fumarique [acide (E)-but-2-én-1,4-dioïque] pour obtenir l'oxyde de manganèse de type -MnO2 qui a une structure hexagonale. Li+ Li -MnO2 Figure 1 Représentation schématique d'une batterie lithium-métal chargée 21. Ecrire la réaction entre les ions MnO4- et l'acide fumarique (C4H4O4), sachant qu'il n'est pas observé de dégagement de dioxyde de carbone dans ces conditions. Dans une seconde étape, le composé -MnO2 ainsi obtenu est chauffé à 600 °C sous air pendant plusieurs heures afin d'obtenir la variété -MnO2. Cette transformation de structure « hexagonale ! cubique » étant irréversible, commenter la notion de stabilité pour la phase -MnO2. Lors de la décharge de la cellule de la batterie (système en fonctionnement), le cristal de -MnO2 de l'une des électrodes est le siège d'une réaction d'insertion des ions Li+. Cet oxyde de manganèse possède une structure cubique qui peut être décrite comme un réseau cubique à faces centrées (cfc) d'ions O2- avec occupation de la moitié des sites octaédriques par des ions Mn4+. 22. Etudier soigneusement la compatibilité de cette description avec la stoechiométrie de l'oxyde. 23. Ecrire les réactions aux électrodes lors de la décharge de la cellule. Préciser le sens du courant et la polarité des électrodes. Ecrire l'équation-bilan globale lorsque la batterie fonctionne, puis déterminer la tension à vide de la cellule Li-Po. 24. En fait, un seul ion Mn4+ par maille est susceptible de se réduire en Mn3+ lors de la décharge de la cellule. Déduire le nombre d'ions Li+ insérés en site tétraédrique dans cette structure et la formule chimique du composé ainsi obtenu. 3 25. La structure initiale -MnO2 possède un paramètre de maille ai = 800 pm et la structure finale (en fin de décharge de la batterie) un paramètre de maille af = 820 pm. Estimer la variation relative du volume de maille lors de l'insertion de lithium dans la structure de cet oxyde. 26. Déterminer la capacité spécifique (quantité de charge stockable) exprimée en Ah.kg-1 du matériau -MnO2. Comparer la valeur estimée avec celle fournie dans le Tableau 1. En déduire la valeur de l'énergie massique (quantité d'énergie stockable) exprimée en Wh.kg-1 de ce matériau. Chargé Déchargé Li C Si Li-MnO2 LiC6 Li15Si4 MnO2 Capacité spécifique (Ah.kg-1) 3860 372 3600 150 ------Densité 0,53 2,26 2,33 4,28 2,20 1,18 5,03 Tableau 1 Propriétés de quelques matériaux d'électrode Les batteries à base de lithium permettent, dans les conditions d'utilisation recommandées, d'effectuer un nombre élevé de recharges sans perte notable de leur capacité initiale. 27. Ecrire l'équation-bilan de la réaction de recharge de la cellule d'une batterie Li-Po. Le redépôt de lithium métal se fait ordinairement selon un processus de croissance dendritique avec formation de fins filaments qui grandissent perpendiculairement à la surface de l'électrode. Expliquer pour quelle raison cela peut constituer un grave problème de sécurité. Préciser ici l'intérêt d'utiliser un électrolyte gélifié. Une autre technologie de batterie au lithium permet de remplacer l'électrode métallique de la cellule de l'étude précédente par une électrode en graphite déposée sur un support. Cette technologie est décrite dans le Document 4 qui expose le fonctionnement de la cellule de batterie Li-ion représentée sur le Schéma 3. 28. Écrire les réactions aux électrodes qui ont lieu au cours du chargement de la batterie Li-ion, puis l'équation-bilan de la réaction. Attribuer l'anode et la cathode. Déterminer la tension à vide d'une cellule de la batterie Li-ion. Des recherches en cours visent à remplacer l'électrode en graphite de la batterie lithium-ion par une électrode constituée d'un autre élément qui puisse s'allier avec le lithium. Le silicium apparaît de ce point de vue particulièrement prometteur. Figure 2 Diagramme binaire solide-liquide isobare à Patm du mélange lithium-silicium 4 29. A l'aide du diagramme binaire isobare d'équilibre Li-Si à Patm de la Figure 2, déterminer la fraction molaire maximale de lithium alliable avec le silicium, à température ambiante. 30. Le processus de lithiation électrochimique du silicium à 415 °C est représenté sur la Figure 3. Décrire les étapes successives observées (à y croissant), et interpréter la correspondance entre la courbe de la Figure 3 et le diagramme de la Figure 2. Figure 3 Courbe de lithiation électrochimique du silicium à 415 °C, la tension est donnée par rapport au cas de Li+/Li choisi comme référence 31. En réalité, lors de l'insertion électrochimique du lithium dans le silicium à température ambiante, le composé ultime formé est Li15Si4. À partir de la position du point représentatif de ce composé dans le diagramme binaire de la Figure 2, préciser la nature des phases solides en présence correspondant à la formule brute Li15Si4. 32. Le silicium cristallise dans un réseau cfc avec occupation d'un site tétraédrique sur deux par des atomes de Si (structure diamant). Étudier sans développement excessif si le composé précédent Li15Si4 est un alliage d'insertion et/ou de substitution. 33. Connaissant les paramètres de maille du composé initial (Si, aSi = 540 pm) et final (Li15Si4, aLi-Si = 1070 pm), estimer la variation relative du volume de maille subi par le silicium. Comparer le comportement des deux électrodes de cette cellule lors de l'insertion du lithium, en s'appuyant sur les résultats de la question 25. Un constructeur de batteries souhaite comparer les performances et gains obtenus en passant d'un système classique C // Li-MnO2 à un système Si // Li-MnO2. 34. D'après les données relatives aux matériaux d'électrodes utilisés figurant dans le Tableau 1 et les données commerciales fournies dans le Tableau 2, déterminer la capacité exprimée en Ah de chacun des deux systèmes concurrents. Etudier la cohérence des résultats pour chaque système. En déduire l'énergie emmagasinée en Wh par ces deux batteries, et commenter les résultats. Masse matériau actif (g) Batterie de format 18650 C // Li-MnO2 C Li-MnO2 2,96 6,47 Batterie de format 18650 Si // Li-MnO2 Si Li-MnO2 0,39 9,50 Volume batterie (cm3) 16,5 16,5 Tableau 2 Données commerciales de deux types de batteries Li-ion 35. Les batteries contenant une électrode en lithium sont progressivement remplacées par les batteries utilisant la technologie d'insertion des ions lithium. Expliquer si l'étude qui vient d'être décrite conforte ce choix. Etayer la réponse en quelques lignes. 5 Annexe Document 1 Extraction du lithium : traitement des saumures du salar (désert de sel) de Atacama au Chili, premier exportateur mondial de lithium Les saumures brutes qui contiennent majoritaiSaumure (2 g.L-1 Li) Chlorures Évaporation solaire rement (concentrations massiques décroissantes) les CaCl2 + + + 2+ + Bassins de halite à carnallite CaSO4.H2O cations Na , K , Mg , et Li sont directement Saumure enrichie (6 à 6,1 % Li, 1 à 8 % Mg, 0,8 % B) H3 BO 3 pompées à partir du lac souterrain situé sous une CaO + Na 2 CO3 croûte superficielle dont la profondeur peut atteindre Précipitation MgCO 3 45 m. Le fort ensoleillement qui règne dans le désert + Mg(OH) d'Atacama permet de concentrer par évaporation les Solides 2 Rejet Épaississage et filtration et sels dissous des saumures dans des bassins artificiels. CaSO4 + Les saumures provenant des puits sont rassemblées Na CO CaCO 3 Précipitation de Li 2 CO3 2 3 dans un canal à partir duquel elles sont envoyées dans des bassins dits de halite (NaCl) où est ajouté CaCl2 Retour aux bassins Épaississage et filtration d'évaporation en faible quantité. La halite est périodiquement récoltée pour être stockée en tas qui peuvent atteindre Séchage 130 - 160 °C Refroidissement 10 m de haut. Quand les bassins de halite sont saturés en chlorure de potassium, les saumures sont envoyées Li 2 CO3 vers les bassins dits de sylvinite, qui est une solution solide de sylvine (KCl) et de halite. La sylvinite est Schéma 1 Diagramme d'extraction du lithium ; récoltée et stockée en tas, avant d'être chargée sur les pourcentages donnés sont massiques. des camions afin d'alimenter l'usine de Coya Sur (Chili) qui réalise la transformation en nitrate de potassium. Les saumures sortant des bassins de sylvinite alimentent ceux de précipitation de bischofite (MgCl2.6H2O) puis de carnallite (KMgCl3.6H2O). À la sortie du bassin de carnallite, les saumures sont transportées par camion à l'usine du salar de Carmen (Chili) et stockées pour la séparation de Li, B, et Mg. Dans les saumures exploitées pour le lithium, le bore présent sous forme d'acide borique, constitue une impureté majeure mais aussi un sous-produit valorisable. Il existe plusieurs solvants plus ou moins efficaces pour extraire l'acide borique (H3BO3). Dans le cas des saumures chiliennes, le bore est extrait par des polyols dissous dans du kérosène. La réextraction à partir de la phase organique est effectuée avec une solution aqueuse d'acide sulfurique. La solution de réextraction passe sur du charbon actif pour éliminer les traces de solvant, puis elle est évaporée pour cristalliser l'acide borique, récupéré par centrifugation. Après récupération du bore, le magnésium est éliminé par précipitation (ajout préalable de CaO et de Na2CO3). La solution épurée obtenue, enrichie en lithium, traverse des échangeurs de chaleur qui augmentent sa température. Elle est alors traitée par du carbonate de sodium (Na2CO3) dans des réacteurs agités revêtus de caoutchouc pour faire précipiter le carbonate de lithium (Li2CO3). La suspension de carbonate de lithium est filtrée ou centrifugée. Le carbonate est ensuite séché et briqueté. Le Schéma 1 résume les opérations depuis les saumures jusqu'au carbonate de lithium. Document 2 Purification du carbonate de lithium et transformation en chlorure de lithium (LiCl) L'obtention du lithium métal se fait en utilisant le chlorure de lithium obtenu à partir du carbonate de lithium. Le carbonate de lithium est d'abord purifié afin d'enlever les impuretés gênantes pour l'électrolyse et pour la pureté du lithium final, en particulier les ions sodium, calcium, magnésium et sulfates. Le procédé le plus utilisé est le procédé au dioxyde de carbone (CO2). Il consiste à solubiliser le lithium sous forme d'hydrogénocarbonate par ajout de dioxyde de carbone en opérant sur une suspension de carbonate de lithium dans l'eau. Après une filtration qui élimine les impuretés solides, on précipite le lithium du filtrat sous forme de carbonate par décomposition thermique à 90 °C de l'hydrogénocarbonate. Le carbonate purifié est transformé en chlorure par réaction avec l'acide chlorhydrique. Par suite de la forte corrosion résultant de cette réaction, les réacteurs sont en aciers 6 spéciaux ou en titane. Le chlorure de lithium est cristallisé, essoré puis séché. Il est extrêmement hygroscopique et un séchage final supplémentaire est nécessaire, juste avant l'électrolyse. Document 3 Procédé pour la préparation continue de lithium par électrolyse du chlorure de lithium (extrait de brevet) La présente invention concerne un procédé pour la préparation de lithium par électrolyse du chlorure de lithium dans un mélange de sels fondus ; l'appareillage utilisé pour la mise en oeuvre dudit procédé est représenté sur le Schéma 2. La présente invention vise pour la réalisation de cette électrolyse un procédé simplifié qui présente les caractéristiques suivantes : - il est mis en oeuvre en continu ; - on sort dudit électrolyseur un mélange 6 constitué du lithium métallique et des sels fondus. Si l'on désire récupérer le lithium pur, il convient de mettre en oeuvre des techniques connues de séparation de ce métal d'avec les sels fondus. - l'anode en graphite est entourée par la cathode en acier inoxydable ; 3 - on effectue l'électrolyse sans utilisation d'un diaphragme entre l'anode et la cathode, mais en réalisant dans l'espace compris entre 5 l'anode et la cathode, une circulation naturelle rapide (0,5 à 5 cm.s-1) du milieu d'électrolyse ; - enfin, on protège l'anode contre une attaque éventuelle du lithium surnageant à la 1 2 surface du milieu d'électrolyse et contre une 7 éventuelle réoxydation directe du lithium sur l'anode en gainant ladite anode dans sa partie surmontant la surface du bain d'électrolyse et 4 jusqu'au-dessous de celle-ci avec un matériau réfractaire isolant (alumine) ; Schéma 2 Schéma de l'électrolyseur - par ailleurs le dichlore produit par l'électrolyse est soutiré en continu sans dilution par un gaz inerte ce qui permet son utilisation industrielle immédiate. Le milieu d'électrolyse est constitué d'un mélange de sels fondus à base de chlorure de lithium et d'au moins un autre chlorure alcalin et/ou alcalino-terreux qui, avec le chlorure de lithium, forment un mélange eutectique fondant à une température comprise entre 320 et 360 °C environ. On étudie plus précisément le cas où le mélange liquide de sels fondus soumis à l'électrolyse est constitué de chlorure de lithium et de chlorure de potassium. L'électrolyse devant être réalisée à une température comprise entre 400 et 500 °C environ, et de préférence aux environs de 450 °C, il convient que le mélange de sels fondus alimentant l'électrolyseur ait une composition assez voisine de la composition eutectique du mélange utilisé, avec un excès en chlorure de lithium. Pour le cas du mélange de chlorure de lithium et de chlorure de potassium, on considère qu'à 450 °C environ, la quantité de chlorure de lithium dudit mélange pourra varier de 69 % en mole à l'entrée de l'électrolyseur à 56 % en mole à la sortie de l'électrolyseur. Dans ce cas, le chlorure de lithium peut être dans un excès allant jusqu'à 10 % en mole par rapport à la composition eutectique du mélange de sels fondus chlorure de lithium-chlorure de potassium. Document 4 Principe de la technologie au « lithium-ion », représentée sur le Schéma 3 Les batteries « lithium-ion » fonctionnent par principe comme des cellules galvaniques, toutefois sans survenue de réaction chimique des matériaux actifs. Pendant la charge et la décharge, les ions lithium sont en quelque sorte échangés entre matériaux des deux électrodes. 7 Pendant le processus de charge, les ions lithium se déplacent en traversant l'électrolyte, pour venir s'intercaler entre les niveaux de graphite constituant l'une des électrodes. Lors de la décharge de la batterie, les ions lithium retournent dans l'oxyde métallique de l'autre électrode. La formation d'une couche de recouvrement protectrice sur l'électrode en graphite est essentielle pour le fonctionnement de l'intercalation. Elle doit être splitéable aux petits ions Li+, mais imperméable aux molécules de solvants. Si la couche de recouvrement est insuffisamment formée, les molécules de solvants s'intercalent avec les ions Li+, entraînant une destruction irréversible de l'électrode en graphite. Cellule de batterie Li-ion Séparateur Li + Li+ Li+ Légende Carbone (graphite ) Métal (Manganèse) Lithium Oxygène Electrolyte non aqueux Processus de chargement Processus de déchargement Schéma 3 Représentation d'une cellule de batterie Li-ion Document 5 Données physico-chimiques !" A 298 K, !" !" ! !!!!"!! ; F = 96500 C.mol-1 ; NA = 6,02.1023 mol-1 ! Atome Masse atomique molaire (g.mol-1) Li 7 C 12 O 16 Si 28 Mn 55 Produits de solubilité dans l'eau à 298 K Espèce Log Ks CaSO4.H2O - 4,9 CaCl2 11,5 Halite 1,6 Sylvine 0,9 13 g.L-1 (298 K) 94 g.L-1 (298 K) 0,15 g.L-1 (298 K) Solubilité de Li2CO3 : Solubilité de LiHCO3 : Solubilité de CO2 : Bischofite 4,5 Carnallite 4,3 Na2CO3.10H2O - 1,4 7 g.L-1 (373 K) 190 g.L-1 (373 K) 0,06 g.L-1 (333 K) MgCO3 - 3,4 0 g.L-1 (373 K) Constante d'acidité à 298 K : pKa = 9,28 pour le couple B(OH)3/B(OH)4Enthalpies molaires standard de formation, entropies molaires standard et capacités thermiques molaires standard à 298 K K(s) Espèce ! f H 298 (kJ.mol-1) Li2CO3(s) - 1175 LiCl(s) - 409 HCl(g) - 92 CO2(g) - 394 H2O(liq) - 286 H2O(g) - 242 S0 (J.K-1.mol-1) 90 59 187 214 70 189 83 ! !!!! !(J.K-1.mol-1) 96 48 29 37 75 35 51 Tf (°C) 723 610 0 63 KCl(s) - 328 771 fus H (LiCl(s) ) = 21 kJ.mol-1 ; vap H (H 2O ( l) ) = 44 kJ.mol-1, TEb (K) = 759 °C . 0 0 Potentiels standard d'oxydoréduction à 298 K en volts (par rapport à l'électrode standard à hydrogène) MnO4-/-MnO2 1,7 O2/H2O 1,2 -MnO2/Li-MnO2 1,2 C2H2O4/C4H4O4 0,5 Acide oxalique, C2H2O4 ; acide fumarique, C4H4O4. 8 Li+(C)/LiC6 - 2,5 Li+(Si)/Li15Si4 - 2,6 Li+/Li -3 Deuxième problème AUTOUR DES ALLÈNES Un soin particulier est attendu dans l'écriture des mécanismes réactionnels : les formules utilisées dans les réponses aux questions portant un astérisque (*) après leur numéro devront obligatoirement être des formules de Lewis et faire apparaître les doublets non liants et les formes mésomères des intermédiaires réactionnels s'il y a lieu. Pour décrire le mécanisme dans les schémas réactionnels, l'écriture des molécules pourra être simplifiée à leur partie pertinente (abréviation avec le sigle R ou R' par exemple). Première partie : structure et réactivité des allènes Les allènes sont des composés comportant deux doubles liaisons éthyléniques C=C sur un même atome de carbone (Figure 4 structure A, l'atome de carbone central C est indiqué pour plus de clarté). Ils constituent une sous-famille de celle des cumulènes qui sont des composés formés par un enchaînement ininterrompu de doubles liaisons (C=C)n avec n > 1. Le premier terme des allènes est le propa-1,2-diène, pour lequel R1=R2=R3=R4=H. Ce diène 1,2 peut exister dans deux configurations notées 1a et 1b. Dans 1a, tous les atomes sont coplanaires (dans le plan yz), tandis que dans 1b, les deux groupements CH2 sont dans deux plans orthogonaux (yz et xz), comme explicité dans la Figure 4. R1 R3 H R4 H H H H C C R2 H A y H C 1a z H x 1b Figure 4 Structure de l'allène A et des configurations possibles 1a et 1b du propa-1,2-diène Afin de déterminer laquelle de ces deux configurations 1a ou 1b de l'allène est la plus stable, leurs orbitales moléculaires (OM) ont été construites à partir des orbitales atomiques (OA) d'un atome de carbone, et des OM du fragment [CH2----CH2] qui correspond à une molécule d'éthène étirée sous sa forme 2a (plane) ou sa forme 2b (CH2 dans des plans orthogonaux) en accord avec la Figure 5. H H H H H H H 2a C H H H H 2b H H + H H C 1b 1a H C + C Figure 5 Construction des configurations 1a et 1b par la méthode des orbitales de fragment Les diagrammes des niveaux énergétiques des OM de 1a et 1b, dont la construction découle de la Figure 5, sont proposés en Figure 7 en page suivante. Les représentations des OM -10,3 np correspondantes n'y sont par contre pas données. Les diagrammes d'OM des configurations 2a et 2b utilisés pour cette construction ont eux-mêmes été obtenus à -11,5 partir des OM du fragment CH2 les plus basses en énergie représentées sur la n Figure 6 avec les énergies données en eV. Dans la suite du problème seules les OA / OM de valence seront à prendre en compte. -14,4 36. Effectuer le remplissage du diagramme d'énergie des OM du fragment CH2 en expliquant la démarche (ZC = 6). CH2 -27,0 CH2 37. Donner le caractère liant, antiliant ou non liant des quatre OM représentées en justifiant les réponses. Préciser quelles OM n'ont pas été dessinées sur ce Figure 6 OM diagramme. Représenter schématiquement l'une de ces OM. du fragment CH2 9 Figure 7 Diagrammes de construction des douze premiers niveaux d'énergie des OM de 1a et 1b 10 -34,9 -28,5 -18,8 -14,9 -15,4 -12,6 -13,2 -7,6 -1,1 1,6 Énergie (eV) a CH2 a*CH2 a CH2 a*CH2 a CC a CC a*CC a*CC 2a H H C H C z x 2b 1b H H H C H H 5 8 10 Les énergies des niveaux des OM numérotés 1 à 10 sont indiquées pour les deux configurations 1a et 1b 1a 1 3 6 1 y 4 7 11 2 b CH2 b b* b*CH2 b CC b*CC 9 12 2 3 4 6 5 7 8 9 10 11 12 C -34,7 -28,6 -19,0 -14,8 -14,9 -10,1 1,2 Énergie (eV) 38. Commenter brièvement la structure de l'une des OM de 2a, au choix, en indiquant quelle(s) règle(s) a(ont) été suivie(s) pour la construire à partir des OM du fragment CH2. 39. Dessiner le diagramme d'OA de la couche de valence du carbone (C central de 1a, OA 2s et 2p), et présenter sous forme de tableau les symétries de chaque OA par rapport aux plans nodaux yz, xz, et xy. Dans le Tableau 3 sont rassemblées les symétries des OM de la forme 2a de la molécule d'éthène étirée par rapport aux mêmes plans nodaux (S = symétrique, A = antisymétrique). OM (2a) yz xz xy * a CC S S A a*CC A S A a CC A S S a CC S S S a*CH2 S A A a CH2 S A S * a CH2 S S A a CH2 S S S Tableau 3 Symétries des OM de la molécule d'éthène étirée 2a par rapport aux plans nodaux 40. En comparant ces symétries avec celles trouvées à la question 39, retrouver les interactions entre les OM de 2a et les OA du carbone central du diagramme de 1a de la Figure 7. Faire un bref commentaire sur les recouvrements orbitalaires qui ont lieu entre les OM liantes de type de 2a (OM des lignes 3 et 6 du Tableau 3) avec les OA p du carbone. 41. En utilisant les diagrammes d'OM de 1a et de 1b de la Figure 7, expliquer pourquoi la structure 1b du propa-1,2-diène est la plus stable. 42. Donner, en indiquant le raisonnement utilisé, l'énergie des niveaux de numéros j et k des deux OM occupées de 1b (notées OMj et OMk), dont les représentations obtenues à l'aide du logiciel Orbimol sont reproduites dans la Figure 8. OMj OMk Figure 8 Représentations obtenues avec Orbimol de deux OM de 1b L'OM3 (niveau n°3) de 1b se décompose sur la base de représentation des OA comme suit : () OM3 = - 0,28C 1 2s () + 0,42C 1 2pz () + 0,43C 2 2s () - 0,28C 3 2s () - 0,42C 3 4 2pz () - 0,27 H i 1s i=1 La notation C(2)2s y représente par exemple l'OA 2s du carbone numéroté 2 (le carbone central). 43. D'après la Figure 7 et la décomposition donnée ci-dessus, envisager, en proposant une argumentation, s'il est correct de considérer l'OM3 de 1b comme résultant de l'interaction de trois orbitales, une OA et deux orbitales de fragment. 11 Les allènes par l'intermédiaire de leurs doubles liaisons peuvent donner des réactions de DielsAlder. L'utilisation de cette cycloaddition avec les allènes est intéressante car sa mise en oeuvre conduit alors à des produits cycliques possédant une double liaison exocyclique aisément fonctionnalisable. 44. Donner la structure du produit susceptible d'être obtenu par chauffage d'un mélange stoechiométrique de propa-1,2-diène et de cyclopenta-1,3-diène dont la structure est représentée sur la Figure 9. En réalité le chauffage modéré de ce mélange conduit à la formation du dimère du cyclopenta-1,3-diène. Préciser la structure de ce dimère, puis expliquer grâce à un schéma simple pourquoi il se forme préférentiellement au composé attendu. Les énergies de la HO et de la BV du propa-1,2-diène calculées par le logiciel Orbimol ont pour valeurs respectives -10,1 et 1,2 eV. H H H H E (eV) OMe H H C H H cyclopenta-1,3-diène H SO 2Me 1-(méthylsulfonyl)propa-1,2-diène 2-méthoxybuta-1,3-diène 3 2 2,2 2,3 0,5 0,5 - 9,1 - 9,1 - 10,9 - 10,8 1 0 - 0,3 - 0,6 SO 2Me SO 2Me -9 -10 -11 - 10,9 - 11,5 SO 2Me -12 SO 2Me Figure 9 Énergies et représentations simplifiées des quatre orbitales frontières du 1-(méthylsulfonyl)propa-1,2-diène, du cyclopenta-1,3-diène et du 2-méthoxybuta-1,3-diène 45. Dans une autre expérience, le 1-(méthylsulfonyl)propa-1,2-diène, représenté sur la Figure 9, est opposé au cyclopenta-1,3-diène à 160 °C. Il réagit complètement pour conduire à deux composés stéréoisomères. Ecrire la structure de Lewis du groupe sulfonyle du 1-(méthylsulfonyl)propa-1,2diène, puis envisager l'interaction entre le groupement SO2Me et le système allénique de type . Déduire une conséquence sur les niveaux d'énergie des orbitales frontières du 1(méthylsulfonyl)-propa-1,2-diène et les comparer à ceux des orbitales frontières du propa-1,2diène. 46. En utilisant les diagrammes d'OM simplifiés de la Figure 9, et l'étude de la question 45, donner la structure de ces stéréoisomères. Indiquer quel(s) produit(s) pourrai(en)t être formé(s) par chauffage du 1-(méthylsulfonyl)propa-1,2-diène avec le 2-méthoxybuta-1,3-diène, également représenté sur la Figure 9. Expliquer précisément la régiochimie et/ou la stéréochimie du(es) produit(s) majoritairement formé(s) dans ce cas. Deuxième partie : synthèse de l'aplysiallène Le motif allène, quoique singulier, est présent dans la structure de plusieurs molécules naturelles d'origine marine ayant des propriétés thérapeutiques remarquables. Le ()-aplysiallène représenté en 12 Figure 10 montre ainsi une activité notable pour le traitement de certaines arythmies cardiaques. Le groupement actif de ce produit naturel est en réalité un motif bromoallène dont la préparation délicate a mobilisé l'imagination des chimistes de synthèse. Des données utiles pour l'ensemble de cette partie figurent dans le Document 6 à la page 16. H O C ()-Aplysiallène Br O Br H Figure 10 Structure du ()-aplysiallène L'aplysiallène a été isolé au début des années 2000 à partir de A. Kurodai, un mollusque récolté près de la ville de Fukui (Japon). Sa structure particulière qui comporte un bicycle formé de deux cycles tétrahydrofurane accolés et un groupement bromoallène, a rapidement attiré l'intérêt des chercheurs. Quelques années après sa découverte, une équipe canadienne en a proposé une première synthèse totale. La stratégie de synthèse choisie par le professeur canadien B.L.P. et son équipe, consiste à tout d'abord construire le motif bis-tétrahydrofuranique (les deux cycles à cinq accolés), à poursuivre par l'ajout de la chaîne latérale bromodiène, puis à terminer par la formation de la partie bromoallénique. 47. La première partie de la synthèse du ()-aplysiallène utilise le tartrate de diéthyle A protégé comme substrat de départ selon la voie décrite sur la Figure 11. Proposer des réactifs et des conditions opératoires pour obtenir A à partir du tartrate de diéthyle [(2R,3R)-2,3-dihydroxybutanedioate de diéthyle] de manière quantitative. Commenter ce dernier point. O O A EtO 1) LiAlH 4 KOH MsOH C OEt 2) Hydrolyse C H O 7 14 4 O D EtOH Pyridine O = Ms = H EtO 2C EtO 2C MsCl (2 équivalents) B O H O Ts = O H 3C S O O S O Me OEt OEt (1 équivalent) OEt C 4H 6O 2 E MgBr 1) (2 équivalents) 2) Hydrolyse OH F G TsOH, H 2O OH Figure 11 Début de la synthèse du ()-aplysiallène : préparation de l'intermédiaire G 48. Identifier les composés B et C de la Figure 11, sachant que le spectre infra-rouge (IR) de B issu de la réduction de A par l'hydrure complexe LiAlH4 contient une bande très large et très intense à 3276 cm-1. Préciser le rôle de la pyridine lors de la transformation de B en C. 49. *Le composé C est ensuite traité par l'acide méthanesulfonique (MsOH, acide fort) dans l'éthanol. Cette réaction conduit à deux produits dont l'un est C(CH3)2(OEt)2, et l'autre celui qui serait obtenu par hydrolyse de la seule fonction cétal de C. Donner un mécanisme plausible pour cette étape, puis déterminer la structure de D. 50. Le spectre IR du composé E isolé dans l'étape suivante ne présente aucune bande dans la région 18001650 cm-1. Proposer une structure pour le produit E, puis préciser la configuration absolue de ses centres stéréogènes. Le spectre RMN du proton de E contient trois multiplets intégrant dans un rapport 1/1/1 ; commenter ce résultat. 51. *Expliquer l'obtention de F à partir de E. Le passage de F à G se fait par l'action d'un équivalent d'orthoacétate de triéthyle [CH3C(OEt)3] en milieu acide. Ces conditions reviennent à traiter le composé F par un équivalent de chlorure d'éthanoyle (CH3COCl). Le spectre IR du produit G obtenu comporte en particulier une bande d'absorption intense à 1730 cm-1 et une bande large à 3440 cm-1. 13 52. *Déterminer la structure de G, puis attribuer les deux bandes observées en IR. Donner l'équation bilan de formation de G, puis proposer un mécanisme acido-catalysé plausible expliquant cette formation. 53. Cette dernière transformation porte le nom de réaction de désymétrisation. Justifier brièvement cette appellation, et indiquer son intérêt. L'étape suivante de la synthèse est une réaction d'oxydation du composé G en H. Cette oxydation dite de Mukaiyama, se fait en présence d'un sel de cobalt, d'hydroperoxyde de tert-butyle (t-BuOOH) et sous atmosphère de dioxygène. Son mécanisme général est explicité sur la Figure 12. Le rôle de l'hydroperoxyde de tert-butyle dans l'étape (1) est mal connu et ne sera pas détaillé ici. O H 2O HO 2 O 2 (+ t-BuOOH) X2Co O2 6 1 X2Co OH 2 O X2Co O O OH R 2 R' 5 OH O X2Co X2Co OH O H O R R' 4 R X2Co O OH R' 1/2 R O O O 3 OH O O O O X= OH N O R' Figure 12 Cycle catalytique décrivant l'oxydation de Mukaiyama 54. Donner la variation du nombre d'oxydation du cobalt au cours des étapes (1), (2), et (6) du cycle catalytique de la Figure 12. Proposer un nom générique pour ces mêmes étapes. 55. D'après le schéma du cycle catalytique, identifier l'étape qui contrôle la stéréosélectivité et préciser s'il s'agit d'énantiosélectivité ou de diastéréosélectivité. 56. Citer le couple oxydo-réducteur dans lequel est impliqué la molécule de propan-2-ol (solvant) dans l'étape (4). Déduire le rôle du propan-2-ol au cours de cette étape. 57. À partir de ce cycle catalytique, déterminer la structure du composé H, sans donner d'importance à la stéréochimie. Le composé K est ensuite préparé en trois étapes selon la séquence réactionnelle de la Figure 13. Le groupement tert-butyldiméthylsilyle (TBS) introduit dans l'étape H ! I est un bon groupement protecteur des alcools, et l'on admettra qu'il n'est pas touché lors des étapes ultérieures. 14 TBSCl H 1) EtMgBr I Imidazole 2) Hydrolyse N Imidazole = CoX 2 / t-BuOOH J C14H 28O3Si NH O O O X= = TBS K Propan-2-ol, O 2 (1 bar) N Si O Figure 13 Formation du squelette bicyclique de l'aplysiallène 58. Donner les structures des composés I, J et K. Préciser le rôle de EtMgBr dans le passage de I à J. La synthèse se poursuit par la fonctionnalisation du bicycle précédemment obtenu, schématisée sur la Figure 14. O ? K O O OTBS Br O H OTBS ylure M + O N' N L Figure 14 Ajout de la chaîne diénique de l'aplysiallène 59. Proposer une séquence réactionnelle permettant de transformer K en L. On pourra utiliser dans cette séquence l'ylure (C6H5)3P=CHCHO qui conduit uniquement au composé de configuration E. Indiquer comment il peut être obtenu à partir de 2-chloroéthanal, en précisant les conditions. 60. Expliciter la structure de l'ylure M qui doit être mis en réaction avec L pour préparer N. 61. Lors de cette conversion, un produit N' de même formule brute que N est obtenu en quantité équivalente. Donner la relation d'isomérie entre N et N'. Sachant qu'il est possible de séparer ces deux derniers composés, proposer une suite de transformations permettant de réutiliser N'. Le composé N est ensuite converti par une séquence réactionnelle non décrite ici en un produit O finalement transformé en ()-aplysiallène en deux étapes décrites sur la Figure 15. OH TrisCl O P Base Br O LiCuBr 2 (-)-Aplysiallène Tris = O S O O Figure 15 Fin de la synthèse du ()-aplysiallène 62. *Sachant que LiCuBr2 est un donneur d'ion bromure Br, proposer un mécanisme pour expliquer la formation du ()-aplysiallène à partir de P, en remarquant que OTris est un analogue d'un groupe partant connu (il n'est pas demandé de discuter la stéréochimie). Pour vérifier que le produit obtenu est bien l'allène souhaité, on étudie la zone 6,5 5,3 ppm de son spectre RMN 1H mesuré à 600 MHz dans le deutériochloroforme (Tableau 4). On indique que sa formule brute obtenue à partir de son spectre de masse haute résolution est C15H18Br2O2. Déplacement Multiplicité Constantes de couplage (Hz) Intégration chimique (ppm) du signal 1 6,41 d J = 11,1 1H 2 6,33 ddd J = 14,6 ; J = 11,1 ; J = 1,2 1H 3 6,09 dd J = 6,0 ; J = 2 1H 4 5,61 dd J = 14,6 ; J = 6,7 1H 5 5,38 dd J = 6,1 ; J = 6,0 1H Tableau 4 Zone 6,5 5,3 ppm du spectre RMN 1H du ()-aplysiallène (d = doublet) Entrée 15 63. En détaillant le raisonnement utilisé, attribuer les différents signaux du Tableau 4 aux protons du ()-aplysiallène concernés, puis indiquer entre lesquels de ces protons ont lieu les couplages observés. Justifier finalement que l'allène bromé désiré a bien été obtenu. Document 6 Données spectroscopiques Tables de spectroscopie RMN 1H Substituant -C=C-H Déplacement chimique 4,5 7,0 R R CH2=C=CH2 CH = 5,9 2,4 2,9 CH2 = 4,8 Déplacements chimiques en RMN du proton (en ppm) (C)n R R R R R H H n > 1, 0 Hz H -CH-O- (cycle à 5) -CH-C=C- 4,6 R R BrCH=C=CH2 R H R H 612 Hz R H H 13 Hz R R R H R H H 68 Hz R O R R R H 1218 Hz 3,5 4,9 H 311 Hz H H R H H R 24 Hz 03 Hz Constantes de couplage typiques en RMN du proton Le couplage proton-proton au-delà de trois liaisons est généralement trop petit pour être détecté (< 1 Hz). Cependant, il existe un certain nombre de situations où ce couplage est présent. Sa valeur peut alors fournir des informations utiles sur la structure du composé étudié. Les couplages passant par des motifs comportant des liaisons de type sont les exemples les plus courants de couplages 4J. On peut citer notamment les couplages allyliques, propargyliques ou encore alléniques. Les couplages sur quatre liaisons dans des systèmes ne comportant que des carbones saturés ou des hétéroatomes sont plus rares et ne sont généralement observés que dans le cas d'un alignement favorable de la chaîne HCCCH (« couplage en W »). Des couplages plus longs (5J et plus) sont aussi parfois observés, particulièrement dans le cas des éthynes et des allènes. H 4J H 4J H H C H = 03 Hz H H H H 4J = 24 Hz 4J = 67 Hz H H = 03 Hz H C H 5J = 08 Hz 5J = 24 Hz H 5J = 23 Hz Exemples de couplages proton-proton lointains : constantes 4J et 5J Données INFRAROUGE Liaison -1 (cm ) O-H C-H C=O C=C 3600 3250 2970 2910 1750 1680 1620 1580 Nombres d'onde de vibration de bandes caractéristiques en IR 16