Mines Chimie PC 2001
| Thème de l'épreuve | Étude de la formation et de la réactivité des alliages du nickel avec le fer et le chrome. Synthèse de la cortisone. |
| Principaux outils utilisés | diagrammes binaires, cristallographie, thermochimie, chimie organique, spectroscopie, réaction de Diels Alder, annellation de Robinson, estérification, oxydation, réduction, hydrogénation |
Corrigé
: 👈 gratuite pour tous les corrigés si tu crées un compte👈 l'accès aux indications de tous les corrigés ne coûte que 5 € ⬅ clique ici
👈 gratuite pour tous les corrigés si tu crées un compte
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
Énoncé complet
(télécharger le PDF)




Rapport du jury
(télécharger le PDF)


Énoncé obtenu par reconnaissance optique des caractères
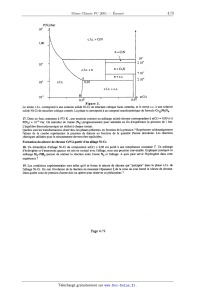
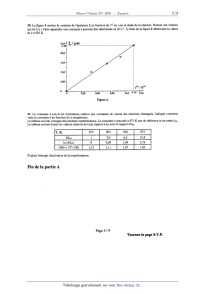
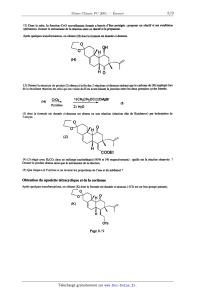
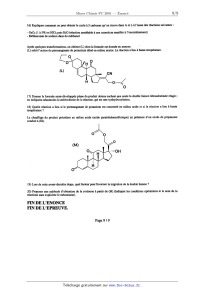
J. 5038 A 2001 Chimie PC ECOLE NATIONALE DESPONTS ET CHAUSSEES. ECOLES. NATIONALES SUPERIEURES DE L'AERONAUTIQUE ET DE L'ESPACE, DES TECHNIQUES AVANCEES, DES TELECOMMUNICATIONS, DES MINES DE PARIS, DES MINES DE SAINT--ETIENNE, DES MINES DE NANCY, DES TELECOMMUNICATIONS DE BRETAGNE. ECOLE POLYTECHNIQUE ( Filière TSI ) CONCOURS D'ADMISSION 2001 EPREUVE DE CHIMIE Filière : PC (Durée de l'épreuve : 4 heures) (L'usage d'ordinateur ou de calculatrice est interdit) Sujet mis à la disposition des concours : Cycle International, ENSTIM,TPE--EIVP. Les candidats sont priés de mentionner de façon apparente sur la première page de la copie : CHIMIE 2001-Filière PC Cet énoncé comporte 9 pages de texte. Si au cours de l'épreuve, un candidat repère ce qui lui semble être une erreur d'énoncé, il le signale sur sa copie et poursuit sa composition en expliquant les raisons des initiatives qu'il est amené à prendre. DEBUT DE DENON CE A QUELQUES PROPRIETES DU NICKEL ET DE SES ALLIAGES I L'élément Nickel. ]. Le nickel a pour numéro atomique Z = 28. Donner la configuration électronique de l'atome de nickel dans son état fondamental, et de l'ion nickel...) à l'état gazeux. 2. Comment évoluent les énergies des orbitales 3d lorsque l'ion nickel(ll) est engagé dans un complexe octaédriqne ? Justifier par l'utilisation de la théorie du champ cristallin. 3. Préciser la répartition des électrons 3d du nickel(ll) dans un complexe octaédrique. Peut--on savoir par des mesures magnétiques si, dans le cas d'un complexe octaédriqne du nickel(ll), le ligand exerce un champ fort ou un champ faible '? Justifier. II Alliages Fer--Nickel. Variétés allotropiques du fer. Le fer Solide existe sous plusieurs variétés cristallines, selon la température. Le tableau suivant donne les variétés stables sous la pression standard. Tournez la page S.V.P. 4. Représenter les structures cubiques faces centrées (c.f.c., aussi notée Cp) et cubiques centrées (c.c., aussi notée C:). Quelle est la coordinence pour un atome de fer dans chaque structure ? 5. Définir la compacité X d'une structure. Donner une expression littérale de la compacité de chaque structure X(c.f.c.) et X(c.f.c.) X(c.c.) Données: x/î =1,4; @ =1,7. X(c.c.). Calculer le rapport 6. On considère un échantillon de fer, sous la pression standard, à 910 °C. Quel est l'effet d'une augmentation de pression selon que le fer est sous la forme a ou y ? Domaines de miscibilité à l'état solide. La figure 1 représente le diagramme de phases isobare liquide-solide d'un système à deux constituants A et B. La miscibilité est totale à l'état liquide et nulle à l'état solide. Un composé défini à l'état solide est présent. T Figure 1. 7. Que représentent les points C, D, E, F, et G ? Quelle est la formule du composé défini ? Dans un tableau indiquer les phases présentes dans les différents domaines ], 2,. . ...7. 8. À l'état solide, le nickel de structure c.f.c. est miscible avec le fer 7, (il forme avec le fer une phase 7) et légèrement soluble dans le fer a (une phase oc est formée). Les rayons métalliques du fer et nickel sont sensiblement égaux. Les alliages fer-nickel formés sont-ils des alliages d'insertion ou de substitution ? La figure 2 représente le diagramme de phases isobare simplifié solide--solide du système fer--nickel. Ce diagramme présente des analogies avec le précédent : la phase liquide est remplacée par la phase solide 7 (phase cfc) . De nouveaux domaines apparaissent du fait, d'une part, de la solubilité partielle du nickel dans le fer a, et d'autre part de la formation du composé défini FeNi3, dans lequel le fer et le nickel présentent une certaine solubilité. 9. Indiquer la (les) phase(s) présente(s) dans les domaines 1, 2 et 3 de la figure 2. Page2/9 X(N i) Figure 2. 10. Les courbes AC et AB sont supposées rectilignes. On utilise, àla température de 800°C, l mole d'un alliage Fer--Nickel dont la fraction molaire en nickel est de 0,25. On laisse refroidir l'alliage jusqu'à la température de 300 °C, suffisamment lentement pour que s'établisse à chaque instant l'équilibre thermodynamique. Cette expérience est réalisée sous la pression standard. . Quelles sont les transformations observées et les phases présentes, en fonction de la température '? Si nécessaire, le candidat fera un schéma sur sa copie. 11. La température de 345°C joue un rôle particulier. Calculer la variance du système à cette température. Que peut--on en conclure ? 12. Quelles sont les phases en présence, et leurs quantités de matière, lorsque le point représentatif du système atteint le segment BC en venant du domaine 1 ? 13. Quelles sont les phases en présence, et leurs quantités de matière, lorsque le point représentatif du système quitte le segment BC en allant dans le domaine 3 ? Alliages N ickel--Chmme, en présence d'azote. Dans cette partie, les alliages Ni-Cr sont surmontés par de l'azote gazeux. La figure 3 montre un diagramme de phases isotherme, tracé à la température de 973 K. Les domaines des différentes phases solides sont indiqués en fonction de la pression de l'azote, et de la fraction métallique en chrome u(Cr). La fraction métallique en chrome est définie par le rapport : _ u(Cr) u(Cr)--W où n est la quantité de matière. 14. Calculer la fraction métallique en chrome u(Cr) pour la phase n. 15. Expliquer pourquoi le point A correspond à une teneur u(Cr) supérieure à celle du point B. 16. D'après le diagramme, quelle est la structure cristalline du chrome pur ? Page 3 / 9 _ Tournez la page S.V.P. P(N,)lbar 10" c.f.c. + CrN 1,00 1: + CrN ' 10"3 --- .. 10"' 2 10 7 10"7 n + c.c. 8 _8 2 10" 10 c.f.c. 0,39 10" B u(Cr) 0,3 09 Figure 3. Le terme c.f.c. correspond à une solution solide Ni-Cr de structure cubique faces centrées, et le terme c.c. à une solution solide N i-Cr de structure cubique centrée. La phase 7: correspond à un composé stoechiométrique de formule Crl3Ni7N4. 17. Dans un four, maintenu à 973 K , une enceinte contient un mélange nickel-chrome correspondant à u(Cr) : 0,80 et à P(N2) : 1010 bar. On introduit de l'azote (NZ) progressivement pour atteindre en fin d'expérience la pression de 1 bar. L'équilibre thermodynamique est réalisé à chaque instant. Quelles sont les transformations observées, les phases présentes, en fonction de la pression ? Représenter schématiquement l'allure de la courbe représentant la pression de diazote en fonction de la quantité d'azote introduite. Les réactions chimiques utilisées pour le raisonnement devront être explicitées. Formation du nitrure de chrome CrN à partir d'un alliage Ni-Cr. 18. Un échantillon d'alliage Ni--Cr de composition u(Cr) : 0,05 est porté à une température constante T. Un mélange d'hydrogène et d'ammoniac gazeux est mis en contact avec l'alliage, sous une pression convenable. Expliquer pourquox ce mélange H2--NH3 permet de réaliser la réaction entre l'azote N2 et l'alliage. A quoi peut servir l'hydrogène dans cette expérience ? 19. Les conditions expérimentales sont telles qu'il se forme le nitrure de chrome qui "précipite" dans la phase c.f.c. de l'alliage N i-Cr. On suit l'évolution de la réaction en mesurant l'épaisseur & de la zone où s'est formé le nitrure de chrome. Dans quelle zone de pression d'azote doit--on opérer pour observer ce phénomène ? Page4/9 20. La figure 4 montre la variation de l'épaisseur & en fonction de t"2 où test la durée de la réaction. Donner une relation qui lie & à t. Faire apparaître une constante k pouvant être déterminée en m2--s". À l'aide de la figure 4 déterminer la valeur de IC à 903 K. 0 3,00 6,00 9,00 12,0 " 14 15,0 Figure 4. 21. La constante k suit la loi d'Arrhénius relative aux constantes de vitesse des réactions chimiques. Indiquer comment varie la constante k en fonction de la température. Le tableau suivant consigne des résultats expérimentaux. La constante k mesurée à 873 K sert de référence et est notée koef. Le tableau suivant donne les valeurs relatives de k par rapport à koef avec le rapport k/koef. ...... Évaluer l'énergie d'activation de la transformation. Fin de la partie A Page 5 / 9 Tournez la page S.V.P. B -- LA CORTISONE La Cortisone : une hormone corticosurrénale aux propriétés anti--inflammatoires. La cortisone (A) appartient à la famille des stéroïdes (produits naturels tétracycliques dotés d'une puissante activité physiologique) comme le cholestérol par exemple. C'est l'une des hormones sécrétée par la partie externe (cortex) des glandes surrénales. Une synthèse de cette hormone, amplement utilisée dans le traitement des inflammations rhumatismales, est proposée par Woodward (un très grand nom de la chimie organique) en 1951. Dans ce problème, nous examinerons quelques aspects de cette synthèse. (A) I - Présentation de la molécule 1) Donner le nombre d'insaturations de la molécule de cortisone. 2) Les carbones numérotés 9, 13 et 17 sont asymétriques. Donner leur configuration à l'aide des règles de Cahn, Ingold et Prelog, en justifiant. Indiquer quels autres carbones sont aussi asymétriques et combien de stéréoisomères sont associés àla formule plane de la cortisone. 3) Quelles bandes caractéristiques sont attendues en spectroscopie LR. ? Prévoir la position de la bande responsable de l'élongation de la liaison C=O conjuguée par rapport à celles associées aux autres liaisons C=O. II - Quelques aspects dela synthèse proposée par Woodward Obtention d'un composé bicyclique L'action du diène (B) sur la quinone (C) pendant 12 heures à température ambiante conduit à plusieurs composés. On s'intéresse ici aux seuls composés bicycliques. Les formules sont données ci-dessous. ? DE (B) \ (C) ... \ | O Page6/9 4) Donner le nom de la réaction observée et dessiner le mouvement des électrons. 5) En examinant les effets électroniques des groupements (-CHs,-C----O et -OCHzCH3) indiquer quelle(s) orbitale (s) est (sont) à considérer pour chaque réactif. Qualifier chaque réactif de nucléophile ou d'électrophila 6) Donner la formule semi--développée plane des composés attendus, sur, le modèle de A ; compte tenu de la stéréochimie de la réaction entre (B) et (C), combien de stéréoisomères sont attendus ? Dans la suite, dans un souci de simplification, on ne s'intéressera qu'à l'un de ces stéréoisomères. L'hydrogénaüon contrôlée de ce composé sur nickel (pression faible en Hz) conduit à (D) dont la formule est donnée ci--dessous. (D) 7) Quel est le rôle du nickel ? 8) Pourquoi est--il nécessaire de contrôler la réaction ? Dans l'étape suivante, (D) est soumis à l'action de LiAlH4 dans du tétrahydrofurane et à température ambiante. 9) Quelle est la réaction qui a lieu ? 10) Donner la formule semi-développée" du produit majoritaire E obtenu après hydrolyse, sachant que le groupement méthyl encombre la face avant et gène l'approche de LiAlH4. Obtention du squelette tricyclique Par une réaction simple, on passe de (E) à (F) dont la formule est donnée ci--dessous (il n'est pas nécessaire de connaître la nature de R). (F) chauffé dans l'éthanol en présence d'une base forte réagit avec la but--l-èn--3--one pour donner (G) au squelette tricyclique. Cette réaction porte le nom d'annulation (ou annellation) de Robinson. 11) Proposer un mécanisme pour cette réaction, qui enchaîne addition nucléophile, cétolisatîon et crotonisation ; pour simplifier l'écriture, on décrira la transformation : r°+%_. Page 7 l 9 Tournez la page S.V.P. 12) Dans la suite, la fonction--C=O nouvellement formée a besoin d'être protégée ; proposer un réactif et ses conditions opératoires. Donner le mécanisme de la réaction entre ce réactif et la propanone. Après quelques transformations, on obtient (H) dont la formule est donnée ci-dessous. [ 0 0 (H) \ 13) Donner la structure du produit (I) obtenu à la fin des 2 réactions ci--dessous sachant que le carbone de (H) impliqué lors de la deuxième réaction est celui qui est voisin du H en avant faisant la jonction entre les deux premiers cycles formés. Cr03 1 )CH36 HZOC£--CMQBr (H) ----------- ___--___. ... Pyridine 2) H20 (J) dont la formule est donnée ci--dessous est obtenu en une réaction (réaction dite de Kutcherov) par hydratation de l'alcyne. 14) (J ) réagit avec KzC03 dans un mélange eau/méthanol (95% et 5% respectivement) : quelle est la réaction observée ? Donner le produit obtenu ainsi que le mécanisme de la réaction. 15) Que risque-t--il d'arriver si on inverse les proportions de l'eau et du méthanol ? Obtention du squelette tétracyclique et de la cortisone Après quelques transformations, on obtient (K) dont la formule est donnée ci--dessous (-OTs est un bon groupe partant). C° " 0 (K) 16) Expliquer comment on peut obtenir le cycle à 5 carbones qu'on trouve dans A et L à l'issue des réactions suivantes : - 0804 (l à 5%) et HID4 puis HzO (réaction semblable à une ozonolyse sensible à l'encombrement) - Méthanolate de sodium dans du méthanol Après quelques transformations, on obtient (L) dont la formule est donnée en annexe. (L) subit l'action du permanganate de potassium dilué en milieu neutre. La réaction a lieu à basse température. CO° (L) 17) Donner la formule semi-développée plane du produit obtenu sachant que seule la double liaison tétrasubstituée réagit ; on indiquera néanmoins la stéréochimie de la réaction, qui est une synhydroxylation. 18) Quelle réaction a lieu si le permanganate de potassium est concentré en milieu acide et si la réaction a lieu à haute température '? Le chauffage du produit précédent en milieu acide (acide pæatoluènesulfonique) en présence d'un excès de propanone conduit à (M). 19) Lors de cette avant--demière étape, quel facteur peut favoriser la migration de la double liaison ? 20) Proposer une méthode d'obtention de la cortisone à partir de (M) (Indiquer les conditions opératoires et le nom de la réactions sans expliciter le mécanisme). FIN DE L'ENONCE _ FIN DE L'EPREUVE. Page 9-- I 9